-
研究NO的性质对建设美丽家乡,打造宜居环境具有重要意义。
(1)自然界在闪电时,生成NO的反应方程式为__________________。
(2)T℃时在容积为2L的恒容密闭容器中,充入NO和O2发生反应:2NO(g)+O2(g)⇌2NO2(g),不同时刻测得容器中n(NO)、n(O2)如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
| n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
①在T℃下,0~2s时,该反应的平均反应速率 =________;
=________;
②该温度下反应的平衡常数K=________,在T℃下,能提高NO的平衡转化率的措施有_______、________。
(3)已知NO和O2反应的历程如图,回答下列问题:
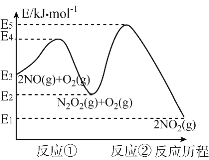
①写出其中反应①的热化学方程式也(△H用含物理量E的等式表示):________。
②试分析上述基元反应中,反应①和反应②的速率较小的是_____(选填“反应①”或“反应②”);已知反应①会快速建立平衡状态,反应②可近似认为不影响反应①的平衡。对该反应体系升高温度,发现总反应速率变慢,其原因可能是____________。
-
“绿水青山就是金山银山”,研究氮氧化物等大气污染物对建设美丽家乡,打造宜居环境具有重要意义。NO在空气中存在如下反应:2NO(g)+ O2(g) 2NO2(g)△H上述反应分两步完成,如下左图所示。
2NO2(g)△H上述反应分两步完成,如下左图所示。
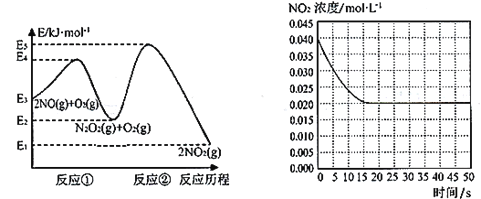
(1)写出反应①的热化学方程式(△H用含物理量E的等式表示):________。
(2)反应①和反应②中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g) 2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
(3)某温度下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如上图所示。前5秒内O2的平均生成速率为_______;该温度下反应2NO+O2 2NO2的化学平衡常数K为_____。
2NO2的化学平衡常数K为_____。
(4)对于(3)中的反应体系达平衡后(压强为P1),若升高温度,再次达平衡后,混合气体的平均相对分子质量_____(填“增大”、“减小”或“不变”);若在恒温恒容条件下,向其中充入一定量O2,再次达平衡后,测得压强为P2,c(O2)=0.09mol·L-1,则P1︰P2=___________。
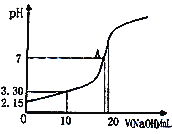
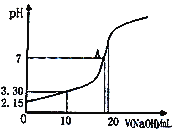
(5)水能部分吸收NO和NO2混合气体得到HNO2溶液。若向20.00mL0.10mol·L-1HNO2溶液中逐滴加入0.10mol·L-1NaOH溶液,所得pH曲线如图所示,则A点对应的溶液c(Na+)/c(HNO2)=____。
-
“绿水青山就是金山银山”,研究氮氧化物等大气污染物对建设美丽家乡,打造宜居环境具有重要意义。NO在空气中存在如下反应:2NO(g)+ O2(g) 2NO2(g)△H上述反应分两步完成,如下左图所示。
2NO2(g)△H上述反应分两步完成,如下左图所示。

(1)写出反应①的热化学方程式(△H用含物理量E的等式表示):________。
(2)反应①和反应②中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g) 2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
2NO2(g)反应速率的是____(填“反应①”或“反应②”);对该反应体系升高温度,发现总反应速率变慢,其原因可能是____(反应未使用催化剂)。
(3)某温度下一密闭容器中充入一定量的NO2,测得NO2浓度随时间变化的曲线如上图所示。前5秒内O2的平均生成速率为_______;该温度下反应2NO+O2 2NO2的化学平衡常数K为_____。
2NO2的化学平衡常数K为_____。
(4)对于(3)中的反应体系达平衡后(压强为P1),若升高温度,再次达平衡后,混合气体的平均相对分子质量_____(填“增大”、“减小”或“不变”);若在恒温恒容条件下,向其中充入一定量O2,再次达平衡后,测得压强为P2,c(O2)=0.09mol·L-1,则P1︰P2=___________。
(5)水能部分吸收NO和NO2混合气体得到HNO2溶液。若向20.00mL0.10mol·L-1HNO2溶液中逐滴加入0.10mol·L-1NaOH溶液,所得pH曲线如图所示,则A点对应的溶液c(Na+)/c(HNO2)=____。
-
习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水”。 消除大气和水体污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)以HCl为原料,用O2氧化制取Cl2可提高效益,减少污染。
反应为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) △H=-118.4 kJ/mol,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g)+2H2O(g) △H=-118.4 kJ/mol,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
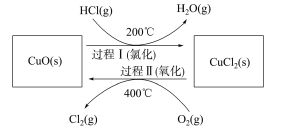
过程I的反应为:2HCl(g)+CuO(s)=CuCl2(s)+H2O(g) △H =-120. 4 kJ•mol-1,过程II反应的热化学方程式为__________________。
(2)CO还原法处理NO:原理为 2CO(g)+2NO(g)=N2(g)+2CO2 (g) △H =-744 kJ•mol-1。在容积为2 L的某密闭容器中充入5 mol CO和4 mol NO,发生该反应。某温度下,上述反应进行到5 min时放出的热量为558 kJ,则N2的平均反应速率v(N2)=_______mol•L-1• min-1。
(3)热分解法处理N2O:某温度下,N2O在金粉表面发生热分【解析】
2N2O(g)=2N2(g)+O2(g),测得c(N2O)随时间t变化关系如图1所示。已知瞬时反应速率v与c(N2O)的关系为v=kcnc(N2O) (k是反应速率常数),则n=________,k=_____________。
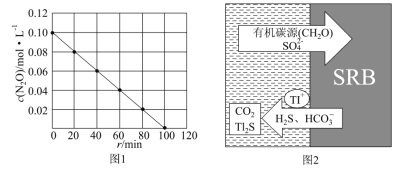
(4)铊为重金属元素,对水体污染严重,通过沉淀法可以去除工业废水中的Tl+。
①利用硫酸盐还原菌(SRB)的催化作用,可以将废水中有机碳源(以CH2O表示)、SO42-、Tl+去除(原理如图2所示)。写出该反应的离子反应方程式_____________________。
②工业污水铊的污染物排放限值为2. 5×10-8 mol•L-1。已知:Ksp(Tl2S) =5×10-21,若铊的含量符合国家排放限值,则处理后的废水中c(S2-)≥______________。
-
治理大气和水体污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)CO泄漏会导致人体中毒,用于检测CO的传感器的工作原理如图所示:写出电极I上发生的反应式:__。

工作一段时间后溶液中H2SO4的浓度__(填“变大”、“变小”或“不变”)
(2)用O2氧化HCl制取Cl2,可提高效益,减少污染。反应为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ∆H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
2Cl2(g)+2H2O(g) ∆H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
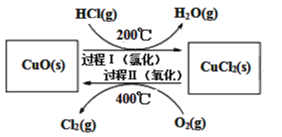
过程I的反应为:2HCl(g)+CuO(s) CuCl2(s)+H2O(g) ∆H1
CuCl2(s)+H2O(g) ∆H1
过程II反应的热化学方程式(∆H2用含有∆H和∆H1的代数式表示)__。
(3)在温度T0℃,容积为1L的绝热容器中,充入0.2molNO2,发生反应:2NO2(g) N2O4(g) ∆H<0,容器中NO2的相关量随时间变化如图所示。
N2O4(g) ∆H<0,容器中NO2的相关量随时间变化如图所示。
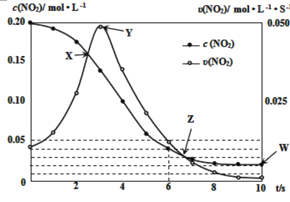
①反应到6s时,NO2的转化率是__。
②根据图示,以下各点表示反应达到平衡状态的是__。
a.X b.Y c.Z d.W
③0~3s内容器中NO2的反应速率增大,而3s后容器中NO2的反应速率减小了,原因是__。
④此容器中反应达平衡时,温度若为T1℃,此温度下的平衡常数K═__。
(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1mol•L-1的Na2SO3溶液吸收SO2,当溶液pH═7时,溶液中各离子浓度的大小关系为:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)═c(OH-)。(已知25℃时:H2SO3的电离常数Ka1═1.3×10-2,Ka2═6.2×10-8)请结合所学理论通过计算说明c(HSO3-)>c(SO32-)的原因___。
-
消除含氮、硫等化合物的污染对建设美丽家乡,打造宜居环境具有重要意义。
I.用NH3催化还原NOx可以消除氮氧化物的污染,NOx若以NO为例,在恒容容器中进行反应:4NH3(g)+6NO(g)  5N2(g)+6H2O(g) ΔH<0。
5N2(g)+6H2O(g) ΔH<0。
(1)以下选项可以判断反应达到平衡状态的是_______。
A..4v正(NH3)=5v逆(N2) B.反应体系中气体密度不变
C..反应体系中气体压强不变 D.反应体系中气体平均摩尔质量不变
(2)图I中曲线表示转化率与反应时间的关系。若改变起始条件,使反应过程由a状态转为b状态进行,可采取的措施是_______
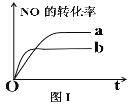
A.降低温度 B.增大反应物中NO的浓度
C.加催化剂 D.向密闭容器中通入氩气
II.燃煤烟气中含有大量SO2和NO。某科研小组研究臭氧氧化的碱吸收法同时脱除SO2和NO工艺,反应进程如图II所示。
反应1:NO(g)+O3(g) NO2(g)+O2(g)
NO2(g)+O2(g)
反应2:SO2(g)+O3(g) SO3(g)+O2(g)
SO3(g)+O2(g)
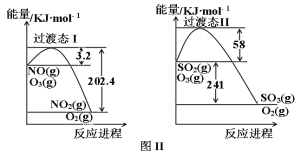
已知该体系中温度80℃以上臭氧发生分解反应:2O3 3O2。且100℃时臭氧的分解率约为10%。请回答:
3O2。且100℃时臭氧的分解率约为10%。请回答:
(1)写出反应1的热化学方程式_______,反应1在高温下不能自发进行,则该反应的熵变ΔS_______0(填“大于”或“小于”)。
(2)其他条件不变,向五个体积固定为1L的密闭容器中均充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0mol O3,在不同温度下反应相同时间后体系中NO和SO2的转化率如图所示:
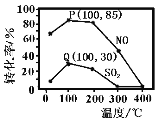
①若P、Q两点为非平衡点,试分析P点转化率大于Q点的可能原因_______。100℃,t秒时反应1进行到P点,反应从开始到t秒时NO的平均速率v(NO)=_______mol·L−1·s−1(用含t的式子表示)。
②若Q点为平衡点,100℃下反应2的平衡常数的数值约为_______(精确到0.01)。
-
习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁” 。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)以HCl为原料,用O2氧化制取Cl2,可提高效益,减少污染。反应为:4HCl(g) + O2(g) 2Cl2(g) + 2H2O(g) ∆H ═ -115.4 kJ•mol-1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g) + 2H2O(g) ∆H ═ -115.4 kJ•mol-1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
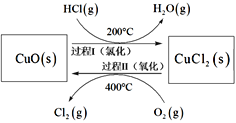
过程I的反应为:2HCl(g) + CuO (s) CuCl2(s) + H2O(g) ∆H1 ═ -120.4 kJ•mol-1,过程II反应的热化学方程式为___________。
CuCl2(s) + H2O(g) ∆H1 ═ -120.4 kJ•mol-1,过程II反应的热化学方程式为___________。
(2)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g)  N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。
N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。
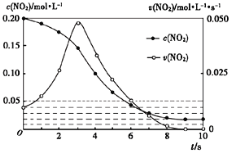
①0~3s内,甲容器中NO2的反应速率增大的原因是______________________。
②甲达平衡时,温度若为T℃,此温度下的平衡常数K═____________________。
③平衡时,K甲_____K乙,P甲_____P乙(填“>”、“<”或“=”)。
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①可用次氯酸钠除去氨氮,同时产生一种大气组成的气体。写出总反应化学方程式:___________。
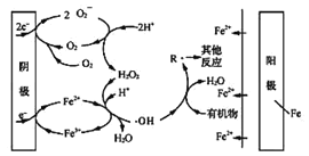
②EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图所示。则阴极附近Fe2+参与反应的离子方程式为______。

(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1 mol• L -1的Na2SO3溶液吸收SO2,当溶液pH═7时,溶液中各离子浓度的大小关系为_________________。(已知25℃时:H2SO3的电离常数Ka1═1.3×10-2,Ka2═6.2×10-8)
-
习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁” 。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)以HCl为原料,用O2氧化制取Cl2,可提高效益,减少污染。反应为:4HCl(g) + O2(g) 2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:

过程I的反应为:2HCl(g) + CuO (s) CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程II反应的热化学方程式为___________。
CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程II反应的热化学方程式为___________。
(2)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g)  N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。
N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。

①0~3s内,甲容器中NO2的反应速率增大的原因是______________________。
②甲达平衡时,温度若为T℃,此温度下的平衡常数K=____________________。
③平衡时,K甲_____K乙,P甲_____P乙(填“>”、“<”或“=”)。
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①可用次氯酸钠除去氨氮,同时产生一种大气组成的气体。写出总反应化学方程式:___________。
②EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图所示。则阴极附近Fe2+参与反应的离子方程式为______。
(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1 mol· L −1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为_________________。(已知25℃时:H2SO3的电离常数Ka1=1.3×10−2,Ka2=6.2×10−8)
-
习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁”。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)以HCl为原料,用O2氧化制取Cl2,可提高效益,减少污染。反应为:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g) ∆H=−115.4kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g)+2H2O(g) ∆H=−115.4kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
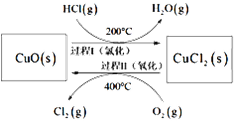
过程I的反应为:2HCl(g)+CuO(s) CuCl2(s)+H2O(g) ∆H1=−120.4kJ·mol−1,过程II反应的热化学方程式为___。
CuCl2(s)+H2O(g) ∆H1=−120.4kJ·mol−1,过程II反应的热化学方程式为___。
(2)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g) N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。
N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。

①0~3s内,甲容器中NO2的反应速率增大的原因是___。
②甲达平衡时,温度若为T℃,此温度下的平衡常数K=__。
③平衡时,K甲__K乙,P甲__P乙(填“>”、“<”或“=”)。
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。可用次氯酸钠除去氨氮,同时产生一种大气组成的气体。写出总反应化学方程式:__。
(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1mol·L-1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为___。(已知25℃时:H2SO3的电离常数Ka1=1.3×10−2,Ka2=6.2×10−8)
-
控制含碳、氮、硫的化合物等大气污染物对打造宜居环境具有重要意义。
(1)已知反应 的
的 分子中化学键断裂时分别需要吸收
分子中化学键断裂时分别需要吸收 的能量,则
的能量,则 分子中化学键断裂时需要吸收的能量为______kJ。
分子中化学键断裂时需要吸收的能量为______kJ。
(2)用 消除
消除 污染的反应原理如下:
污染的反应原理如下: ,不同温度条件下,
,不同温度条件下, 与NO的物质的量之比分别为
与NO的物质的量之比分别为 时,得到
时,得到 脱除率曲线如图所示:
脱除率曲线如图所示:
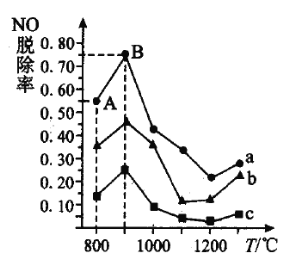
曲线 对应
对应 与
与 的物质的量之比是_______。
的物质的量之比是_______。
②曲线 中
中 的起始浓度为
的起始浓度为 ,从
,从 点到
点到 点经过
点经过 ,该时间段内
,该时间段内 的脱除速率为_________________
的脱除速率为_________________ 。
。
(3)已知常温下电离平衡常数: 的
的 的
的 。
。
①溶液中下列微粒可以大量共存的是___________(填字母)。
a. b.
b. c.
c.
②常温下,某种碳酸钠与碳酸氢钠混合溶液的 ,则
,则 _____________。
_____________。
(4)利用电解法处理高温空气中稀薄的 (
( 浓度约为
浓度约为 的10倍),装置示意图如图所示,固体电解质可传导
的10倍),装置示意图如图所示,固体电解质可传导 。
。
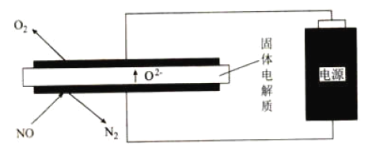
①阴极的电极反应式为_______________。
②消除一定量的 所消耗的电量远远大于理论计算量,可能的原因是(不考虑物理因素)__________。
所消耗的电量远远大于理论计算量,可能的原因是(不考虑物理因素)__________。
=________;








 2Cl2(g)+2H2O(g) ∆H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
2Cl2(g)+2H2O(g) ∆H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:













