-
二甲醚和乙醇是两种常见的有机溶剂,也可作为新能源。
(1)通过以下反应可获得二甲醚(CH3OCH3):
①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH 1=a kJ·molˉ1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH 2=b kJ·molˉ1
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH 3=c kJ·molˉ1
则反应 2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的 ΔH=_________kJ·molˉ1。
(2)已知气相直接水合法可以制取乙醇:H2O(g)+C2H4(g)  CH3CH2OH(g)。
CH3CH2OH(g)。
在 n(H2O)∶n(C2H4)=1∶1 的条件下投料,乙烯的平衡转化率与温度(T)及压强(p) 的关系如图1所示。
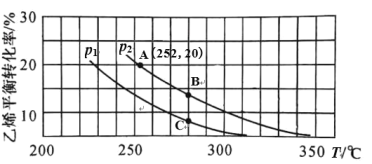 图1
图1
①下列有关说法中正确的是_________。
A.p1>p2 B.280℃时,vB>vC
C.A、B、C 三点的平衡常数 KA>KB>KC D.低温有利于该反应自发进行
②在 p2,280℃条件下,C 点的 v 正 ____v 逆 (填“>”、“<”或“=”),理由是________。
③计算图 1 中 A 点的平衡常数 Kp=_________。(结果用 p2 的代数式表示,平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)在 n(H2O)∶n(C2H4)=1∶x 的条件下投料,某研究小组在压强为 p2,温度为 252℃ 时,进行平衡体系中乙醇的体积分数随投料比变化的测定实验。在图 2 中画出平衡体系中乙醇的体积分数 φ 随 x 变化的示意图____。

-
通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是
①C(s) + H2O(g)==CO(g) + H2 (g) ΔH1 = akJ·mol−1
②CO(g) + H2O(g)==CO2(g) + H2 (g) ΔH2 = bkJ·mol−1
③CO2 (g) + 3H2 (g)==CH3OH(g) + H2O(g) ΔH3 = ckJ·mol−1
④2CH3OH(g)==CH3OCH3 (g) + H2O(g) ΔH4 = dkJ·mol−1
A. 反应①、②为反应③提供原料气
B. 反应③也是CO2资源化利用的方法之一
C. 反应CH3OH(g)== CH3OCH3 (g) +
CH3OCH3 (g) + H2O(l)的ΔH =
H2O(l)的ΔH = kJ·mol−1
kJ·mol−1
D. 反应2CO(g) + 4H2 (g)==CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol−1
-
通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是
①C(s) + H2O(g) CO(g) + H2 (g) ΔH1 = a kJ·mol-1
CO(g) + H2 (g) ΔH1 = a kJ·mol-1
②CO(g) + H2O(g) CO2 (g) + H2 (g) ΔH 2 = b kJ·mol-1
CO2 (g) + H2 (g) ΔH 2 = b kJ·mol-1
③CO2 (g) + 3H2 (g) CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol-1
CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol-1
④2CH3OH(g) CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol-1
CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol-1
A. 反应①、②为反应③提供原料气
B. 反应③也是 CO2资源化利用的方法之一
C. 反应CH3OH(g)
 CH3OCH3 (g) +
CH3OCH3 (g) + H2O(l)的ΔH =
H2O(l)的ΔH = kJ·mol-1
kJ·mol-1
D. 反应 2CO(g) + 4H2 (g)  CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol-1
CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol-1
-
通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s) + H2O(g)==CO(g)+H2(g) ΔH1=a kJ•mol-1
②CO(g) + H2O(g)==CO2(g)+H2(g) ΔH2=b kJ•mol-1
③CO2(g)+3H2(g)==CH3OH(g)+H2O(g) ΔH3 =c kJ•mol-1
④2CH3OH(g) ==CH3OCH3(g)+H2O(g) ΔH4=d kJ•mol-1
A. 反应①②为反应③提供原料气
B. 反应③也是CO2资源化利用的方法之一
C. 反应CH3OH(g)==  CH3OCH3(g)+
CH3OCH3(g)+  H2O(1)的ΔH =
H2O(1)的ΔH = kJ•mol-1
kJ•mol-1
D. 反应 2CO(g)+4H2(g) ==CH3OCH3(g)+H2O(g)的ΔH= (2b+2c+d) kJ•mol-1
-
通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s)+H2O(g)=CO(g)+H2(g) △H1=akJ/mol
②CO(g)+H2O(g)=CO2(g)+H2(g) △H2=bkJ/mol
③CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3=ckJ/mol
④2CH3OH(g)=CH3OCH3(g)+H2O(g) △H4=dkJ/mol
A. 反应①、②为反应③提供原料气,且a>0
B. 反应③也是CO2资源化利用的方法之一
C. 反应CH3OH(g)=1/2CH3OCH3(g)+1/2H2O(g) △H=d/2kJ/mol
D. 反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的△H=-(2b+2c+d)kJ/mol
-
通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s)+H2O(g)==CO(g)+H2(g) ΔH1=akJ/mol
②CO(g)+H2O(g)==CO2(g)+H2(g) ΔH2=bkJ/mol
③CO2(g)+3H2(g)==CH3OH(g)+H2O(g) ΔH3=ckJ/mol
④2CH3OH(g)==CH3OCH3(g)+H2O(g) ΔH4=dkJ/mol
A. 反应①、②为反应③提供原料气,且a>0
B. 反应③也是CO2资源化利用的方法之一
C. 反应CH3OH(g)==1/2CH3OCH3(g)+1/2H2O(g)的ΔH=d/2kJ/mol
D. 反应2CO(g)+4H2(g)==CH3OCH3(g)+H2O(g)的ΔH=-(2b+2c+d)kJ/mol
-
[2017江苏]通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是
①C(s) + H2O(g) CO(g) + H2 (g) ΔH1 = a kJ·mol−1
CO(g) + H2 (g) ΔH1 = a kJ·mol−1
②CO(g) + H2O(g) CO2 (g) + H2 (g) ΔH 2 = b kJ·mol−1
CO2 (g) + H2 (g) ΔH 2 = b kJ·mol−1
③CO2 (g) + 3H2 (g) CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol−1
CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol−1
④2CH3OH(g) CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol−1
CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol−1
A.反应①、②为反应③提供原料气
B.反应③也是CO2资源化利用的方法之一
C.反应CH3OH(g)
 CH3OCH3 (g) +
CH3OCH3 (g) + H2O(l)的ΔH =
H2O(l)的ΔH = kJ·mol−1
kJ·mol−1
D.反应 2CO(g) + 4H2 (g) CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol−1
CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol−1
-
二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
I.CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
II.2CH3OH(g)===CH3OCH3(g)+H2O(g)
(1)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为_______反应(填“吸热”或“放热”)。
(2)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是______________(填“a”或“b”)。
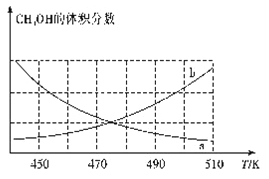
②下列说法能表明反应已达平衡状态的是____(填标号)。
A.容器中气体的压强不再变化 B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化 D.v正(H2)=2v正(CH3OH)
(3)500K时,在2L密闭容器中充入4 mol CO和8 mol H2,4 min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3) ,则:
① 0~4 min,反应I的v(H2)=______,反应I的平衡常数K=______。
② 反应II中CH3OH的转化率α=_______。
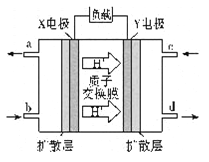
(4)二甲醚燃料电池的工作原理如图听示,则X电极的电极反应式为_______。用该电池对铁制品镀铜,当铁制品质量增加64 g时,理论上消耗二甲醚的质量为_______g(精确到0.01)。
-
二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
I.CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
II.2CH3OH(g)===CH3OCH3(g)+H2O(g)
(1)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为_______反应(填“吸热”或“放热”)。
(2)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是______________(填“a”或“b”)。
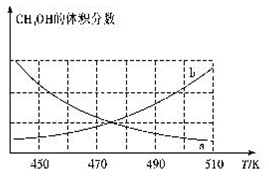
②下列说法能表明反应已达平衡状态的是____(填标号)。
A.容器中气体的压强不再变化 B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化 D.v正(H2)=2v正(CH3OH)
(3)500K时,在2L密闭容器中充入4 mol CO和8 mol H2,4 min达到平衡,平衡时CO的转化率为80%,且2c(CH3OH)=c(CH3OCH3) ,则:
① 0~4 min,反应I的v(H2)=______,反应I的平衡常数K=______。
② 反应II中CH3OH的转化率α=_______。
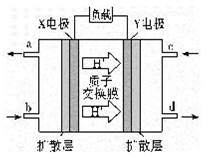
(4)二甲醚燃料电池的工作原理如图听示,则X电极的电极反应式为_______。用该电池对铁制品镀铜,当铁制品质量增加64 g时,理论上消耗二甲醚的质量为_______g(精确到0.01)。
-
开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)催化反应室中的总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K=
CH3OCH3(g)+CO2(g),计算△H=___。反应原料来自煤的气化。已知该反应的平衡常数表达式为K= ,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
,每生成1molH2需要吸收131.3kJ的热量。写出该反应的热化学方程式___。
(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L-1,c(H2)=1.4mol·L-1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为___。
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L-1) | 0.46 | 1.0 | 1.0 |
此时刻v正___v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___。
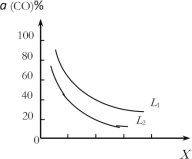
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)
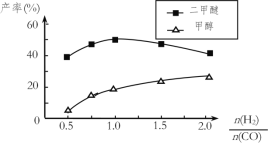
(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:__。
CH3CH2OH(g)。
 图1
图1




