-
实验室中需要22.4L(标准状况)SO2气体。化学小组依据化学方程
Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后,取65g锌粒与质量分数为98%的浓硫酸(密度
ZnSO4+SO2↑+2H2O计算后,取65g锌粒与质量分数为98%的浓硫酸(密度 )110mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
)110mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是 (填分子式)。产生这种结果的主要原因是 (用化学方程式和必要的文字加以说明)
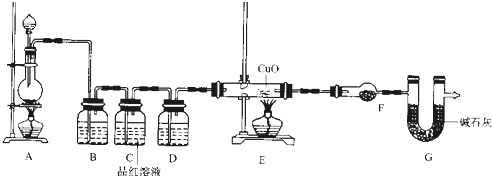
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。

①装置B中加入的试剂 ,作用是 。
②装置D加入的试剂 ,装置F加入的试剂 。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是 。
④U型管G的作用为 。
-
实验室中需要22.4l(标准状况)SO2气体.化学小组同学依据化学方程式Zn+2H2SO4(浓)
 ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质.
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质.
(1)化学小组所制得的气体中混有的主要杂质气体可能是______(填分子式).产生这种结果的主要原因是______
(用化学方程式和必要的文字加以说明)
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究.
①装置B中加入的试剂______,作用是______.
②装置D加入的试剂______,装置F加入的试剂______.
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是______.
④U型管G的作用为______.
-
校办厂漂白车间需22.4L(标准状况)SO2.化学小组同学依据化学方程式Zn+2H2SO4(浓)
 ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g/cm3)110mL充分反应,锌全部溶解后,即将收集所得气体如数送至车间,不料经质检科检验存在严重质量问题,气体随即被退回.
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g/cm3)110mL充分反应,锌全部溶解后,即将收集所得气体如数送至车间,不料经质检科检验存在严重质量问题,气体随即被退回.
(1)化学小组所制得的气体中混有的主要杂质气体可能是______(填分子式).产生这种结果的主要原因是______.
(2)为证实相关分析,化学小组的同学设计了如下实验,对退回气体(X)取样进行认真探究(遇有气体吸收过程,视为全吸收).
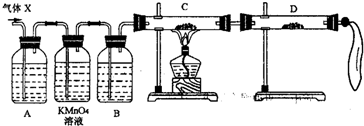
①组装好仪器后,盛放药品前,必要的一个操作是______.
②A中加入的试剂可能是:______,作用是:______.B中加入的试剂可能是:______,作用是:______.
③可证实气体X中混有较多量某杂质气体的实验现象是______.
(3)对上述装置略加改进,可粗略测定X气体中SO2的体积分数.改进时可选用的下列仪器为______(填代号).
A 导管 B 水槽 C 广口瓶 D 容量瓶 E 量筒 F 单孔塞 G 双孔塞.
-
Zn与浓硫酸反应的化学方程式:Zn+2H2SO4(浓)====ZnSO4+SO2↑+2H2O。向100 mL 18 mol·L-1H2SO4溶液中加入足量的锌粒充分反应后,被还原的H2SO4的物质的量 ( )
A.等于1.8 mol B.小于0.9 mol
C.等于0.9 mol D.在0.9 mol和1.8 mol之间
-
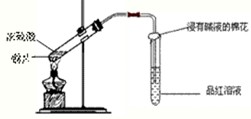
研究性学习小组为探究Cu与浓H2SO4反应及其产物SO2的性质,设计如下实验装置:
(1)写出铜与浓硫酸反应的化学方程式:______ CuSO4+SO2+2H2O
-
某化学小组为了证明SO2和Cl2的漂白性,设计了如下图所示的实验装置:
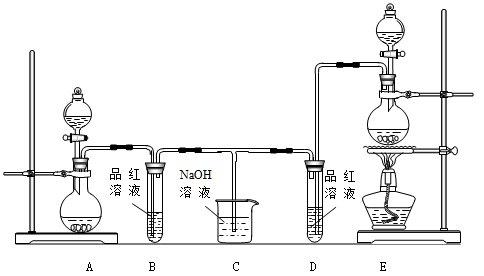
(1)他们制备Cl2依据的原理是:MnO2 + 4HCl(浓) MnCl2 + 2H2O + Cl2↑,应选用上图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 。
MnCl2 + 2H2O + Cl2↑,应选用上图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是 。
(3)NaOH溶液分别与两种气体反应的离子方程式是 、 。
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 。
-
某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
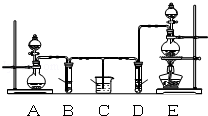
(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)△MnCl2+2H2O+Cl2↑,应选用图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 .
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是 .
(3)写出过量NaOH溶液与SO2气体反应的离子方程式是 .
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色.查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 .
-
(12分)某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
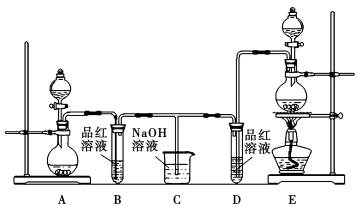
(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。
MnCl2+2H2O+Cl2↑,应选用上图A、E装置中的______________(填序号)制Cl2,反应中浓盐酸所表现出的性质是__________________。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是________________________________。
(3)NaOH溶液分别与两种气体反应的离子方程式是
______________________________________________________
________________________________________________。
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是____________________________。
-
为了探究Cl2、SO2同时通入H2O中发生的反应,某化学兴趣小组同学设计了图1所示的实验装置。
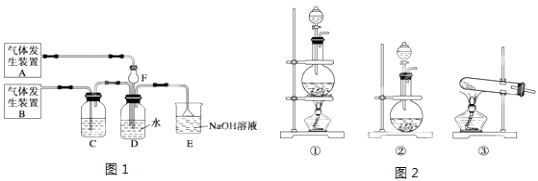
(1)该化学兴趣小组同学为制取Cl2和SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol/L)为原料制取Cl2。请写出制取Cl2的离子方程式: 。
(2)在此实验中,F仪器的作用是:______________;发生装置B应选择图2三种装置中的___________(填序号)。
(3)D装置中主要反应的离子方程式为 。
(4)为验证通入D装置中过量的气体是Cl2还是SO2气体,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰酸钾溶液 ④品红溶液 ⑤溴水 ⑥稀硝酸
A.若Cl2过量:取适量D中溶液滴加至盛有试剂的试管内,发生的现象是: ;(试剂可以多选,请填试剂的序号,下同)。
B.若SO2过量:取适量D中溶液滴加至盛有试剂的试管内,发生的现象是: 。
-
(11分)为了探究Cl2、SO2同时通入H2O发生的反应,某校化学兴趣小组同学设计了如下图所示的实验装置。
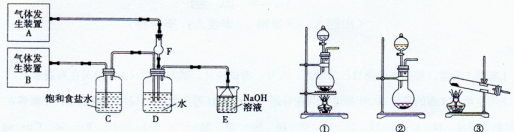
试填空:
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的浓硫酸为原料制取SO2,采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是________;气体发生装置B应选择①、②、③三种装置中的________(选填序号)。
(2)D装置中主要反应的离子方程式为:________。
(3)为验证通入D装置中气体是Cl2过量还是SO2过量,兴趣小组的同!学准备了以下试剂:氯化铁溶液;氯化亚铁溶液;硫氰化钾溶液;苯酚溶液;品红溶液;酸性高锰酸钾溶液。
若Cl2量:取适量D中溶液滴加至盛有________(试剂名称,下同)的试管中,再加入产生的现象是,说明Cl2过量;
若SO2过量:取适量D中溶液滴加至盛有________的试管内,产生的现象是________。
ZnSO4+SO2↑+2H2O计算后,取65g锌粒与质量分数为98%的浓硫酸(密度
)110mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。








