-
下列解释事实的方程式不正确的是
A.84 消毒液(有效成分为NaClO)中加入少量白醋可增强消毒效果:ClO− + CH3COOH = HClO + CH3COO−
B.用 Na2CO3 将水垢中的 CaSO4 转化为易于除去的CaCO3:CaSO4 + CO = CaCO3 + SO
= CaCO3 + SO
C.稀硫酸酸化的淀粉−KI 溶液在空气中放置一段时间后变蓝:2I− + SO + 4H+ = I2 + SO2 + 2H2O
+ 4H+ = I2 + SO2 + 2H2O
D.用 Na2S2O3 做碘量法实验时,溶液 pH 不可太低:S2O + 2H+ = SO2 + S↓ + H2O
+ 2H+ = SO2 + S↓ + H2O
-
下列解释事实的离子方程式中,不正确的是
A.铝片放入NaOH 溶液中有气体产生:
B.泡沫灭火器灭火的原理:
C.氨水吸收少量 防止污染空气:
防止污染空气:
D.“84”消毒液中滴少量白醋可增强漂白性:
-
下列解释事实的方程式中,不正确的是
A. 铜和浓HNO3反应可用于制NO2气体:Cu + 4HNO3((浓) = Cu(NO3)2 + 2NO2↑+ 2H2O
B. “84”消毒液中滴少量白醋可增强漂白性:ClO- + H+ = HClO
C. 氨水吸收少量SO2防止污染空气:2NH3·H2O + SO2 = 2NH4+ + SO32-+ H2O
D. Na2O2在潜艇中可用于吸收二氧化碳并供氧:2Na2O2 +2CO2= 2Na2CO3 + O2
-
下列解释实验过程或事实的反应方程式不正确的是( )
A. 在海带灰的浸出液(含有I-)中滴加H2O2得到I2: 2I-+H2O2+2H+=I2+2H2O
B. “84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+Cl-+2H+=Cl2↑+H2O
C. Fe(NO3)2溶液中滴加 NaHSO3溶液:3SO32-+2NO3-+2H+=3SO42-+2NO↑+H2O
D. Ca(HCO3)2溶液中滴加少量的氨水:Ca2++ HCO3+NH3·H2O=CaCO3↓+H2O+NH4+
-
下列解释事实的方程式不正确的是
A.用食醋清洗水垢:CO32- + 2CH3COOH = 2CH3COO- + H2O + CO2↑
B.84 消毒液与洁厕灵混用产生有毒气体:ClO- + Cl- + 2H+ = Cl2↑ + H2O
C.用氢氧化铝治疗胃酸过多:Al(OH)3 + 3H+ =Al3+ + 3H2O
D.用硫化钠除去废水中的汞离子:Hg2+ + S2- = HgS↓
-
氯气是一种非常重要的化工原料,含氯消毒剂在生产生活中有着广泛的用途。
(1)用氯气可制取“84消毒液”(有效成分为NaClO)。
①该制备反应的离子方程式为 。
②下列措施能增强“84消毒液”杀菌能力的是 。
A.加入适量醋酸
B.加入适量亚硫酸
C.加入少量NaOH粉末
③“84消毒液”不能对钢铁(含Fe、C)制品进行消毒,原因是 。
(2)二氧化氯(ClO2)是一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前,工业上开发出用电解法制取ClO2的新工艺,生产原理如图所示。
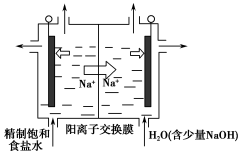
上述示意图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式: 。
-
下列离子方程式表达正确的是 ( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
B.“84消毒液”(有效成分NaClO溶液)和“沽厕灵”(浓HCl)混合放出氯气:
ClO-+Cl-+H+=Cl2↑+OH-
C.硫酸亚铁溶液被空气中氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH-
D.含Fe(SCN)3的溶液中滴加浓氢氧化钠溶液:Fe(SCN)3+3OH-=Fe(OH)3↓+3SCN-
-
“84”消毒液(有效成分为NaClO)可用于消毒和漂白,下列实验现象的分析,不正确的是 ( )
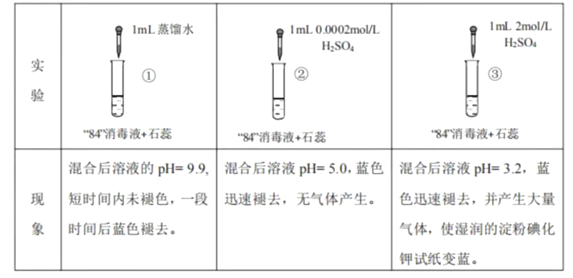
A. 对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO−+H+ ===HClO
B. 实验③中产生的气体是Cl2,由HClO分解得到:2HClO===Cl2↑+H2O
C. 对比实验②和③,溶液的pH可能会影响ClO− 的氧化性或Cl− 的还原性
D. 加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用
-
下列解释事实的离子方程式不正确的是
A.84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+=Cl2↑+H2O
B.向水玻璃中加入盐酸有白色沉淀生成:2H++SiO32-=H2SiO3↓
C.SO2使紫色石蕊溶液变红色:SO2+H2O  2H++SO32-
2H++SO32-
D.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HClO
-
(7 分)某消毒液的主要成分为 NaClO(混有少量NaCl),请用相应的化学用语来解释下列事实。
(1)该消毒液可用NaOH 溶液吸收Cl2 制备,化学方程式为 。
(2)该消毒液的pH 约为12,离子方程式为 。
(3)向FeSO4 溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为 。
(4)该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。每产生1 mol Cl2(标准状况下),转移电子个数约为 。
= CaCO3 + SO
+ 4H+ = I2 + SO2 + 2H2O
+ 2H+ = SO2 + S↓ + H2O

