-
已知:298K时,N2(g)+3H2(g) 2NH3(g) △H=-92.2kJ·mol-1。
2NH3(g) △H=-92.2kJ·mol-1。
(1)若N≡N的键能为941.3kJ·mol-1,H—H的键能为436.4kJ·mol-1,则N—H的键能为___。
(2)实验室将1.1molN2、3molH2充入2L容器,一定条件下反应。保持温度和容器体积不变,
①若2min末测得H2的物质的量为1.8mol,则该时间段内氨气的平均反应速率为___。
②保持温度和容器体积不变,下列措施可加快该反应速率的是___。
A.充入He气
B.使用恰当的催化剂
C.升高反应体系的温度
D.再充入N2
③当下列物理量保持不变时,表明该反应一定处于化学平衡状态的是___。
A.容器内N2与H2的含量
B.容器内气体密度
C.恒温下容器的压强
D.H2的物质的量
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示:
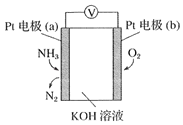
①外电路电流的运动方向:___。(填“a极到b极”或“b极到a极”)。
②b极电极反应式为___。
-
273K时,反应N2(g)+3H2(g)  2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
2NH3(g) 生成2 molNH3(g)时放出92.2kJ的热量。在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2。则下列判断不正确的是:
A.同时进行时,用N2表示的反应速率:情况1>情况2
B.平衡时,情况1:Q1= 92.2kJ
C.达到平衡时,混合气体的密度:情况1>情况2
D.平衡时,情况2:Q2<46.1kJ
-
273K时,反应N2(g)+3H2(g)═2NH3(g) 生成2molNH3(g)时放出92.2kJ的热量.在该温度下,向一固定容积的密闭容器内通入1mol N2和3mol H2,达到平衡时,放出热量为Q1;向另一容积相同的密闭容器中通入0.5mol N2和1.5mol H2,达到平衡时放出热量为Q2.则下列判断不正确的是( )
A.同时进行时,用N2表示的反应速率:情况1>情况2
B.平衡时,情况1:Q1=92.2kJ
C.达到平衡时,混合气体的密度:情况1>情况2
D.平衡时,情况2:Q2<46.1kJ
-
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:
N2(g)+3H2(g) 2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
A.10到15秒内c(NH3) 增加量等于0.25mol •L—1
B.10秒内氨气的平均反应速率为0.025mol•L—1·s—1
C.达平衡后,分离出少量NH3,v正 增大
D.该反应的逆反应的活化能不小于92.2kJ•mol—1
-
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是( )
A.10到15秒内c(NH3) 增加量等于0.25mol •L—1
B.10秒内氨气的平均反应速率为0.025mol•L—1·s—1
C.达平衡后,分离出少量NH3,v正 增大
D.该反应的逆反应的活化能不小于92.2kJ•mol—1
-
298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol,在该温度下,取1 mol N2和3 mol H2放在密闭容器内反应。下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ/mol,在该温度下,取1 mol N2和3 mol H2放在密闭容器内反应。下列说法正确的是( )
A. 在有催化剂存在的条件下,反应放出的热量为92.4 kJ
B. 有无催化剂该反应放出的热量都为92.4 kJ
C. 反应放出的热量始终小于92.4 kJ
D. 若再充入1 mol H2,到达平衡时放出的热量应为92.4 kJ
-
(1)已知3N2H4(l) 4NH3(g)+N2(g) △H = —336.6kJ/mol,
4NH3(g)+N2(g) △H = —336.6kJ/mol,
N2(g)+3H2(g) 2NH3(g) △H = —92.4kJ/mol,
2NH3(g) △H = —92.4kJ/mol,
则N2H4(g) N2(g)+2H2(g) △H = ________________。
N2(g)+2H2(g) △H = ________________。
(2)写出下列物质的电离方程式:
①NaHSO4___________________________________,
②K2SO4_____________,
③NH4NO3___________________________。
(3)写出下列物质的电子式:
Na2S:_________; CO2:_________。
-
已知N2(g)+3H2(g)==2NH3(g) △H=-92 kJ·mol-1 。且1 mol N≡N键完全断裂时吸收热量946 kJ, 1 mol H-N键形成时放出热量391 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
-
已知:①N2(g)+O2(g)===2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)  2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是 ( )
A. 反应②中的能量变化如图所示:
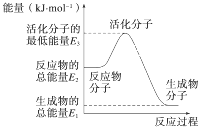
则ΔH2=E1-E3
B. H2的燃烧热为241.8 kJ·mol-1
C. 氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+ 6H2O(g) ΔH=+906 kJ·mol-1
D. 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,最终反应放出的热量小于92.4 kJ,
-
已知N≡N键能为946 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2  2NH3 ΔH=-92 KJ/mol,则H—H键的键能是
2NH3 ΔH=-92 KJ/mol,则H—H键的键能是
A. < 436 KJ/mol B. 436 KJ/mol C. 497 KJ/mol D. 467 KJ/mol
2NH3(g) △H=-92.2kJ·mol-1。

