-
在25°C时,向a mL 0.10mol·L-1的HNO2溶液中逐滴加入0.10mol·L-1的NaOH溶液,滴定过程中,混合溶液的pOH[pOH= -lgc(OH-)]与NaOH溶液的体积V的关系如图所示。已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),下列说法不正确的是( )
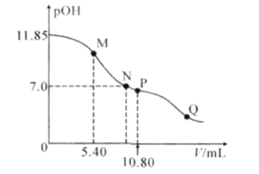
A.25°C时,HNO2电离常数的数量级是10-4
B.M点溶液中存在:3c(H+)+ c(HNO2)=3c(OH-)+ c(NO2-)
C.图上M、N、P、Q四点溶液中所含离子的种类相同
D.a=10.80
-
在25°C时,向amL0.10mol·L-1的HNO2溶液中逐滴加入0.10mol·L-1的NaOH溶液。滴定过程中混合溶液的pOH[pOH=-lgc(OH-)]与NaOH溶液的体积V的关系如图所示。已知P点溶液中存在c(OH-)=c(H+)+c(HNO2),下列说法不正确的是( )
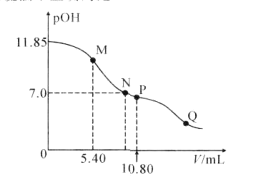
A.25°C时,HNO2电离常数的数量级是10-4
B.M点溶液中存在:2c(H+)+c(HNO2)=c(OH-)+c(NO2-)
C.图上M、N、P、Q四点溶液中所含离子的种类相同
D.a=10.80
-
常温下,向20mL0.10mol·L-1HClO溶液中逐滴加入0.10mol·L-1NaOH溶液,滴定过程中溶液中水电离出的c(H+)变化曲线如图所示。下列说法正确的是
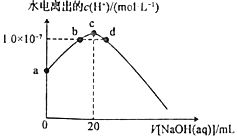
A.可用pH试纸测定a点溶液的pH
B.b、c、d三点溶液中离子、分子种类不同
C.a、b、c、d四点溶液中水的电离程度:c>b=d>a
D.d点溶液中c(Na+)=c(ClO-)
-
室温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1的CH3COOH 溶液和HCN溶液所得滴定曲线如图所示。下列说法正确的是
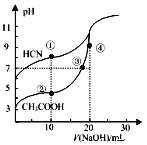
A. 当加入10mLNaOH时:c(CH3COOH)>c(HCN)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 已知室温下某碱AOH的Kb=1×10-9,则ACN的水溶液呈碱性
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
-
下列关于各图象的解释或得出的结论正确的是
A.图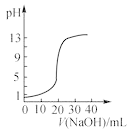 表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图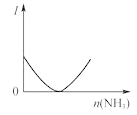 表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图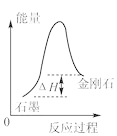 所示可知:石墨比金刚石稳定
所示可知:石墨比金刚石稳定
D.图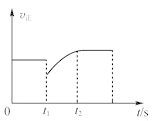 表示反应2SO2+O2
表示反应2SO2+O2 2SO3,t1时刻只减小了的SO3的浓度
2SO3,t1时刻只减小了的SO3的浓度
-
下列关于各图象的解释或得出的结论正确的是
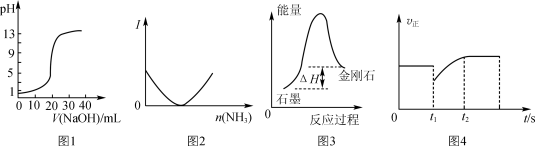
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O2 2SO3,t1时刻只减小了的SO3的浓度
2SO3,t1时刻只减小了的SO3的浓度
-
下列关于各图象的解释或得出的结论正确的是
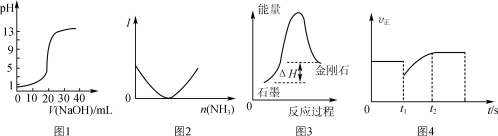
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O2 2SO3,t1时刻只减小了SO3的浓度
2SO3,t1时刻只减小了SO3的浓度
-
下列关于各图象的解释或得出的结论正确的是
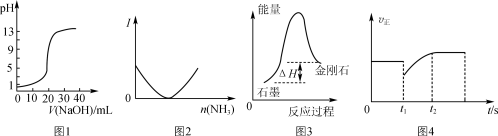
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O2 2SO3,t1时刻只减小了SO3的浓度
2SO3,t1时刻只减小了SO3的浓度
-
已知电导率越大导电能力越强。常温下用0.10 mol·L-1NaOH溶液分别滴定10mL浓度均为0.10 mol·L-1的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示。下列说法正确的是
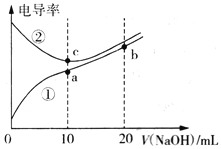
A.曲线①代表滴定盐酸的曲线
B.滴定醋酸的过程应该选择甲基橙作为指示剂
C.a、b、c三点溶液中水的电离程度:c>a>b
D.b点溶液中:c(OH-)>c(H+)+c(CH3COO-)+c(CH3COOH)
-
室温下,用0.10 mol·L-1盐酸分别滴定20.00 mL 0.10 mol·L-1氢氧化钾溶液和氨水,滴定过程中溶液pH随加入盐酸体积[V(HCl)]的变化关系如图所示。下列说法正确的是( )
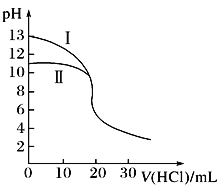
A. Ⅰ表示的是滴定氨水的曲线
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且此时溶液中c(NH4+)=c(Cl-)
C. 滴定氢氧化钾溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(H+)>c(K+)>c(OH-)
D. 当滴定氨水消耗V(HCl)=10 mL时,c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)>c(H+)




 表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线 表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化 所示可知:石墨比金刚石稳定
所示可知:石墨比金刚石稳定 表示反应2SO2+O2
表示反应2SO2+O2



