下列关于各图象的解释或得出的结论正确的是
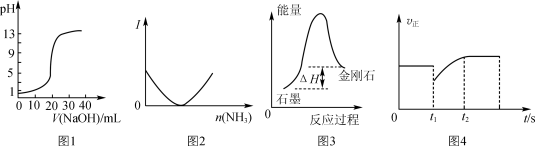
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O22SO3,t1时刻只减小了的SO3的浓度
高三化学选择题困难题
下列关于各图象的解释或得出的结论正确的是

A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O22SO3,t1时刻只减小了的SO3的浓度
高三化学选择题困难题
下列关于各图象的解释或得出的结论正确的是
A.图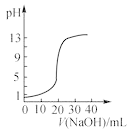 表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
表示用0.10 mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图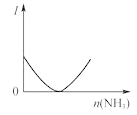 表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图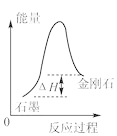 所示可知:石墨比金刚石稳定
所示可知:石墨比金刚石稳定
D.图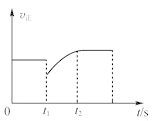 表示反应2SO2+O2
表示反应2SO2+O22SO3,t1时刻只减小了的SO3的浓度
高三化学单选题中等难度题查看答案及解析
下列关于各图象的解释或得出的结论正确的是

A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O22SO3,t1时刻只减小了的SO3的浓度
高三化学选择题困难题查看答案及解析
下列关于各图象的解释或得出的结论正确的是
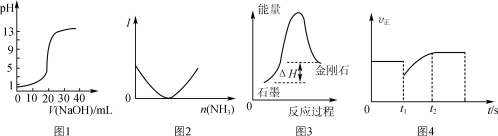
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O22SO3,t1时刻只减小了SO3的浓度
高三化学选择题中等难度题查看答案及解析
下列关于各图象的解释或得出的结论正确的是
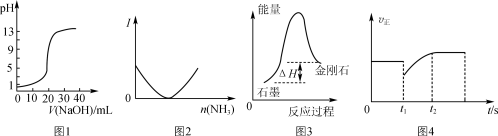
A.图1表示用0.10 mol·L-1 NaOH溶液滴定20.00 mL 0.10 mol·L-1醋酸溶液的滴定曲线
B.图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图3所示可知:石墨比金刚石稳定
D.图4表示反应2SO2+O22SO3,t1时刻只减小了SO3的浓度
高三化学选择题中等难度题查看答案及解析
25℃时,用0.1 mol•L-1的NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法正确的是

A.③为滴定终点,可用甲基橙作指示剂
B.点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C.点①和点②所示溶液中:c(CH3COO-)<c(CN-)
D.点②和点④所示溶液中:c(CH3COO-)+ c(CH3COOH)的值相等
高三化学选择题极难题查看答案及解析
下图为常温下用0.10mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1盐酸和20.00 mL 0.10 mol·L-1醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
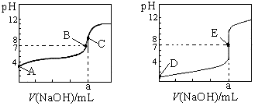
A.左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c(Na+)= c(A—)
C.B点时,反应消耗溶液体积:V(NaOH)>V(HA)
D.当0mL<V(NaOH)<20. 00mL时,溶液中一定是c(A-)>c(Na+)>c(H+) >c(OH-)
高三化学选择题困难题查看答案及解析
常温下,用0.10mol/LNaOH溶液滴定20.00mL 0.10mol/LHA溶液(滴定曲线见图)。下列说法正确的是( )
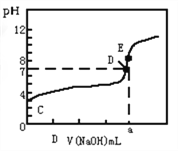
A. 此图可以表示从NaOH滴定盐酸的曲线
B. 图中D点状态时溶液中有:c(Na+)<c(A-)
C. 达到D、E状态时,均有:c(Na+)+c(H+)=c(A-)+c(OH-)
D. 当O<V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)> c(Na+)> c(H+)>c(OH-)
高三化学选择题困难题查看答案及解析
常温下,用0.10mol/LNaOH溶液滴定20.00mL 0.10mol/LHA溶液(滴定曲线见图)。下列说法正确的是( )

A. 此图可以表示从NaOH滴定盐酸的曲线
B. 图中D点状态时溶液中有:c(Na+)<c(A-)
C. 达到D、E状态时,均有:c(Na+)+c(H+)=c(A-)+c(OH-)
D. 当O<V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)> c(Na+)> c(H+)>c(OH-)
高三化学选择题困难题查看答案及解析
常温下,用0.10mol/LNaOH溶液滴定20.00mL 0.10mol/LHA溶液(滴定曲线见图)。下列说法正确的是

A. 此图可以表示从NaOH滴定盐酸的曲线
B. 图中D点状态时溶液中有:c(Na+)<c(A-)
C. 达到D、E状态时,均有:c(Na+)+c(H+)=c(A-)+c(OH-)
D. 当O<V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)> c(Na+)> c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
常温下,用0.1mol/L NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1mol/L的HX、HY溶液,pH随NaOH溶液体积变化如图。下列结论正确的是
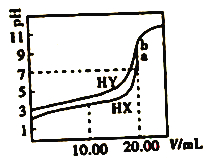
A. 水解常数:X->Y-
B. a、b两点溶液混合后:c(HX) +c(HY) +c(H+)=c(OH-)
C. pH=7时,c(Y-)>c(X-)
D. 10.00mlL时,有c(Na+)>c(HX)>c(X-)>c(H+)
高三化学单选题困难题查看答案及解析