25℃时,向1L0.01 mol•L-1H2B溶液中滴加盐酸或NaOH溶液,溶液中 c(H2B)、c(HB-)、c(B2-)、c(OH-)、c(H+) 的对数值(lgc)与pH的关系如图所示(温度保持不变),下列说法错误的是
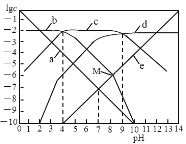
A.曲线c表示lgc(HB-)与pH的关系
B.随pH增加,c(H2B)•c(OH-)增大
C.0.01 mol•L-1Na2B溶液,Kh1(B2-)的数量级为10-9
D.M点溶液中n(Na+)+n(H+)―n(B2-)=0.01mol
高三化学多选题困难题
25℃时,向1L0.01 mol•L-1H2B溶液中滴加盐酸或NaOH溶液,溶液中 c(H2B)、c(HB-)、c(B2-)、c(OH-)、c(H+) 的对数值(lgc)与pH的关系如图所示(温度保持不变),下列说法错误的是

A.曲线c表示lgc(HB-)与pH的关系
B.随pH增加,c(H2B)•c(OH-)增大
C.0.01 mol•L-1Na2B溶液,Kh1(B2-)的数量级为10-9
D.M点溶液中n(Na+)+n(H+)―n(B2-)=0.01mol
高三化学多选题困难题
25℃时,向1L0.01 mol•L-1H2B溶液中滴加盐酸或NaOH溶液,溶液中 c(H2B)、c(HB-)、c(B2-)、c(OH-)、c(H+) 的对数值(lgc)与pH的关系如图所示(温度保持不变),下列说法错误的是

A.曲线c表示lgc(HB-)与pH的关系
B.随pH增加,c(H2B)•c(OH-)增大
C.0.01 mol•L-1Na2B溶液,Kh1(B2-)的数量级为10-9
D.M点溶液中n(Na+)+n(H+)―n(B2-)=0.01mol
高三化学多选题困难题查看答案及解析
下列说法正确的是
A. 0.1mol/LpH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
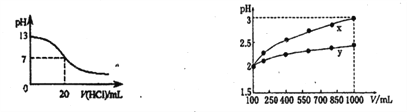
B. 左图表示25℃时,用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
C. 在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-)
D. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy
高三化学选择题困难题查看答案及解析
某二元弱酸(简写为H2B)溶液,按下式发生一级和二级电离:
H2BH++HB-
HB-H++B2-
已知相同浓度时的电离度a(H2B)>>a(HB-),现有下列四种溶液:
①0.01mol•L-1的H2B溶液
②0.01mol•L-1的NaHB溶液
③0.02mol•L-1的HCl溶液与0.04mol•L-1的NaHB溶液等体积混合后的溶液
④0.02mol•LL-1的NaOH溶液与0.02mol•L-1的NaHB溶液等体积混合后的溶液
下列说法错误的是( )
A.溶液④一定显碱性 B.c(H2B)最大的是③
C.c(B2-)最小的是① D.c(H+)最大的是③
高三化学单选题中等难度题查看答案及解析
常温下,电解质溶液中的下列关系式不正确的是
A. 已知A-+H2B(过量)==HA+HB-,则结合H+的能力:HB-<A-<B2-
B. 在0.1mol·L-1的氨水中滴加0.1 mol·L-1盐酸,恰好完全中和时, c(NH4+)+c(NH3 •H2O)=0.05 mol·L-1
C. 将c mol·L-1的醋酸溶液与0.02 mol·L-1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数ka=
D. 将0.2 mol·L-1盐酸与0.1 mol·L-1的KAlO2溶液等体积混合,溶液中离子浓度由大到小的顺序:c(Cl-)> c(K+)> c(Al3+)> c(H+)> c(OH-)
高三化学选择题中等难度题查看答案及解析
下列说法正确的是
A. 0.1 mol·L-1pH为4的NaHB溶液中:c (HB-)>c(H2B)>c(B2-)
B. 如下图表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1 NaOH溶液时,溶液的pH随加入酸体积的变化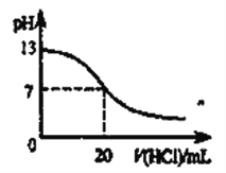
C. 在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-)
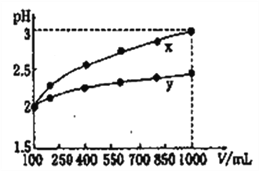
D. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy
高三化学单选题困难题查看答案及解析
下列说法正确的是
A. 0.1 mol·L-1pH为4的NaHB溶液中:c (HB-)>c(H2B)>c(B2-)
B. 如下图表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1 NaOH溶液时,溶液的pH随加入酸体积的变化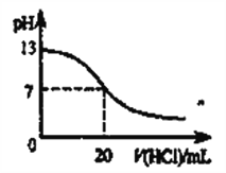
C. 在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-)
D. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy
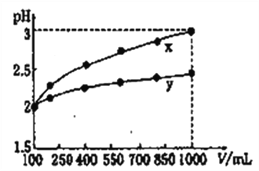
高三化学单选题困难题查看答案及解析
下列说法正确的是
A. 0.1 mol·L-1pH为4的NaHB溶液中:c (HB-)>c(H2B)>c(B2-)
B. 如下图表示25℃时,用0.1mol·L-1盐酸滴定20mL 0.1mol·L-1 NaOH溶液时,溶液的pH随加入酸体积的变化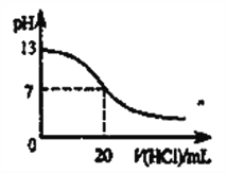
C. 在pH=2的NaHSO4溶液中c(H+)=c(OH-)+ c(SO42-)
D. pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如下图所示,分别滴加NaOH溶液(c=0.1mol·L-1)至pH=3,消耗NaOH溶液的体积为Vx、Vy,则x为强酸,y为弱酸且Vx>Vy
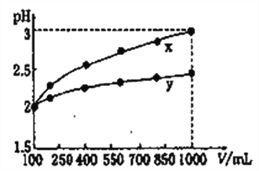
高三化学单选题困难题查看答案及解析
下列叙述正确的是( )
A.0.1mol/LpH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
B.常温下,pH=2的CH3COOH溶液和H2SO4溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离出的c(H+)不相等
C.常温下将浓度为0.1mol/L的HF溶液加水不断稀释,溶液中的值始终保持增大
D.常温下0.1mol/L的下列溶液①NH4Fe(SO4)2;②NH4Cl;③NH3·H2O;④CH3COONH4中c(NH4+)由大到小的顺序是:②>①>④>③
高三化学单选题中等难度题查看答案及解析
下列叙述正确的是
A. 0.1 mol • L-1pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
B. 常温下,PH=2的CH3COOH溶液和H2SO4溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离出的c(H+)不相等
C. 常温下将浓度为0.1 mol·L-1的HF溶液加水不断稀释,溶液中c(H+)/c(HF)的值始终保持增大
D. 常温下0.1 mol·L-1的下列溶液①NH4Fe(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中:c(NH4+)由大到小的顺序是:②>①>④>③
高三化学选择题困难题查看答案及解析
回答下列问题:
(1)某二元酸(分子式用H2B表示)在水中的电离方程式是:H2B===H++HB-;HB-H++B2-。在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol/L
B.c(B2-)+c(HB-)+c(H2B)=c(Na+)
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(OH-)=c(H+)+c(HB-)
(2)下表为几种酸的电离平衡常数
| CH3COOH | H2CO3 | H2S |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 |
则pH相同的CH3COONa、Na2CO3、NaHS溶液物质的量浓度由大到小的顺序为________________,少量CO2与NaHS反应的离子方程式为______________。
高三化学简答题中等难度题查看答案及解析