-
在下列物质中:
①H2O②NH3③NH3•H2O④乙醇⑤乙烯⑥CO2⑦CuSO4•5H2O⑧甲烷⑨H2O2
含非极性键的极性分子有( )
A.①②⑥ B.③④⑦ C.④⑨ D.③④⑧⑨
高三化学单选题简单题查看答案及解析
-
下列物质中,含极性键和非极性键且分子有极性的是( )
A.乙烯 B.H2O2 C.甲烷 D.三氯甲烷
高三化学单选题简单题查看答案及解析
-
下表各组物质分类不正确的是( )
选项
A
B
C
D
物质
液氧、空气、Cl2、铜丝
HCl、H2SO4、H2O、HNO3
NaCl溶液、盐酸、CuSO4·5H2O
NH3、NaOH、BaSO4固体
分类标准
单质
酸
混合物
电解质
不属于该
类的物质
空气
H2O
盐酸
NH3
A. A B. B C. C D. D
高三化学选择题中等难度题查看答案及解析
-
下列物质中,含有非极性共价键的离子化合物是 ( )
A.Na2O2 B.NaOH C.H2O2 D.NH3·H2O
高三化学选择题简单题查看答案及解析
-
以冶铜工厂预处理过的污泥渣(主要成分为 CuO 和 Cu)为原料制备 CuSO4•5H2O 晶体的流程如下 :
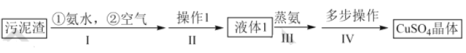
已知:①CuO在氨水作用下可以生成 Cu(NH3)4(OH)2
②CuSO4•5 H2O 加热到 4 5℃时开始失水。
请回答:
(1)步骤 l 中,空气的主要作用是____。
(2)下列关于步骤II说法不正确的是____。
A.操作 1 可选择倾析法过滤, 玻璃棒的作用是: 先搅拌, 再引流
B.操作 1 应趁热过滤, 要防止液体 1 中的溶质因冷却而析出
C.操作 1 为抽滤,在加入需抽滤的物质时,用玻璃棒引流液体, 玻璃棒底端需紧贴在滤纸上
D.抽滤时,布氏漏斗的底部斜口面需正对抽滤瓶的抽气口处, 是为了提高抽滤的速率
(3)液体 1 通过步骤 III 与步骤IV可得到CuSO4•5 H2O 晶体 。
①蒸氨过程的生成物均是由两种元素组成的化合物, 则除氨外其余产物的化学式为_____。
②步骤IV中包含多步操作, 将下列步骤按正确的步骤排序(必要时步骤可重复选)。_____→得到固体物质→ ____ →将液体放于蒸发皿中加热→ ____→_____→_____→_____ →得到晶体
a.过滤 b.用玻璃棒不断搅拌溶液 c.用足量稀硫酸溶解固体 d.停止加热 e.至溶液表面析出晶膜
(4)步骤1中分别选用氨水、氨水-碳酸铵混合溶液氨浸时, 铜元素回收率随温度变化如图所示。
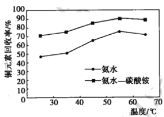
①浸取液为氨水时,反应温度控制为 55℃,温度过高铜元素回收率降低的原因是_______。
②浸取液为氨水一碳酸铵混合溶液时,铜元素回收率受温度影响较小的原因可能是______。
(5)为了提高 CuSO4晶体的产率, 实验室还采用以下方法: 将CuSO4 溶液转移至蒸馏烧瓶中, 加入适量冰醋酸, 通过下图所示的装置获取晶体。
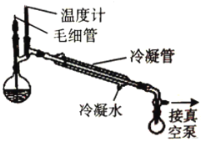
①加入适量乙酸的目的是:_____。
②图中接真空泵的作用是:______。
高三化学工业流程中等难度题查看答案及解析
-
当下列各组物质的总物质的量不变时,使各组分以任意比混合后充分燃烧,消耗氧气的量和生成CO2的物质的量不变的是( )
A.乙烯、乙醇、乙醛
B.乙炔、乙醛、乙二醇
C.甲烷、甲醇、乙酸
D.甲烷、甲酸甲酯、丙二酸
高三化学选择题中等难度题查看答案及解析
-
下列各组物质中,都是由极性键构成的极性分子的一组是( )。
A.CH4 Br2 B.H2O NH3
C.CCl4 H2S D.CO2 HCl
高三化学选择题中等难度题查看答案及解析
-
下列各组物质中,都是由极性键构成的极性分子的一组是
A.NH3和H2O B.CH4和Br2
C.H2S和CCl4 D.CO2和HCl
高三化学选择题中等难度题查看答案及解析
-
天然气( 主要成分为甲烷)是一种高效的清洁能源,也是一种重要的化工原料,利用天然气制备甲醇、乙醇、二甲醚(CH3OCH3)、乙烯(C2H4)等物质的主要反应有:
①CH4(g)+H2O(g)=CO(g)+ 3H2(g) △H1= + 206.2 kJ/ mol
②CO(g)+2H2(g)=CH3OH(g) △H2=- 90.1kJ/ mol
③2CH3OH(g) = CH3OCH3(g) + H2O(g) △H3=- 24.5kJ/ mol
④2CH3OH(g)
C2H4(g) + 2H2O(g) △H4=- 29.1kJ/ mol
⑤CH3OCH3(g)== C2H5OH(g) △H5=- 50.7 kJ /mol
请回答下列问题:
(1)反应2CH4(g)+H2O(g)= C2H5OH(g)+2H2(g)的△H =______kJ/mol;根据化学原理,可 以同时加快该反应的速率和提高甲烷转化率的措施有_______________________。
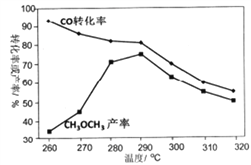
(2)CO与H2在一定条件下,同时发生②和③的反应,产生二甲醚的结果如上图所示。260℃时,CO转化率虽然很高,而二甲醚的产率却很低,可能的原因是 ( 答出一条即可) _______;CO 与H2 合成二甲醚的最佳的温度是_____________。
(3) 对于气体参与的反应如反应④[2CH3OH(g)
C2H4(g) + 2H2O(g)],可以用某组分B的平衡压强(PB)代替物质的量浓度(c)表示平衡常数(Kp),则反应④的平衡常数表达式Kp=____;也可以用压强(PB)变化表示化学反应速率,体积不变的密闭容器中充入一定量的CH3OH气体发生反应④,在10分钟内,容器的压强由xkPa 升高到ykPa,则这段时间该反应的化学反应速率v(CH4)=_____________。
(4) 反应①~⑤中有多种物质可以做燃料电池的燃料,其中H2是单位质量燃料释放电能最多的物质,若与下列物质构成电池,H2 与_______构成的电池比能量最大。
a.H2O2 b.Cl2 C.O2 d.NiOOH
高三化学综合题中等难度题查看答案及解析
-
下列含有非极性键的非极性分子是( )
A.H2 B.H2O C.H2O2 D.CO2
高三化学选择题简单题查看答案及解析