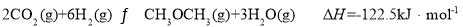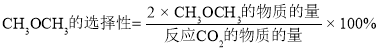-
 资源化利用的方法之一是合成二甲醚(
资源化利用的方法之一是合成二甲醚( 简写做
简写做 )。
)。 催化加氢法合成
催化加氢法合成 ,其过程中主要发生下列反应:
,其过程中主要发生下列反应:
反应Ⅰ:

反应Ⅱ:

其中,反应Ⅱ分以下两步完成,请写出反应Ⅳ的热化学方程式。
反应Ⅲ:

反应Ⅳ:___________。
⑴反应Ⅳ的热化学方程式为________。
⑵在 和
和 的起始量一定的条件下,
的起始量一定的条件下, 的平衡转化率和平衡时
的平衡转化率和平衡时 、
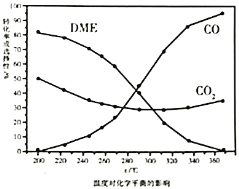
、 的选择性随压强或温度的变化见下图。已知:
的选择性随压强或温度的变化见下图。已知:
 的选择性
的选择性 ;
;
 的选择性
的选择性
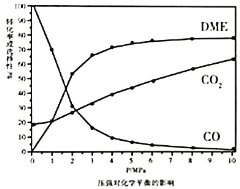
①依据图像中的数据分析,提高平衡时 的选择性应当选择的条件为________。
的选择性应当选择的条件为________。
A 高温高压 B 低温低压 C 高温低压 D 低温高压
按照温度对化学平衡的影响图像分析温度低于300℃, 平衡转化率随温度升高而降低的原因是_______。
平衡转化率随温度升高而降低的原因是_______。
②某温度和压强下,起始投入 与足量
与足量 发生反应,达到平衡时
发生反应,达到平衡时 的转化率为40%,部分物质的物质的量如下表:
的转化率为40%,部分物质的物质的量如下表:
计算平衡时 的选择性为________,反应Ⅳ的化学平衡常数为________。
的选择性为________,反应Ⅳ的化学平衡常数为________。
⑶经研究发现,在不同反应条件下反应相同时间(未平衡)测定发现,体系中 的浓度均很低,则可知活化能大小关系:反应Ⅲ________反应Ⅳ(填“大于”、“小于”或“等于”)。
的浓度均很低,则可知活化能大小关系:反应Ⅲ________反应Ⅳ(填“大于”、“小于”或“等于”)。
⑷ ,投料比为
,投料比为 时进行反应,
时进行反应, 的浓度随时间变化如下图所示,则下列说法正确的为________。
的浓度随时间变化如下图所示,则下列说法正确的为________。

A 在 范围内,反应Ⅰ的速率随温度升高而增大
范围内,反应Ⅰ的速率随温度升高而增大
B 200℃条件下,随反应时间的延长, 的浓度始终增大
的浓度始终增大
C 260℃条件下,随反应时间的延长, 的浓度先增大后减小最终不变
的浓度先增大后减小最终不变
D 260℃条件下, 后
后 的浓度减小是因为随时间推移反应Ⅱ的进行使体系中
的浓度减小是因为随时间推移反应Ⅱ的进行使体系中 浓度越来越高,反应Ⅰ的逆反应速率不断增大,从而使
浓度越来越高,反应Ⅰ的逆反应速率不断增大,从而使 浓度逐渐下降
浓度逐渐下降
-
CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(3)CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH =41.2 kJ·mol−1
CO(g)+H2O(g) ΔH =41.2 kJ·mol−1
反应Ⅱ:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ΔH =﹣122.5 kJ·mol−1
CH3OCH3(g)+3H2O(g) ΔH =﹣122.5 kJ·mol−1
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:CH3OCH3的选择性=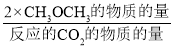 ×100%
×100%
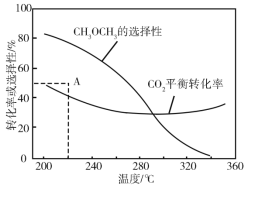
①温度高于300 ℃,CO2平衡转化率随温度升高而上升的原因是________。
②220 ℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有________。
-
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究新的热点。 完成下列问题:
(1)CO2催化加氢合成CH3OCH3是一种CO2转化方法,其过程中主要发生下列反应:
反应I:
反应Ⅱ: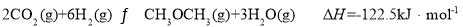
①写出CO和H2合成CH3OCH3的热化学方程式____。
②分别在2L恒温密闭容器甲(恒温恒容)、乙(恒温恒压)中,加入CO2和H2各1 mol的混合气体,假设只发生反应Ⅱ,则两容器中反应达平衡后放出或吸收的热量较多的是____(填“甲”或“乙”)。当反应5 min时,测得甲容器中压强变为原来的一半,则用CO2表示的反应的速率= ___。
③在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:
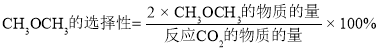
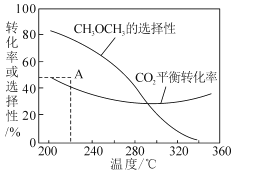
i)温度高于300℃,温度对CO2平衡转化率影响较大的是反应____(填“I”或“Ⅱ”)。
ii)220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施可以是____(任答一条)。
(2)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为____(写离子符号);若所得溶液c(HCO3-):c(CO32-)=1:5,溶液pH= ___。(室温下,H2CO3的 )
)
-
CO2的转化和重整受到越来越多的关注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)热化学转化法。
CO2催化加氢合成CH4,其过程中主要发生下列反应:
反应Ⅰ:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
反应Ⅱ:CO(g)+H2O (g)=CO2(g)+H2(g);ΔH=+2.8 kJ·mol-1
反应Ⅲ:2CO(g)+O2(g)=2CO2(g);ΔH=-566.0 kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g) 的ΔH=________kJ·mol-1。
(2)CO2催化还原法。
图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当有1 mol CO2反应时,直接传递的电子物质的量为________mol。
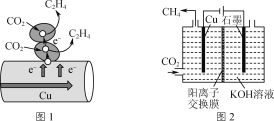
(3)CO2电化学催化重整法。
①图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为______________________,电解一段时间后,阳极区溶液pH减小,其原因是__________________。
②CO2与CH4在催化剂作用下合成乙酸,反应的化学方程式为________。
(4)CO2与丙烯通过金属杂多酸盐[CoxH(3-2x)PW12O40] 催化合成甲基丙烯酸。
①研究发现金属杂多酸盐中x对CO2转化率的影响如图3所示,由图3得出催化效果最好的金属杂多酸盐化学式是________。
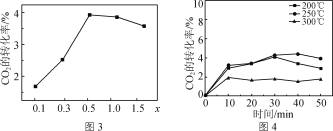
②催化剂在温度不同时对CO2转化率的影响如图4所示,300 ℃催化效果远不如200 ℃ 和250 ℃的原因为__________________________________。
-
CO2的转化和重整受到越来越多的关注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)热化学转化法。
CO2催化加氢合成CH4,其过程中主要发生下列反应:
反应Ⅰ:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1
反应Ⅱ:CO(g)+H2O (g)=CO2(g)+H2(g);ΔH=+2.8 kJ·mol-1
反应Ⅲ:2CO(g)+O2(g)=2CO2(g);ΔH=-566.0 kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g) 的ΔH=________kJ·mol-1。
(2)CO2催化还原法。
图1表示的是利用CO2的“直接电子传递机理”。在催化剂铜的表面进行转化。当有1 mol CO2反应时,直接传递的电子物质的量为________mol。
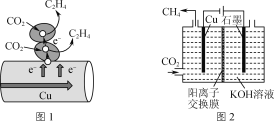
(3)CO2电化学催化重整法。
①图2表示以KOH溶液作电解质溶液进行电解的示意图,CO2在Cu电极上可以转化为CH4,该电极反应的方程式为______________________,电解一段时间后,阳极区溶液pH减小,其原因是__________________。
②CO2与CH4在催化剂作用下合成乙酸,反应的化学方程式为________。
(4)CO2与丙烯通过金属杂多酸盐[CoxH(3-2x)PW12O40] 催化合成甲基丙烯酸。
①研究发现金属杂多酸盐中x对CO2转化率的影响如图3所示,由图3得出催化效果最好的金属杂多酸盐化学式是________。
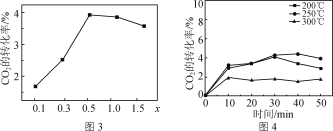
②催化剂在温度不同时对CO2转化率的影响如图4所示,300 ℃催化效果远不如200 ℃ 和250 ℃的原因为__________________________________。
-
研究CO2的综合利用对促进“低碳经济”的发展有重要意义。CO2与H2合成二甲醚(CH3OCH3)是一种CO2转化方法,其过程中主要发生下列反应:
反应I CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1= -49.0 kJ.mol-1
CH3OH(g)+H2O(g) △H1= -49.0 kJ.mol-1
反应II 2CH3OH(g) CH3OCH3(g)+H20(g) △H2=- 24.5 kJ.mol-1
CH3OCH3(g)+H20(g) △H2=- 24.5 kJ.mol-1
反应III CO2(g)+H2(g) CO(g)+H2O(g) △H3=41.2 kJ.mol-1
CO(g)+H2O(g) △H3=41.2 kJ.mol-1
(1)写出CO2与H2一步合成二甲醚(反应IV)的热化学反应方程式:_______________
(2)有利于提高反应IV平衡转化率的条件是_______。
A.高温高压 B.低温诋压 C.高温低压 D.低温高压
(3)在恒压、CO2和H2起始物质的量之比为1:3的条件下,CO2平衡转化率和平衡时二甲醚的选择性随温度的变化如图1。CH3OCH3的选择性=


①温度低于300℃,CO2平衡转化率随温度升高而下降的原因是_____________________
②关于合成二甲醚工艺的理解,下列说法正确的是_____________
A.反应IV在A点和B点时的化学平衡常数K(A)小于K(B)
B.当温度、压强一定时,在原料气(CO2和H2的比例不变)中添加少量惰性气体,有利于提高平衡转化率
C.其他条件不变,在恒容条件下的二甲醚平衡选择性比恒压条件下的平衡选择性低
D.提高催化剂的活性和选择性,减少CO等副产物是工艺的关键
③在某温度下,若加入CO2的物质的量为1mol,生成二甲醚的选择性为80%,现收集到0.2mol的二甲醚,则CO2转化率为__________________
④一定温度压强下,二甲醚的体积分数随时间变化如图2所示。在t1时刻,再加入物质的量之比为1:3的CO2和H2,t2时刻重新达到平衡。画出t1—t3时刻二甲醚体积分数的变化趋势。__________________
(4)光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成二甲醚的光能储存装置如图所示,则b极的电极反应式为____________________
-
“低碳循环”引起各国的高度重视,而如何降低大气中 的的含量及有效地开发利用
的的含量及有效地开发利用 ,也正成为科学家研究的主要课题。利用
,也正成为科学家研究的主要课题。利用 直接加氢合成二甲醚包括以下三个相互联系的反应。
直接加氢合成二甲醚包括以下三个相互联系的反应。
I甲醇的合成
II甲醇脱水
Ⅲ逆水汽变换
已知:相关物质变化的焓变示意图如下:
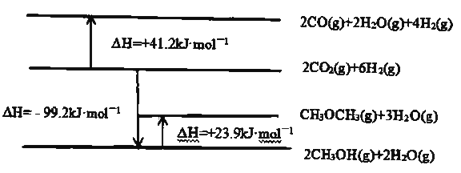
(1)请写出 直接加氢合成二甲醚的热化学方程式:________________。
直接加氢合成二甲醚的热化学方程式:________________。
(2)保持恒温恒容的条件,当a充入 、b充入
、b充入 ,在其他条件不变时,请在下图中分别画出平衡时
,在其他条件不变时,请在下图中分别画出平衡时 的体积分数随投料比
的体积分数随投料比 变化的曲线图,请用a、b标注曲线图。_________
变化的曲线图,请用a、b标注曲线图。_________
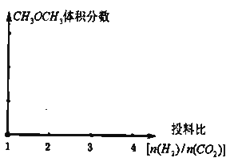
(3)在恒容密闭容器里按体积比为 充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是________________。
充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是________________。
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积分数增大
(4)温度、压强对反应中 平衡转化率和二甲醚的选择性的影响如下图1,图2:
平衡转化率和二甲醚的选择性的影响如下图1,图2:
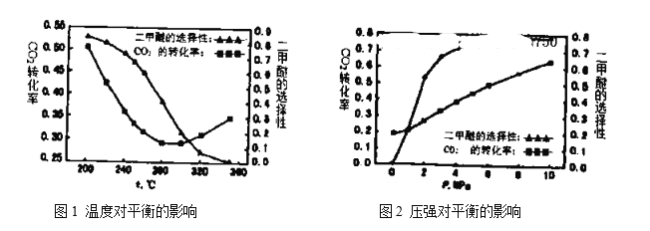
①根据图1,下列说法正确的是________。
A.温度较高时,反应以逆水汽变换反应为主,温度升高,反应速率加快,所以 转化率增大
转化率增大
B.温度较低时,反应以合成二甲醚为主,正反应放热,升高温度, 平衡转化率降低
平衡转化率降低
C.由图像可知, 加氢合成二甲醚应该选择具有良好的低温活性的催化剂
加氢合成二甲醚应该选择具有良好的低温活性的催化剂
D.由图像可知,高温有利于逆水汽变换反应,而不利于二甲醚的生成
②根据图2可知:随着压强升高, 平衡转化率和二甲醚的选择性都增大,分析原因:__________。
平衡转化率和二甲醚的选择性都增大,分析原因:__________。
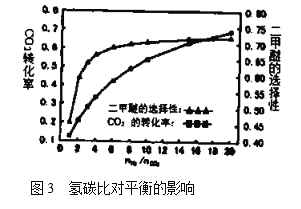
(5)在 ,压强为3.0MPa的反应条件下,氢碳比
,压强为3.0MPa的反应条件下,氢碳比 对
对 转化率和二甲醚选择性的影响见图3.分析实际工业生产中制备二甲醚选择氢碳比在3~6之间的原因:________________。
转化率和二甲醚选择性的影响见图3.分析实际工业生产中制备二甲醚选择氢碳比在3~6之间的原因:________________。
-
生物质能是一种洁净、可再生能源。生物质气(主要成分为 CO、CO2、H2 等)与H2混合,催化合成甲醇和二甲醚(CH3OCH3)及许多烃类物质等,是生物质能利用的方法之一.
(1)已知碳的气化反应在不同温度下平衡常数的对数值(lgK)如下表:

反应:CO(g)+H2O(g) CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.
CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.
(2)甲醇是一种重要的能源和化工原料,工业上合成甲醇的反应为:CO+2H2⇌CH3OH.现已知:H2(g)、CO(g)、CH3OH(l)的燃烧热ΔH分别为-285.8KJ/mol、-283.0KJ/mol和-726.5KJ/mol。则:CH3OH不完全燃烧生成CO和液态H2O的热化学反应方程式________.
(3)在一定温度、压强和催化条件下,工业上用CO和H2反应生成二甲醚,同时产生一种参与大气循环的无机物。则该反应的化学反应方程式为:________.
(4)下图左为绿色电源“二甲醚燃料电池”的工作原理示意图.a电极上发生反应的电极反应式为 ________ .
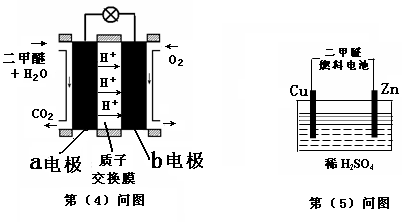
(5)连接下图右装置的电源为(4)问中的二甲醚燃料电池。接通电源一段时间后,观察到装置中电解质溶液颜色由无色变为蓝色,并逐渐加深。则该装置中的Cu电极应与二甲醚燃料电池中________ 电极(填a或b)相连。通电时发生反应的总的离子反应方程式为:________.
-
碳基能源的大量消耗使大气中CO2浓度持续不断地增加,以CO2为原料加氢合成,甲烷等能源物质具有较好的发展前景。回答下列问题:
(1)CO2催化(固体催化剂)加氢合成甲烷过程发生以下两个反应:
主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H1=akJ·mol-1
CH4(g)+2H2O(g) △H1=akJ·mol-1
副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2=41.1kJ·mol-1
CO(g)+H2O(g) △H2=41.1kJ·mol-1
已知相关的化学键键能数据如下:

则a=___。加氢合成甲烷时,通常控制温度为500℃,不能过高也不宜过低的原因是___。
(2)为了提高CO2加氢制CH4过程中CH4选择性(CH4选择性= ×100%),主要是通过对催化剂的合理选择来实现。
×100%),主要是通过对催化剂的合理选择来实现。
①CO2加氢制CH4的一种催化机理如图,下列说法正确的是___(填标号)。
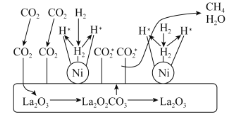
A.催化过程使用的催化剂为La2O3和La2O2CO3
B.La2O2CO3可以释放出CO2*(活化分子)
C.H2经过Ni活性中心裂解产生活化态H*的过程为放热过程
D.CO2加氢制CH4的过程需要La2O3和Ni共同催化完成
②保持500℃不变,向1L密闭容器中充入4molCO2和12molH2发生反应,若初始压强为p,20min后,主、副反应都达到平衡状态,测得此时c(H2O)=5mol·L-1,体系压强变为0.75p,则主、副反应的综合热效应为___,v(CH4)=___mol·L-1·min-1,CH4选择性=___(保留三位有效数字),主反应的平衡常数K=___。
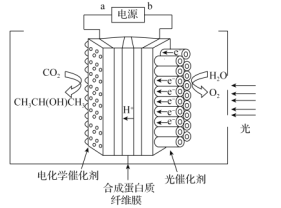
(3)CO2的光电催化反应器如图所示。以TiO2为阳极,通过光解水产生电子和质子,而后传递到阴极(Pt/CNT)诱导阴极催化还原CO2制得异丙醇。
①阴极常伴有析氢等副反应发生,为此选用了电化学催化剂,其依据是___。
②阴极生成异丙醇的电极反应为___。
-
CO2催化加氢制甲醇,是极具前景的温室气体资源化研究领域。在某CO催化加氢制甲醇的反应体系中,发生的主要反应有:
i.CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g)  CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g)  CH3OH(g) △H3
CH3OH(g) △H3
(1)△H3________ kJ·mol-1
(2)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
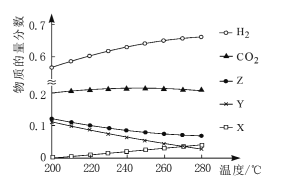
①体系中CO2的物质的量分数受温度的影响不大,原因是____。
②250℃时,反应ii的平衡常数____1(填“>”“<”或“=”)。
③下列措施中,无法提高甲醇产率的是____(填标号)。
A 加入适量CO B 增大压强 C 循环利用原料气 D 升高温度
④如图中X、Y分别代表____(填化学式)。
(3)反应i可能的反应历程如下图所示。
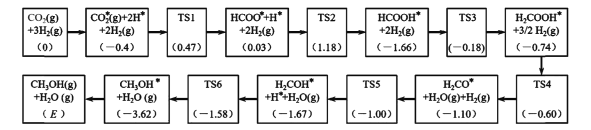
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中,TS表示过渡态、*表示吸附在催化剂上的微粒。
①反应历程中,生成甲醇的决速步骤的反应方程式为____。
②相对总能量E=____(计算结果保留2位小数)。(已知:leV=1.6×10-22kJ)
(4)用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,往电解池的____极通入氢气,阴极上的电极反应为____。
资源化利用的方法之一是合成二甲醚(
简写做
)。
催化加氢法合成
,其过程中主要发生下列反应:
和
的起始量一定的条件下,
的平衡转化率和平衡时
、
的选择性随压强或温度的变化见下图。已知:
的选择性
 ;
;的选择性



的选择性应当选择的条件为________。
平衡转化率随温度升高而降低的原因是_______。
与足量
发生反应,达到平衡时
的转化率为40%,部分物质的物质的量如下表:
的选择性为________,反应Ⅳ的化学平衡常数为________。
的浓度均很低,则可知活化能大小关系:反应Ⅲ________反应Ⅳ(填“大于”、“小于”或“等于”)。
,投料比为
时进行反应,
的浓度随时间变化如下图所示,则下列说法正确的为________。

范围内,反应Ⅰ的速率随温度升高而增大
的浓度始终增大
的浓度先增大后减小最终不变
后
的浓度减小是因为随时间推移反应Ⅱ的进行使体系中
浓度越来越高,反应Ⅰ的逆反应速率不断增大,从而使
浓度逐渐下降
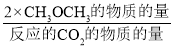 ×100%
×100%