-
以煤为原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol,
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
请写出甲醇燃烧生成H2O(g)的热化学方程式_________;
(2)向1 L密闭容器中加入2 mol CO、4 mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)⇌CH3OCH3(l)+H2O(l) ΔH=+71 kJ/mol
①该反应能否_________自发进行(填“能”、“不能”或“无法判断”)
②下列叙述能说明此反应达到平衡状态的是_________.
a.混合气体的平均相对分子质量保持不变 b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变 d.混合气体的密度保持不变
e.1 mol CO生成的同时有1 mol O-H键断裂
(3)CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH<0在一定条件下,某反应过程中部分数据如下表:
反应条件
反应时间
CO2(mol)
H2(mol)
CH3OH(mol)
H2O(mol)
恒温恒容
(T1℃、2L)
0min
2
6
0
0
10min
4.5
20min
1
30min
1
①0~10 min内,用H2O(g)表示的化学反应速率v(H2O)=_________mol/(L·min);
②达到平衡时,该反应的平衡常数K=_________(用分数表示),平衡时H2的转化率是_________;
③在其他条件不变的情况下,若30 min时向容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡_______移动(填“正向”、“逆向”或“不”);
(4)用甲醚(CH3OCH3)作为燃料电池的原料,请写出在碱性介质中电池负极反应式_________。
高二化学综合题中等难度题查看答案及解析
-
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
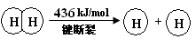

下列说法不正确的是
A.该反应原理可用于设计氢氧燃料电池
B.破坏1 mol H—O 键需要的能量是463.4 kJ
C.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
D.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
高二化学选择题中等难度题查看答案及解析
-
已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJ·mol−1
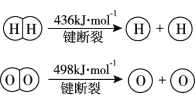
下列说法不正确的是
A.该反应可作为氢氧燃料电池的反应原理
B.破坏1 mol H-O键需要的能量是463.4 kJ
C.H2的燃烧热ΔH<-241.8 kJ·mol−1
D.H2(g)中的H-H键比H2O(g)中的H-O键牢固
高二化学单选题简单题查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(g),△H=-483.6kJ/mol,下列说法错误的是( )
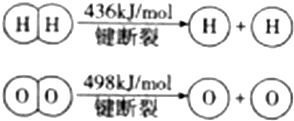
A.该反应原理可用于设计氢氧燃料电池
B.破坏1mol H-O键需要的能量是926.8kJ
C.H2O(g)=H2(g)+
O2(g)△H=+241.8kJ/mol
D.H2(g)中的H-H键比H2O(g)中的H-O键能小
高二化学选择题中等难度题查看答案及解析
-
I.将CO2转化成甲醇燃料是减排、环保的一种科学方法。
已知:2H2(g)+O2(g) =2H2O(g);△H=-483.6kJ·mol-1 ①
2CO2(g)+4H2O(g)
2CH3OH(g)+3O2(g);ΔH=+1352.8kJ·mol-1②
则用CO2与H2反应制备 CH3OH(g),同时生成水蒸气的热化学方程式为___________________
II.在容积为2L的密闭容器中,进行如下反应:A(g)+2B(g)
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。
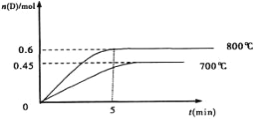
试回答下列问题:
(1)800℃时,0—5min内,以B表示的平均反应速率为____________。
(2)能判断该反应达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中c(A)不变
c.2v正(B)=v逆(D) d.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=________,该反应为_______反应(填吸热或放热),判断理由是______________________________。
(4)800℃时,某时刻测得体系中各物质的量如下:n(A)=0.9mol,n(B)=2.0mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应________进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
高二化学综合题中等难度题查看答案及解析
-
已知下列热化学方程式:
①2H2(g)+O2 (g)=2H2O(l);△H=-570kJ•mol-1
②2H2(g)+O2 (g)=2H2O(g);△H=-483.6kJ•mol-1
③C(s)+O2 (g)=CO(g);△H=-110.5kJ•mol-1
④C(s)+O2 (g)=CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)H2的燃烧热为______;
(2)燃烧1gH2生成液态水,放出的热量为______.
(3)写出CO燃烧的热化学方程式______.高二化学解答题中等难度题查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1
现有1g液态H2O,蒸发时吸收的热量是( )
A.2.44 kJ B.4.88 kJ C.44.0 kJ D.88.0 kJ
高二化学选择题简单题查看答案及解析
-
已知
2H2(g)+O2(g)=2H2O(g), △H=-483.6kJ·mol-1
2H2(g)+O2(g)=2H2O(l), △H=-571,6 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l), △H=-2220kJ·mol-1根据上述热化学方程式,回答下列问题:
(1)H2的燃烧热△H为__________,C3H8的燃烧热△H为__________.
(2)1molH2和2molC3H8组成的混合气体完全燃烧恢复到室温时释放的热量为__________.
(3)现有H2和C3H8的混合气体共5mol,完全燃烧恢复到室温时放热3847kJ,则在混合气体中H2和C3H8的体积比是__________。
高二化学计算题简单题查看答案及解析
-
10.已知热化学方程式:
(1)2H2O(l)===2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
(2)2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
当1 g液态水变为气态水时,对其热量变化有下列描述:①放出;②吸收;③2.44 kJ;④4.88 kJ;⑤88 kJ。其中正确的是
A.②和⑤ B.①和③ C.②和③ D.②和④
高二化学选择题中等难度题查看答案及解析
-
已知下列热化学方程式:①2H2(g)+O2(g)=2H2O(l)△H=﹣570kJ/mol,②2H2O(g)=2H2(g)+O2(g)△H=+483.6kJ/mol,③2CO(g)=2C(s)+O2(g)△H=+220.8kJ/mol,④2C(s)+2O2(g)=2CO2(g)△H=﹣787kJ/mol,回答下列问题:
(1)上述反应中属于放热反应的是_____(填写序号)。
(2)H2的燃烧热为_____。
(3)燃烧10g H2生成液态水,放出的热量为______。
(4)H2O(g)=H2O(l)△H=________。
(5)C(s)的燃烧热的热化学方程式为_______。
高二化学计算题中等难度题查看答案及解析