按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
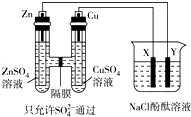
A.11 B.12 C.13 D.14
高三化学选择题困难题
按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )

A.11 B.12 C.13 D.14
高三化学选择题困难题
按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )

A.11 B.12 C.13 D.14
高三化学选择题困难题查看答案及解析
按如图所示装置连接,X、Y均为惰性电极,常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
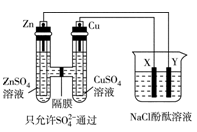
A.11 B.12 C.13 D.14
高三化学选择题中等难度题查看答案及解析
用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。
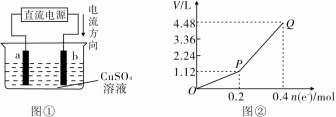
(1)电解过程中,a电极表面的现象是___________________________________;
(2)a电极上发生的反应为________________________________________________;
(3)从P点到Q点时收集到的混合气体的平均摩尔质量为___________ g·mol-1;
(4)如果要使溶液恢复到电解前的状态,向溶液中加入0.8 g CuO即可,则电解后溶液的pH为______;
(5)如果向所得的溶液中加入0.1 mol Cu2(OH)2CO3后,使溶液恰好恢复到电解前的浓度和pH(不考虑CO2的溶解),电解过程中转移的电子为______mol。
高三化学填空题困难题查看答案及解析
用惰性电极电解100mLCuSO4稀溶液,一段时间内,阴极无气体生成时,在阳极收集到气体56mL(标准状况),若不考虑Cu2+的水解和溶液体积的变化,则此时电解液的pH为
A.1 B.0 C.2 D.13
高三化学选择题中等难度题查看答案及解析
标准状况下;用惰性电极电解200 mL NaCl、CuSO4的混合溶液;阴、阳两极所得气体的体积随时间变化如图所示;则 c(CuSO4)为
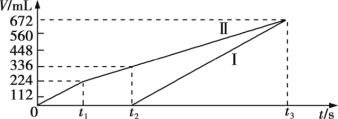
A. 0.10 mol·L−1 B. 0.15 mol·L−1 C. 0.20 mol·L−1 D. 0.25 mol·L−1
高三化学单选题中等难度题查看答案及解析
(1)用惰性电极电解CuSO4溶液(如图的装置),
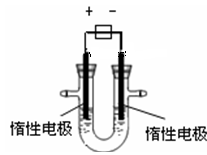
该过程中电解池电极反应式为是阳极: , 阴极: 。
(2)若电解池中装入足量溶液,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为 (假设气体全部逸出)。
(3)欲使电解液恢复到起始状态,应向溶液中加入适量的
A.CuSO4 B.H2O C.CuO D.CuSO4·5H2O
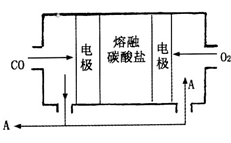
(4)用Na2CO3熔融盐作电解质,CO、O2为原料组成的新型电池的研究取得了重大突破。该电池示意图如右:负极电极反应式为_________________________,为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的化学式为__________________。
高三化学填空题简单题查看答案及解析
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲,电解过程中的实验数据如图乙。横坐标表示转移电子的物质的量,纵坐标表示产生气体的总体积(标准状况)。则下列说法不正确的是

A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的反应方程式为:4OH--4e- = 2H2O+O2↑
C.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/ mol
D.从开始到P点收集到的气体是O2
高三化学选择题困难题查看答案及解析
用惰性电极电解50 mL锰酸钾溶液:K2MnO4+H2O→KMnO4+H2↑+KOH(未配平),当生成112 mL氢气(标准状况)时停止通电。下列判断正确的是 ( )
A.K+浓度减小 B.KMnO4在阳极区生成
C.阴极周围溶液的pH减小 D.反应过程中共转移0.005mol电子
高三化学选择题简单题查看答案及解析
用惰性电极电解50 mL锰酸钾溶液:K2MnO4+H2O→KMnO4+H2↑+KOH(未配平),当生成112 mL氢气(标准状况)时停止通电。下列判断正确的是 ( )
A.K+浓度减小 B.KMnO4在阳极区生成
C.阴极周围溶液的pH减小 D.反应过程中共转移0.005mol电子
高三化学单选题中等难度题查看答案及解析
用惰性电极电解50 mL锰酸钾溶液:K2MnO4+H2O→KMnO4+H2↑+KOH(未配平),当生成112 mL氢气(标准状况)时停止通电。下列判断正确的是 ( )
A.K+浓度减小 B.KMnO4在阳极区生成
C.阴极周围溶液的pH减小 D.反应过程中共转移0.005mol电子
高三化学选择题中等难度题查看答案及解析