-
SCR法是工业上消除NOx的常用方法,其原理为:4NH3(g)+4NO(g)+O2(g)  4N2(g)+6H2O(g) △H<0。
4N2(g)+6H2O(g) △H<0。
(1)NOx破坏臭氧层原理为:①NO+O3 NO2+O2 K1 ②NO2+O
NO2+O2 K1 ②NO2+O NO+O2 K2;则O3+O
NO+O2 K2;则O3+O 2O2的K=__________(用K1、K2表示),NOx在该反应中的作用是________。
2O2的K=__________(用K1、K2表示),NOx在该反应中的作用是________。
(2)SCR法除NO时,投料比一定时利于提高NO平衡转化率的反应条件是________、________。该法可能发生副反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),减小副反应的主要措施是______、________。
4NO(g)+6H2O(g),减小副反应的主要措施是______、________。
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
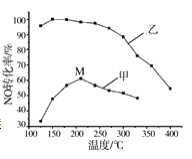
①工业上选择催化剂乙的原因是__________;
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率________(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。
(4)消除汽车尾气中的NO时,可用CO(NH2)2还原NO,与SCR法相比,等物质的量的CO(NH2)2与NH3可消除的NO物质的量之比为_________。(不考虑副反应)
-
氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一。SCR法是工业上消除氮氧化物的常用方法,反应原理为:
4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H<0
4N2(g)+6H2O(g) △H<0
(1)氮氧化物破坏臭氧层原理为:①NO+O3 NO2+O2 ②NO2+O
NO2+O2 ②NO2+O NO+O2
NO+O2
常温下反应①的平衡常数为K1,反应②的平衡常数为K2,则反应O3+O 2O2的平衡常数K =________(用K1、K2表示)。
2O2的平衡常数K =________(用K1、K2表示)。
(2)SCR法除NO时,投料比一定时有利于提高NO平衡转化率的反应条件是________、________。该法可能发生副反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
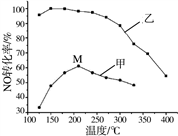
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
①工业上选择催化剂乙的原因是________;
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率_________(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是________。
(4)消除汽车尾气中的NO时,可用尿素[(NH2)2CO]还原NO,既安全又高效,且产物都是空气中含有的成分。与SCR法相比,等物质的量的尿素与氨气可消除的NO物质的量之比为________。(不考虑副反应)
-
选择性催化还原法(SCR)烟气脱硝技术是一种成熟的NOx控制处理方法,主要反应如下:
①4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H1=a kJ·mol-1
4N2(g)+6H2O(g) △H1=a kJ·mol-1
②4NH3(g)+2NO2(g)+O2(g) 3N2(g)+6H2O(g) △H2=b kJ·mol-1
3N2(g)+6H2O(g) △H2=b kJ·mol-1
副反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H4=d kJ·mol-1
4NO(g)+6H2O(g) △H4=d kJ·mol-1
可以计算出反应2NO(g)+O2(g) 2NO2(g)的△H为( )
2NO2(g)的△H为( )
A. (4b-3a+d)/4 B. (4a-3b+d)/4 C. (3b-4a+d)/4 D. (3a-4b+d )/4
-
氮氧化物(NOx)是电厂主要排放污染物之一。工业上采用氨脱硝处理后排放,原理如下:
①4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H1=-1632.4kJ·mol-1
4N2(g)+6H2O(g) △H1=-1632.4kJ·mol-1
②4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H2=akJ·mol-1
5N2(g)+6H2O(g) △H2=akJ·mol-1
当反应温度过高时,NH3会发生氧化反应:③NH3(g)+5O2(g) 4NO(g)+6H2O(g)、△H3=-902.0kJ·mol-1
4NO(g)+6H2O(g)、△H3=-902.0kJ·mol-1
回答下列问题:
(1)有利于提高反应①中NO转化率(脱硝率)的条件是___________(填标号)。
A.高温低压 B.低温低压 C.低温高压 D.增大氨气浓度
(2)反应②中的a=___________。温度下,实验室在2L密闭容器中加入2 molNH3、3 molNO模拟反应②,达到平衡时测得脱硝率为60%,则平衡常数Ke=___________(只列出计算式,不必求出计算结果)。
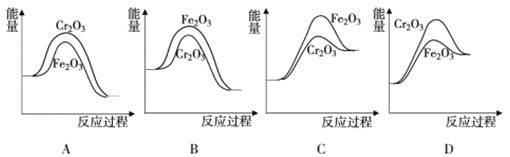
(3)反应③中,常用的催化剂有Cr2O3和Fe2O3,Cr2O3的催化效率更好一些。下列表示两种催化剂在反应③催化过程中的能量变化示意图合理的是___________(填字母序号)。
(4)下图为混合气中O2含量6%时,不同温度下脱硝率的变化曲线[其中氨氮摩尔比RNS=n(NH3)/n(NO)],由图可知:
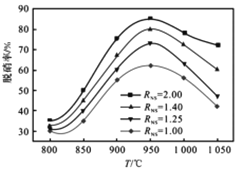
(i)氨氮摩尔比对脱硝率的影响规律是______________________。
(ⅱ)温度在800-950℃变化时,脱硝率随温度升高而___________,但高于950℃后,脱硝率反而下降,一方面是由于平衡移动的影响,另一方面是由于___________。
-
(11分)工业制硝酸的主要反应是:4NH3(g)+5O2(g) 4NO(g)+6H2O (g) ΔH=" -1025" KJ/mol
4NO(g)+6H2O (g) ΔH=" -1025" KJ/mol
(1)一定温度下,现将0.8mol NH3和1.5mol O2充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________
(2)在容积为1L的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.5 | 0 |
| 第2min | 0.7 | a | 0.1 |
| 第4min | 0.4 | 1.0 | 0.4 |
| 第6min | 0.4 | 1.0 | 0.4 |
| 第8min | 1.2 | 2.5 | 0.4 |
①起始时物料比c (O2) : c (NH3)>1.25,其原因是________
②反应在第2min到第4min时O2的平均反应速率为________ mol·L-1·min-1
③反应在第2min改变了反应条件,改变的条件可能是________(填字母序号)
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是________,再次达到平衡时,NO的体积分数________(填“增大”、“减小”或“不变”)
(3)室温下,将第一次达到平衡时的混合气体通入水中,然后向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中,溶液中水的电离平衡将________(填“正向”“ 逆向”或“不”)移动,所滴加氨水的浓度为________mol·L-1。(NH3·H2O的电离平衡常数Kb=2×10-5 mol·L-1)
-
工业制硝酸的主要反应是:4NH3(g)+5O2(g) 4NO(g)+6H2O (g) ΔH= -1025 KJ/mol
4NO(g)+6H2O (g) ΔH= -1025 KJ/mol
(1)一定温度下,现将0.8mol NH3和1.5mol O2充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________

(2)在容积为1L的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.5 | 0 |
| 第2min | 0.7 | a | 0.1 |
| 第4min | 0.4 | 1.0 | 0.4 |
| 第6min | 0.4 | 1.0 | 0.4 |
| 第8min | 1.2 | 2.5 | 0.4 |
①起始时物料比c (O2) : c (NH3)>1.25,其原因是________
②反应在第2min到第4min时O2的平均反应速率为________ mol·L-1·min-1
③反应在第2min改变了反应条件,改变的条件可能是________(填字母序号)
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是________,再次达到平衡时,NO的体积分数________
________(填“增大”、“减小”或“不变”)
-
SCR法(选择性催化还原技术)是一种以NH3作为还原剂,将烟气中NOx,分解成无害的N2和H2O的干法脱硝技术,反应原理为:
① 6NO+4NH3=5N2+6H2O ② 6NO2+8NH3=7N2+12H2O ③ NO+NO2+2NH3=2N2+3H2O
下列说法正确的是
A.NO2为酸性氧化物
B.H2O很稳定是因为水分子之间存在氢键
C.反应③中每生成22.4 LN2,转移电子数1.5NA
D.NH3的沸点比PH3的沸点高
-
SCR法(选择性催化还原技术)是一种以NH3作为还原剂,将烟气中NOx分解成无害的N2和H2O的干法脱硝技术,反应原理为:①6NO+4NH3=5N2+6H2O;②6NO2+8NH3=7N2+12H2O;③NO+NO2+2NH3=2N2+3H2O
下列说法正确的是
A.NOx主要来自于汽车尾气的排放,是引起温室效应的主要气体之一
B.N2中π键与σ键之比为1:2
C.反应③中每生成22.4LN2,转移电子数1.5NA
D.NH3的沸点比PH3的沸点高
-
下列解释事实的方程式不准确的是
A.铝热法炼铁:Fe2O3 + 2Al 高温 Al2O3 + 2Fe
B.工业上用NH3制备NO:4NH3 + 5O2高温 4NO + 6H2O
C.向受酸雨影响的湖泊中喷洒CaCO3粉末:CO32- + 2H+催化剂 H2O + CO2↑
D. 过氧化钠用于呼吸面具中作为氧气的来源:2Na2O2 + 2CO2 ==2Na2CO3 + O2
-
硝酸生产中,500℃时,NH3和O2可能发生如下反应:
① 4NH3 (g)+ 5O2 (g) 4NO (g)+ 6H2O (g)△H = -9072kJ·mol-1 K=1.1×1026
4NO (g)+ 6H2O (g)△H = -9072kJ·mol-1 K=1.1×1026
② 4NH3 (g)+ 4O2 (g) 2N2O (g)+ 6H2O (g)△H=-1104.9kJ·mol-1 K=4.4×1028
2N2O (g)+ 6H2O (g)△H=-1104.9kJ·mol-1 K=4.4×1028
③ 4NH3 (g)+ 3O2 (g) 2N2 (g)+ 6H2O (g)△H=-1269.02kJ·mol-1 K=7.1×1034
2N2 (g)+ 6H2O (g)△H=-1269.02kJ·mol-1 K=7.1×1034
其中,②、③是副反应。若要减少副反应,提高单位时间内NO的产率,最合理的措施是
A.增大O2浓度 B.使用合适的催化剂 C.减小压强 D.降低温度
4N2(g)+6H2O(g) △H<0。
NO2+O2 K1 ②NO2+O
NO+O2 K2;则O3+O
2O2的K=__________(用K1、K2表示),NOx在该反应中的作用是________。
4NO(g)+6H2O(g),减小副反应的主要措施是______、________。





