-
根据20℃时某些物质的溶解度(g)数据:
| CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| 1.4×10-3 | 2.55×10-2 | 9×10-4 | 1.1×10-2 |
下列说法不正确的是
A.硫酸钙悬浊液中存在CaSO4(s) Ca2+(aq)+ SO42-(aq)
Ca2+(aq)+ SO42-(aq)
B.用Na2CO3溶液浸泡锅炉中的水垢,可将水垢中的CaSO4转化为CaCO3
C.向Mg(OH)2悬浊液中滴加FeCl3,沉淀变为红褐色,说明溶解度Fe(OH)3< Mg(OH)2
D.向2ml饱和MgCl2 溶液中先后滴加0.1mol/L的Na2CO3、NaOH溶液各2滴,产生的白色沉淀为Mg(OH)2
-
常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:
| CaSO4 | CaCO3 | MgCO3 | Mg(OH)2 | CuS | BaSO4 | H2S | H2CO3 |
| Ksp或Ka | 9.1×10﹣6 | 2.8×10﹣9 | 6.8×10﹣6 | 1.8×10﹣11 | 6.3×10﹣36 | 1.1×10﹣10 | K1=1.3×10﹣7 K2=7.1×10﹣15 | K1=4.4×10﹣7 K2=4.7×10﹣11 |
则下列说法不正确的是
A. 相同温度、相同浓度的钠盐溶液的pH:Na2S>Na2CO3>NaHS>NaCl>NaHSO4
B. 在NaHS溶液中滴加硫酸铜溶液,生成黑色沉淀:HS﹣+Cu2+=CuS↓+H+
C. 除去锅炉中水垢时,通常先加入足量硫酸钠溶液,将碳酸钙转化成硫酸钙,然后再用酸液处理
D. 在Mg(HCO3)2溶液中滴加足量澄清石灰水发生反应的离子方程式为:Mg2++2HCO3﹣+2Ca2++4OH﹣=Mg(OH)2↓+2CaCO3↓+2H2O
-
常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:
| CaSO4 | CaCO3 | MgCO3 | Mg(OH)2 | CuS | BaSO4 | H2S | H2CO3 |
| Ksp或Ka | 9.1×10﹣6 | 2.8×10﹣9 | 6.8×10﹣6 | 1.8×10﹣11 | 6.3×10﹣36 | 1.1×10﹣10 | K1=1.3×10﹣7 K2=7.1×10﹣15 | K1=4.4×10﹣7 K2=4.7×10﹣11 |
则下列说法不正确的是
A.相同温度、相同浓度的钠盐溶液的pH:Na2S>Na2CO3>NaHS>NaCl>NaHSO4
B.在NaHS溶液中滴加硫酸铜溶液,生成黑色沉淀:HS﹣+Cu2+=CuS↓+H+
C.除去锅炉中水垢时,通常先加入足量硫酸钠溶液,将碳酸钙转化成硫酸钙,然后再用酸液处理
D.在Mg(HCO3)2溶液中滴加足量澄清石灰水发生反应的离子方程式为:Mg2++2HCO3﹣+2Ca2++4OH﹣=Mg(OH)2↓+2CaCO3↓+2H2O
-
家用水壶中积存的水垢的主要成分是 ( )
A.CaCO3和MgCO3 B.Mg(OH)2和CaCO3
C.CaSO4和MgC03 D.A12O3和CaCO3
-
某研究性学习小组为研究水垢的生成,查得CaCO3和Mg(OH)2溶解度曲线如图所示。已知:40°C时,Ksp(MgCO3)=7×10-6,下列有关分析错误的是( )
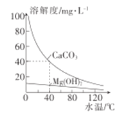
A.CaCO3、Mg(OH)2溶解均放热
B.MgCl2溶液中加入少量CaCO3粉末加热搅拌,有Mg(OH)2生成
C.含有Ca(HCO3)2和Mg(HCO3)2的自来水长时间加热,水垢的主要成分为CaCO3和MgCO3
D.40℃时,Ksp(CaCO3)=1.6×10-7
-
下列为某同学根据中学化学教材中数据所做的判断,其中错误的是 ( )
A.根据溶解度数据,判断长时间煮沸Mg(HCO3)2溶液所得的沉淀是MgCO3还是Mg(OH)2
B.根据沸点数据,判断能否用分馏的方法分离一些液体混合物
C.根据反应热数据,判断不同反应的反应速率的大小
D.根据晶格能的数据,判断离子晶体的稳定性
-
常温下,有关物质的溶度积如下
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
B.常温下,除去NaCl溶液中的CaCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
C.向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg 2+)∶c(Fe3+)=2 .125×1021
D.将适量的Ca(OH)2固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.054×10-2mol/L],若保持温度不变, 向其中加入100mL 0.012mol/L的NaOH,则该溶液变为不饱和溶液。
-
常温下,有关物质的溶度积如下表所示。
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
B.常温下,除去NaCl溶液中的CaCl2杂质,选用Na2CO3溶液比NaOH溶液效果好
C.常温下,向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021:1
D.无法利用Ca(OH)2制备NaOH
-
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
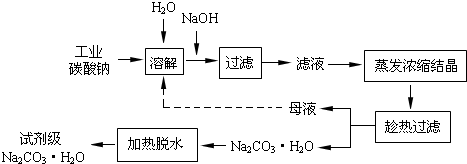
(1)加入NaOH溶液时,反应的离子方程式为__________________;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= ___________;
(3)“母液”中除了含有Na+、CO32-外,还含有_________等离子。
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行_________(填“可行”或“不可行”),并说明理由__________________;
(5)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g) △H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式__________________;
-
从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10–9 | 6.8×10–6 | 5.5×10–6 | 1.8×10–11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成份是碳酸钙),你认为________(填“能”或“不能”)将贝壳研磨成粉末直接投入海水中,理由是________;如果不能直接投入,应将贝壳作何处理,试写出化学方程式。
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用烧碱代替,你认为________(填“可以”或“不可以”)得到Mg(OH)2。在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他________(填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是________(用离子方程式表示)。
(3)已知海水中镁离子浓度为1.8×10–3mol·L–1,则要使镁离子产生沉淀,溶液的PH最低应为________。
Ca2+(aq)+ SO42-(aq)

