-
S2Cl2是工业上常用的硫化剂,已知S2C12中硫元素显+1价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂。实验室常用CS2与纯净的氯气制备S2C12。反应涉及到的几种物质的熔沸点如下:
| 物质 | CS2 | Cl2 | CCl4 | S2C12 |
| 沸点/℃ | 47 | -34.6℃ | 77 | 137 |
| 熔点/℃ | -109 | -100.98℃ | -23 | -77 |
实验室利用下列装置制备S2C12 (部分夹持仪器己略去):
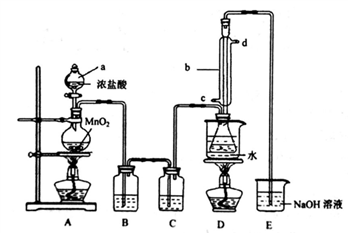
回答下列问题:
(1)装置中b玻璃仪器的名称为_______;写出制备S2C12的化学方程式_______。
(2)整套装置装配完毕后,首先进行的操作是________,再添加试剂。
(3)实验中盐酸试剂通常采用36.5%的浓盐酸,不用稀盐酸的理由是________。
装置A中反应的离子方程式是___________。
(4) D中采用热水浴加热的原因是__________,反应结束后从锥形瓶内混合物中分离出产品的方法是_______________。
(5)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因化学方程式表示为__________。
(6)该实始装置设计存在缺陷,你的改进建议及改进目的是_______________。
-
 是工业上常用的硫化剂,已知
是工业上常用的硫化剂,已知 中硫元素显
中硫元素显 价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂。实验室常用
价,它不稳定,在水中易发生岐化反应,易溶于有机溶剂。实验室常用 与纯净的氯气制备
与纯净的氯气制备 。反应涉及到的几种物质的熔沸点如下:
。反应涉及到的几种物质的熔沸点如下:
实验室利用下列装置制备 (部分夹持仪器己略去):
(部分夹持仪器己略去):

回答下列问题:
(1)装置中b玻璃仪器的名称为_________;写出制备 的化学方程式_________。
的化学方程式_________。
(2)D中采用热水浴加热的原因是 _________,反应结束后从锥形瓶内混合物中分离出产品的方法是______。
(3)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因化学方程式表示为______________。
(4)该实始装置设计存在缺陷,你的改进建议是 _________________________________。
-
S2Cl2是工业上常用的硫化剂,实验室制备的方法有2种:
 已知在S2Cl2中硫元素显+1价,电子式:
已知在S2Cl2中硫元素显+1价,电子式: ,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
实验室利用下列装置制备 (部分夹持仪器已略去):
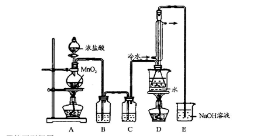
回答下列问题:
(1)写出A装置中发生反应的离子方程式
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是
(3)D中冷凝管起到导气和冷凝回流双重作用。这种冷却装置可应用于下列高中化学中 实验。
A.石油分馏 B.制备乙烯 C.制取乙酸乙酯 D.制取溴苯
(4)B装置中盛放的是 ,反应结束后从锥形瓶内混合物中分离出产品的方法是 ,D中采用热水浴加热的原因是
(5)A装置仪器装配时,整套装置装配完毕后,应先进行 ,再添加试剂。实验完毕,拆除装置时,应先将E中长导管移开液面,目的是
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为 。实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是 (用离子方程式表示)。
-
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
① CS2+3Cl2 CCl4+S2Cl2;② 2S+Cl2
CCl4+S2Cl2;② 2S+Cl2 S2Cl2。
S2Cl2。
已知S2Cl2中硫元素显+1价,电子式: ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
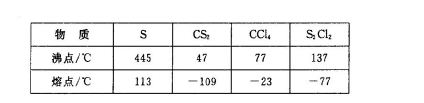
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
实验室利用下列装置制备S2Cl2(部分夹持仪器已略去):
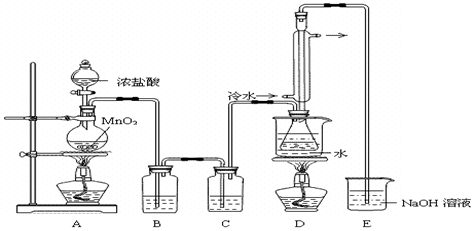
回答下列问题:
(1)装置B、C中玻璃容器的名称:________;反应原理(填写数字序号):________。
(2)实验中盐酸试剂通常采用36.5%的浓溶液,不用稀盐酸的理由是________ 。
(3)D中冷凝管起到导气和冷凝双重作用,其冷却水流动方向与热气流流动方向相同(见图)。这种冷却方式可应用于下列高中化学中________实验。
A.石油分馏 B.制取溴苯 C.制取乙酸乙酯 D.制备阿司匹林
(4)B装置中盛放的是________,反应结束后从锥形瓶内混合物中分离出产品的方法是________,D中采用热水浴加热的原因是________。
(5)A部分仪器装配时,放好铁架台后,应先固定________(填仪器名称),整套装置装配完毕后,应先进行________再添加试剂。实验完毕,A中不再产生氯气时,可拆除装置。拆除时,最先的操作应当是。
(6)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因可用化学方程式表示为________ 。实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是:________(用离子方程式表示)。
-
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:①CS2+3Cl2 CCl4+S2Cl2;②2S+Cl2
CCl4+S2Cl2;②2S+Cl2 S2Cl2.已知S2Cl2中硫元素显+1价,电子式:
S2Cl2.已知S2Cl2中硫元素显+1价,电子式: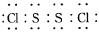 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低),反应涉及的几种物质的熔沸点如表:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低),反应涉及的几种物质的熔沸点如表:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | ﹣109 | ﹣23 | ﹣77 |
实验室利用下列装置制备S2Cl2(部分夹持仪器已略去)。回答下列问题:
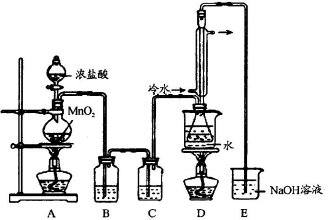
(1)写出A装置中发生反应的离子方程式____ ___。
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是__________。
(3)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中_ _____实验。
A.石油分馏 B.制备乙烯
C.制取乙酸乙酯 D.制取溴苯
(4)B装置中盛放的是_________,反应结束后从锥形瓶内混合物中分离出产品的方法是_________,D中采用热水浴加热的原因是__________。
(5)A装置仪器装配时,整套装置装配完毕后,应先进行__________,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是__________。
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清,出现该现象的原因可用化学方程式表示为______________。实验完毕,当把剩余浓盐酸倒人E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是___ _____。(用离子方程式表示)
-
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的方法有2种:
①CS2+3Cl2 CCl4+S2Cl2;②2S+Cl2
CCl4+S2Cl2;②2S+Cl2 S2Cl2.已知S2Cl2中硫元素显+1价,S2Cl2不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).
S2Cl2.已知S2Cl2中硫元素显+1价,S2Cl2不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).
反应涉及的几种物质的熔沸点如表:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
实验室利用下列装置通过方法①来制备S2Cl2(部分夹持仪器已略去)。回答下列问题:

(1)S2Cl2分子中各原子都满足最外层8电子结构,则其电子式为____ ___。
(2)实验中盐酸通常采用36.5%的浓溶液,不用稀盐酸的理由是__________。
(3)D中采用热水浴加热的原因是__________。
(4)D中冷凝管起到导气和冷凝回流双重作用.这种冷却装置可应用于下列高中化学中_ _____实验。
A.银镜反应 B.制取乙酸乙酯 C.制取溴苯 D.制备乙烯
(5)A装置仪器装配时,整套装置装配完毕后,应先进行气密性检查,再添加试剂.实验完毕,拆除装置时,应先将E中长导管移开液面,目的是__________。
(6)实验过程中,若缺少C装置,则发现产品浑蚀不清且生成两种有刺激性气味的气体,出现该现象的原因可用化学方程式表示为____________。实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的浓氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是 。(用离子方程式表示)
-
S2C12是一种金黄色易挥发的液体,常用作橡胶硫化剂。某化学兴趣小组 拟设计实验制备少量的S2C12,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价 降低)。加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2C12,反应的化学方程式为:2S+Cl2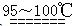 S2Cl2。
S2Cl2。
反应涉及的几种物质的熔沸点如下:
| 物质 | S | S2Cl2 |
| 沸点/℃ | 445 | 138 |
| 熔点/℃ | 113 | -76 |
该小组设计的制备装置如下图(夹持仪器已略去)
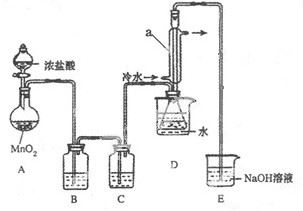
回答下列问题:
(1)连接好实验装置后的第一步实验操作是______。
(2)实验中需要加热的仪器是 (填写字母)
(3)装置B、C中的试剂分别是 。
(4)装置D中仪器a的作用是 。
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是____________。
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因____________。
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气体产生。用离子方程式表示产生该现象的原因____________。
-
S2C12是一种金黄色易挥发的液体,常用作橡胶硫化剂。某化学兴趣小组 拟设计实验制备少量的S2C12,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价 降低)。加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2C12,反应的化学方程式为:2S+Cl2 S2Cl2。
S2Cl2。
反应涉及的几种物质的熔沸点如下:
| 物质 | S | S2Cl2 |
| 沸点/℃ | 445 | 138 |
| 熔点/℃ | 113 | -76 |
该小组设计的制备装置如下图(夹持仪器已略去

回答下列问题:
(1)连接好实验装置后的第一步实验操作是______。
(2)实验中需要加热的仪器是______。(填 写 字 母)
(3)装置B、C中的试剂分别是______。
(4)装置D中仪器a的作用是______。
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是____________。
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因____________
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气 体产生。用离子方程式表示产生该现象的原因____________。
-
S2C12是橡胶工业上常用的硫化剂,是一种金黄色液体。
已知:①S2C12不稳定,进一步氯化可得SCl2;②S2Cl2、SCl2都能与水反应,  ==
==  ==
== ;③几种物质的熔沸点如表:
;③几种物质的熔沸点如表:
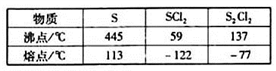
下图是实验室中通过向熔融的单质硫中通入少量氯气制取S2Cl2的装置(部分夹持、加热装置已略去)。
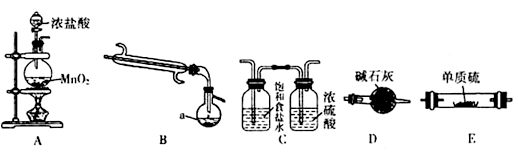
(1)B装置中仪器a的名称___________。
(2)装置的连接顺序是(每个装置只能使用一次)________________________________。
(3)装置D的作用是_________。
(4)实验开始时先点燃_______酒精灯再点燃 _______处酒精灯。
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是_________,该操作的温度范围是___________。
(6)请设计实验证明所得产品中是否含有杂质SCl2_____________________。
-
(15 分) S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:
① CS2+3Cl2 ℃CCl4+S2Cl2;② 2S+Cl2
℃CCl4+S2Cl2;② 2S+Cl2 ℃S2Cl2。
℃S2Cl2。
已知:S2Cl2易与水反应,S2Cl2+Cl2 2SCl2。
2SCl2。
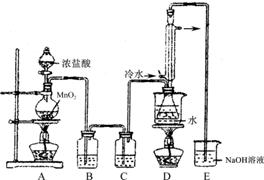
下列是几种物质的熔沸点和反应装置图
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(1)利用上图装置(部分夹持仪器已略去)来制备S2Cl2,反应原理是________(填写以上两种反应原理的数字序号)
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是________。
(3)D装置中冷凝管的作用是________;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是________。
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为________。
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和________。
(6)上图尾部装置不够完善,存在的问题是________。


 已知在S2Cl2中硫元素显+1价,电子式:
已知在S2Cl2中硫元素显+1价,电子式: ,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生歧化反应 (一部分硫元素价态升高,一部分降低)。反应涉及的几种物质的熔沸点如下:


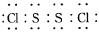 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低),反应涉及的几种物质的熔沸点如表:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低),反应涉及的几种物质的熔沸点如表:

 S2Cl2。
S2Cl2。



