-
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4︰1,其d轨道中的电子数与最外层电子数之比为5︰1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子
式分别是________、________;杂化轨道分别是________、________;a分子的
立体结构是________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________晶体、
________晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)________。
(4)Y与Z比较,电负性较大的是。
(5)W的元素符号是________,其+2价离子的核外电子排布式是________。
高三化学填空题中等难度题查看答案及解析
-
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数这比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_________、_________;杂化轨道分别是__________、_________;a分子的立体结构是___________。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________晶体,_________晶体。
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________。
(4)Y与Z比较,电负性较大的_________,
(5)W元素的化学式__________,其+2价离子的核外电子排布式是___________。
高三化学填空题困难题查看答案及解析
-
【化学——选修5:有机化学基础】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
元素
第一电离能
第二电离能
第三电离能
W
495.8
4562
6910.3
(1)U原子电子排布式为_______________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为_______,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为_______;
(3)W的氯化物和Mg的氯化物中,熔点较高的是________(填化学式),原因是_______。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式______。
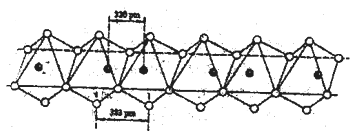
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。则该化合物中Nb和I的原子个数比为______。
高三化学推断题困难题查看答案及解析
-
X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57。Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数比为2:1,其d轨道处于全充满状态。
(1)U原子的电子排布式为______________。
(2)Y和W电负性,较小的是______ (填元素符号);Y和Z的第一电离能,较大的是______(填元素符号)。
(3)X与Z形成最简单化合物Q时,Z原子采取的杂化轨道类型为_______,Q分子空间构型为_________;请写出U2+与Q形成配离子的离子反应方程式:_______________。
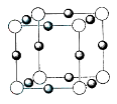
(4)U+与Z3+形成的晶胞结构如图所示,阴、阳离子间核间距为a cm与同―个Z3+相连的U+有_____个,该晶体的密度为______g • cm-3(NA 表示阿伏加德罗常数)。
高三化学填空题中等难度题查看答案及解析
-
X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57。Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)U2+的外围电子排布式为 。
(2)X、Y、Z 可以形成化学式为XYZ的分子。该分子中各原子均达到稀有气体稳定结构,则该分子中Y采取的杂化轨道类型为
(3)比较Y和W的第一电离能,较大的是 (填元素符号),
(4)X与Z形成的最简单化合物Q的分子构型为 ;U2+与Q形成的配离子的离子反应方程式为 。
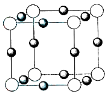
(5)U+与Z3-形成的晶胞结构如图所示,阴、阳离子间的核间距为a cm。与同一个Z3-相连的U+有 个,该晶体的密度为 g·cm-3。(设NA表示阿伏加德罗常数)
高三化学填空题困难题查看答案及解析
-
X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57。Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数比为2:1,其d轨道处于全充满状态。
(1)U原子的电子排布式为______________。
(2)Y和W电负性,较小的是______(填元素符号);Y和Z的第一电离能,较大的是______(填元素符号)。
(3)X与Z形成最简单化合物Q时,Z原子采取的杂化轨道类型为_______,Q分子空间构型为_________;请写出U2+与Q形成配离子的离子反应方程式:_______________。
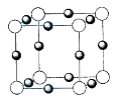
(4)U+与Z3+形成的晶胞结构如图所示,阴、阳离子间核间距为a cm与同―个Z3+相连的U+有_____个,该晶体的密度为______g • cm-3(NA 表示阿伏加德罗常数)。
高三化学填空题中等难度题查看答案及解析
-
【化学——选修3 物质结构与性质】(15分)A,B,C,D,E五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57;B原子的L层P轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同,E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)B,D可分别与A形成只含一个中心原子的共价化合物X和Y,其中X的电子式为 ;Y采取的杂化轨道类型为 ;C与A形成的常见化合物的分子构型为 。
(2)B和D的最高价氧化物的晶体中熔点较高的是(填化学式) ,其原因 。
(3)B与C比较电负性较大的是 (填元素符号),E2+的核外电子排布式为 。
(4)E2+与C的常见氢化物形成的配离子的离子反应方程式为 。
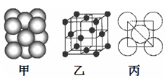
(5)铝单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。若已知铝原子半径为d,NA表示阿伏加德罗常数,摩尔质量为M,则该原子的配位数 ,该晶体的密度可表示为______________,据下图计算,Al原子采取的面心立方堆积的空间利用率为 __________。
高三化学填空题极难题查看答案及解析
-
A,B,C,D,E五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57;B原子的L层P轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同,E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)B,D可分别与A形成只含一个中心原子的共价化合物X和Y,其中X的电子式为________;Y采取的杂化轨道类型为________;C与A形成的常见化合物的分子构型为________。
(2)B和D的最高价氧化物的晶体中熔点较高的是(填化学式)________,其原因________。
(3)B与C比较电负性较大的是________(填元素符号),E2+的核外电子排布式为________。
(4)E2+与C的常见氢化物形成的配离子的离子反应方程式为________。
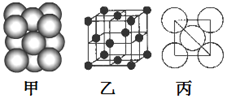
(5)铝单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。若已知铝原子半径为d,NA表示阿伏加德罗常数,摩尔质量为M,则该原子的配位数________,该晶体的密度可表示为______________,据下图计算,Al原子采取的面心立方堆积的空间利用率为 __________。
高三化学填空题困难题查看答案及解析
-
【化学—选修3:物质结构与性质】(15分)已知位于元素周期表前四周期的六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同。请回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序是____________(填元素符号)
(2)化合物BD3的分子空间构型可描述为_________,B的原子轨道杂化类型为_______。
(3)已知F元素在人体内含量偏低时,会影响O2在体内的正常运输。已知F2+与KCN溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物。则F的基态原子价电子排布式为________________。CN-与___________(一种分子)互为等电子体,则1个CN-中π键数目为___________。
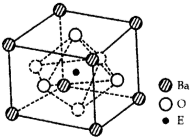
(4)EO2与碳酸钡在熔融状态下反应,所得晶体的晶胞结构如图所示,则该反应的化学方程式为__________
在该晶体中,E4+的氧配为数为___________。若该晶胞边长为a nm可计算该晶体的密度为__________g/cm3(阿伏加德罗常数为NA)
高三化学填空题困难题查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,且位于三个不同周期,X与W同主族,W元素金属性在短周期中最强,Z原子最外层电子数是其内层电子总数的3倍,Z原子的核电荷数等于X、Y原子核电荷数之和。下列说法正确的是
A.原子半径:r(W)>r(Z)>r(Y)>r(X)
B.元素Y的简单气态氢化物的热稳定性比Z的强
C.仅由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性也可能呈酸性
D.化合物X2Z2与W2Z2所含化学键类型完全相同
高三化学单选题中等难度题查看答案及解析