-
在一定温度、压强下,1体积X2(气)和3体积Y2(气)化合生成2体积的气体化合物,则该气体化合物的化学式为( )
A.XY3 B.XY C.X3Y D.X2Y3
高三化学单选题中等难度题查看答案及解析
-
在一定的温度和压强下,1体积X2(气)跟3体积Y2(气)化合生成2体积化合物(气),则该化合物的化学式是( )。
A.XY3 B.XY C.X3Y D.X2Y3
高三化学选择题简单题查看答案及解析
-
(1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是 。
(2)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断A可能是 ,B可能是 。
(3)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是 L,质量是 g。
高三化学填空题中等难度题查看答案及解析
-
(1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是 。
(2)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断A可能是 ,B可能是 。
(3)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是 L,质量是 g。
高三化学选择题中等难度题查看答案及解析
-
(1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是________。
(2)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为________。若其中CO和N2的物质的量之比为1∶1,则混合气体中氧元素的质量分数为________。
(3)相同条件下,某Cl2与O2混合气体100 mL恰好与150 mL H2化合生成HCl和H2O,则混合气体中Cl2与O2的体积比为________,混合气体的平均相对分子质量为________。
(4)现有m g某气体,它的摩尔质量为M g·mol-1,则
①该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为________。
②该气体溶于水后形成V L溶液,其溶液的物质的量浓度为______ mol·L-1。
高三化学填空题中等难度题查看答案及解析
-
在一定温度和压强下,2L气体XY2与1L气体Y2化合,生成2L气体化合物,则该化合物的化学式为 ( )
A.X3Y B.X3Y2 C.X2Y3 D.XY3
高三化学选择题简单题查看答案及解析
-
同温同压下,同体积的气体单质X2和气体单质Y2化合生成Z,其体积不变,则Z的化学式为( )
A.X2Y2
B.X2Y
C.XY2
D.XY高三化学选择题中等难度题查看答案及解析
-
(9分)运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)氮是地球上含量丰富的元素,氮及其化合物在工农业生产、生活中有着重要作用。
①下图是一定的温度和压强下是N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:。(△H的数值用含字母a、b的代数式表示)
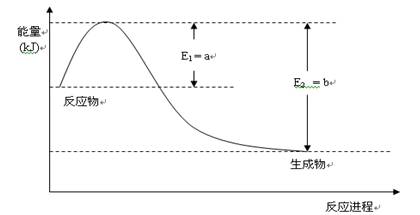
②氨气溶于水得到氨水。在25°C下,将m mol·L-1的氨水与n mol·L-1的盐酸等体积混合,反应后的溶液呈中性,则c(NH+4)________c(Cl-)(填“>”、“<”或“=”);用含m和n的代数式表示出混合液中氨水的电离平衡常数表达式________。
(2)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。
25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1硝酸银溶液,有白色沉淀生成。从沉淀溶解平衡的角度解释产生沉淀的原因是________,向反应后的浊液中,继续加入适量0.1mol·L-1的NaI溶液,振荡、静置,看到的现象是________,产生该现象的原因是(用离子方程式表示)________。
(已知25°C时
)
高三化学填空题简单题查看答案及解析
-
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义。
(1)如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式____________(△H的数值用含字母
Q1、Q2的代数式表示):
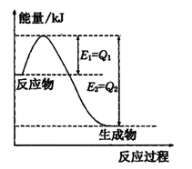
(2)已知:25℃时KSP(AgCl)=1.6×l0-10KSP(AgI)=1.5×l0-16
海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合态存在。在25℃下,向0.1L0.002mol·L-l的NaCl溶液中逐滴加入适量的0.1L0.002mol·L-l硝酸银溶液,有白色沉淀生成,从难溶电解质的溶解平衡角度解释产生沉淀的原因是 ,向反应后的浑浊液中继续加入0.1L0.002mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示)
。
(3)氨气溶于水得到氨水。在25℃下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合(混合后体积为混合前体积之和),反应后溶液显中性。求25℃下该混合溶液中氨水的电离平衡常数。
高三化学填空题中等难度题查看答案及解析
-
根据下列有关天然气的研究和应用回答问题:
(l)在一定温度和压强下,由最稳定单质生成lmol化合物的焓变称为该物质的摩尔生成焓。根据此定义,稳定单质的摩尔生成焓为0,某些化合物的摩尔生成焓如下表所示:
化合物
CO2
CH4
CO
摩尔生成焓(kJ·mol-1)
-395
-74.9
-110.4
CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为______________________
(2)若上述反应分Ⅰ、Ⅱ两步进行,其能量曲线如图所示。则总反应的反应速率取决于反应_______(填“I”或“Ⅱ”)。
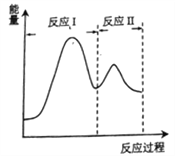
(3)一定温度下反应:CO2(g)+CH4(g)
2CO(g)+2H2(g)的平衡常数表达式Kp= __________(用平衡分压p代替平衡浓度表示)
(4)在压强为p1、p2、p3的三个恒压密闭容器中分别通入1.0molCH4(g)与1.0mol CO2(g ), 发生反应:CO2(g)+CH4(g)
2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图所示。
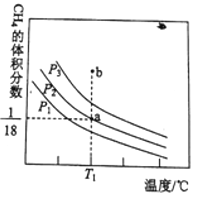
① a点时CH 4的转化率为___________________________
② 压强p 1、p 2、p 3由大到小的顺序为________________,判断理由是______________________。温度为T l℃、压强为P 3时,b点处v(正) ________v(逆)(填“<”、“>”或“="”)
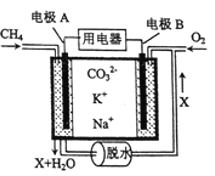
(5)某种燃料电池以熔融碳酸钠、碳酸钾为电解质,其工作原理如图所示,该电池负极的电极反应式为_____________________________________________.若电极B附近通入1m 3空气(假设空气中O 2的体积分数为20% )并完全反应,理论上可消耗相同条件下CH 4的体积为_______m3
高三化学综合题困难题查看答案及解析