-
利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品—3PbO·PbSO4·H2O (三盐),主要制备流程如下:
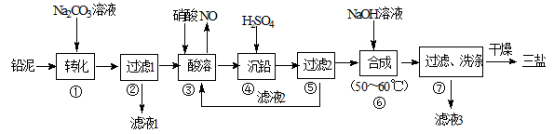
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 。
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为 (写化学式)。
(3)步骤③酸溶时,其中的铅与硝酸生成 Pb(NO3)2 及NO的离子方程式为 ;滤液2中溶质主要成分为 (写化学式)。
(4)步骤⑥合成三盐的化学方程式为 。
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是 。
-
利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbO•PbSO4•H2O (三盐),主要制备流程如下:

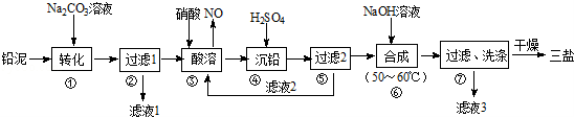
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为______________.
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为______________(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为______________;滤液2中溶质主要成分为______________(写化学式).
(4)步骤⑥合成三盐的化学方程式为______________.
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是______________.
-
利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品—3PbO·PbSO4·H2O (三盐),主要制备流程如下:
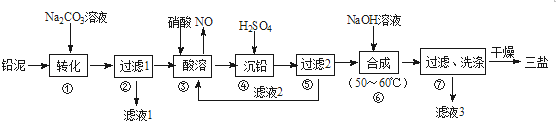
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为______________。
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为_________(写化学式)。
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2 及NO的离子方程式为_______;滤液2中溶质主要成分为________(写化学式)。
(4)步骤⑥合成三盐的化学方程式为___________。
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是_________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。
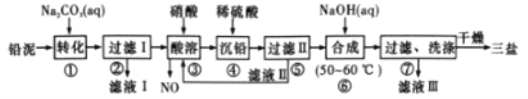
请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。
(2)将滤液Ⅰ、滤液Ⅲ合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为______________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液Ⅱ中溶质的主要成分为______(填化学式)。
(4)步骤⑥合成三盐的化学方程式为______________________。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是__________________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。
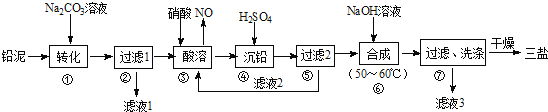
请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为__________。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为__________。
(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为______________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液2中溶质的主要成分为______(填化学式)。
(4)步骤⑥合成三盐的化学方程式为______________________。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是__________________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)制备精细化工产品PbSO4·3PbO·H2O(三盐)的主要流程如下:
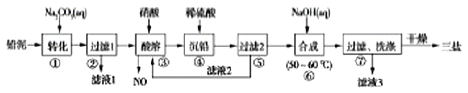
已知:常温下,Ksp(PbSO4)≈1.0×10-8,Ksp(PbSO4)≈1.0×10-13
回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是:Pb+PbO+2H2SO4 2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为__________。若铅蓄电池放电前,正、负极质量相等,放若电时转移了lmol电子,则理论上两电极质量之差为_____________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为__________。若铅蓄电池放电前,正、负极质量相等,放若电时转移了lmol电子,则理论上两电极质量之差为_____________。
(2)将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为________________;滤液2中溶质的主要成分为_____________(写化学式)。
(4)步骤⑥合成三盐的化学方程式为______________。
(5)步骤⑦洗涤的操作是________________________________。
(6)在步骤①的转化中,若硫酸铅和碳酸铅在浊液中共存,则 =________。
=________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)制备精细化工产品PbSO4·3PbO·H2O(三盐)的主要流程如下:
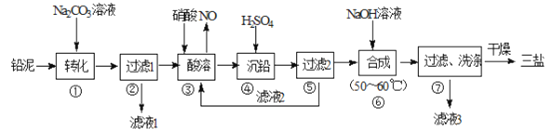
已知:常温下,Ksp(PbSO4)=2.0×10-8 Ksp(PbCO3)=1.0×10-13 ,请回答以下问题:
(1)铅蓄电池工作原理是PbO2+Pb+2H2SO4 2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
2PbSO4+2H2O,在放电过程中负极的质量__________;电解质溶液的pH___________(用“变大”、“不变”或“变小”填写)。该铅蓄电池放电过程中的正极反应式为__________________________________________。
(2)步骤③的目的是使铅泥中的Pb溶解,其对应的离子方程式为________________ 。滤液2中的溶质主要是_____________(填化学式),过滤操作中使用到的玻璃仪器有_____。
(3)步骤⑥合成三盐的化学方程式为________________________。
(4)步骤⑦洗涤产品的方法是________________________________。
(5)在“转化”过程中,若PbSO4和PbCO3在悬浊液中共存,则c(SO42-):c(CO32-)=____________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4· H 2O(三盐),主要制备流程如下。
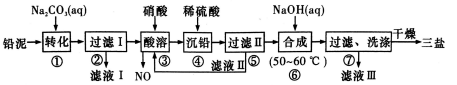
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4  2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
(2)将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为______________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为_____________;滤液II中溶质的主要成分为________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为____________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是____________。
-
用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4· H 2O(三盐),主要制备流程如下。
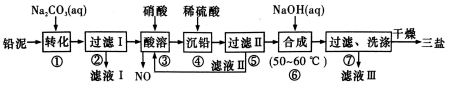
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4  2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
2PbSO4+2H2O。铅蓄电池在充电时,阳极的电极反应式为_________。若铅蓄电池放电前正、负极质量相等,放电时转移了lmol电子,则理论上两极质量之差为___________。
(2)将滤液I、滤液III合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物( Mr=322) ,其化学式为______________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO的离子方程式为_____________;滤液II中溶质的主要成分为________(填化学式)。
(4)步骤⑥合成三盐的化学方程式为____________ 。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是____________。
-
铅蓄电池的阴、阳极填充物又被称为铅膏(主要含PbO、PbO2、PbSO4)是废旧铅蓄电池需要回收的部分,通过回收铅膏可制备聚氯乙烯塑料的热稳定剂三盐基硫酸铅(组成可表示为3PbO·PbSO4·H2O),其工艺流程如下:
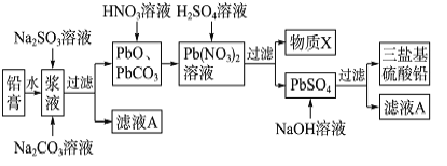
已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。
请回答下列问题:
(1)加入Na2CO3 溶液的目的是______________________________________;浆液中PbO2 转化为PbCO3 的离子方程式是_____________________________________。
(2)从滤液A可提取出一种含结晶水的钠盐副产品,若测定该晶体中结晶水的含量,所需的仪器有:三脚架、托盘天平、瓷坩埚、干燥器 、 酒精灯,还需要的仪器有(填序号)
____________。
A .坩埚钳 B .泥三角 C .烧杯 D .蒸发皿
(3)物质X 是一种可以循环利用的物质,该物质是_______,若其中残留SO42-过多,循环利用时可能出现的问题是__________________________。
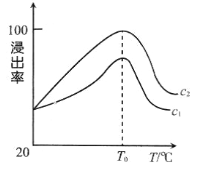
(4)硝酸溶解时,“酸溶”的效率与温度、硝酸的浓度关系如图所示。浓度:c1____________ c2(填“大于”“小于”或“等于”)。温度高于T0 时,浸出率降低最有可能原因是___________________ 。
(5)若铅膏的质量为78g,假设浆液中PbO2 和PbSO4 全部转化为PbCO3,且PbO 未发生反应;硝酸溶解时共收集到5.6 L CO2(标准状况),最后获得90.9g PbSO4,则铅膏中PbO 的质量分数为_________________%(假设流程中原料无损失,小数点后保留一位数字)。




 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。





