-
(18分)
(Ⅰ)某钠盐溶液中通入足量氨气,无明显现象。再在所得溶液中通入过量CO2,产生大量白色沉淀。
(1)写出氨气的电子式 。
(2)该钠盐溶液中一定不可能含有下列哪种微粒 (填编号)。
A.Cl- B.Fe2+ C.SiO32- D.AlO2-
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式 。
(Ⅱ)电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放。某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下:
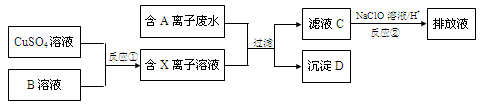
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,生成的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
(4)沉淀D的化学式是 。
(5)写出沉淀D在氧气中灼烧发生的化学方程式 。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理 。
(7)反应①为制得某种元素的低价X离子,试从氧化还原反应的角度分析,是否可以用Na2SO3溶液来代替B溶液 ,
并设计实验证明所用Na2SO3溶液是否变质 。
-
Ⅰ.某钠盐溶液中通入足量氨气,无明显现象.再在所得溶液中通入过量CO2,产生大量白色沉淀。
(1)写出氨气的电子式 。
(2)该钠盐溶液中一定不可能含有下列哪种微粒 (填编号)。
A.Cl﹣ B.Fe2+ C.SiO32﹣ D.AlO2﹣
(3)写出一个通入过量CO2时生成白色沉淀的离子方程式 。
Ⅱ.电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放.某种高浓度有毒的含A离子(阴离子)废水在排放前的处理过程如下:
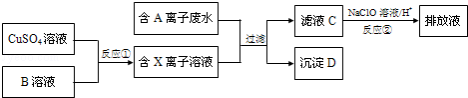
已知:9.0g沉淀D在氧气中灼烧后,产生8.0g黑色固体,反应后的气体通过足量澄清石灰水时,产生10.0g白色沉淀,最后得到的混合气体除去氧气后,还剩余标况下密度为1.25g/L的气体1.12L。
(4)沉淀D的化学式是 。
(5)写出沉淀D在氧气中灼烧发生的化学方程式 。
(6)滤液C中还含有微量的A离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理 。
(7)反应①为制得某种元素的低价X离子,从氧化还原反应的角度分析, (填“能”或“不能”用Na2SO3溶液来代替B溶液,原因是 。
(8)设计实验证明所用Na2SO3溶液是否变质 。
-
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。淀粉KI溶液中通入SO2气体,溶液无明显变化。则下列分析中正确的是
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液时,转移2mol e- 时生成1mol白色沉淀
C.通入SO2时,SO2与I—反应,I—作还原剂
D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
-
(18 分)(Ⅰ) 将某红棕色气体 A 通入到稀钠盐溶液甲中,有白色沉淀产生;当红棕色气体通入过量时,白色沉淀逐渐完全消失。上述过程中还产生一种无色气体B,B 遇空气后又可产生 A。则:
(1)写出钠离子的结构示意图 ; B 与空气反应的化学方程式 。
(2)甲中肯定不含有下列物质中的 ;(填选项字母)。
A.Na2S B.NaAlO2 C.Na2SiO3 D.NaCl
(3)通入气体 A 使白色沉淀逐渐消失且产生气体 B,该反应的离子方程式是 。
(Ⅱ)某研究小组为了探究一种无机化合物X(化合物 X 中带有 6 个结晶水,仅含五种元素,且每种元素在该化合物中均只有单一价态,X 的式量为400)的组成和性质,设计了如下实验: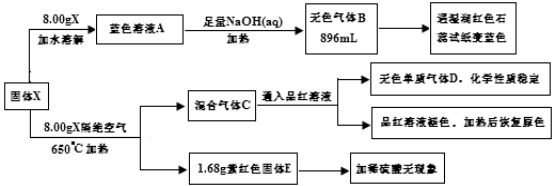
(注明:以上气体体积均在标准状况下测定,产物中只有水未标出)
(1)写出气体B 的电子式 ,气体 D 的结构式 。
(2)混合气体 C 通入品红溶液褪色,加热后恢复原色的原因是 。
(3)8.00 固体 X 所含阴离子的物质的量是 mol。
(4)固体X 受热分解的化学方程式是 。
-
下列叙述不正确的是( )
A.向澄清石灰水中通入CO2产生白色沉淀,再通入过量CO2,沉淀消失
B.向AlCl3溶液中滴加NaOH溶液,产生白色沉淀,再加入过量NaOH溶液,沉淀消失
C.向AgNO3溶液中滴加氨水,产生白色沉淀,再加入过量氨水,沉淀消失
D.向Na2SiO3溶液中滴加盐酸,产生白色沉淀,再加入过量盐酸,沉淀消失
-
向某盐溶液中通入过量Cl2无明显现象,滴加Ba(NO3)2溶液和稀HNO3后,有白色沉淀生成,则原溶液可能是( )
A.AgNO3溶液 B.CaCl2溶液 C.Na2SO3溶液 D.Na2CO3溶液
-
下列说法中正确的是( )
A.向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象
B.将8gSO3放入92g水中,所得溶液溶质质量分数为8%
C.已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol.将4g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出了5.73kJ的热量
D.向100ml1mol/L的Ca(HCO3)2溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱
-
下列有关实验操作,现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将过量CO2通入CaCl2溶液中 | 无白色沉淀 | 生成Ca(HCO3)2溶于水 |
| B | 常温下将Al片插入浓硫酸中 | 无明显现象 | Al片和浓硫酸不反应 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| D | 将SO2通入溴水中 | 溶液褪色 | SO2具有漂白性 |
-
下列有关实验原理,方法和结论都正确的是( )
A.某钠盐溶液中加入硝酸无明显现象,再加入氯化钡溶液有白色沉淀,该钠盐一定是硫酸钠
B.在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
C.新制氯水中加入碳酸钙粉末搅拌,过滤、滤液中c(HClO)将增大
D.相同质量的两份锌粒分别加入足量稀硫酸,在一份中加入少量CuSO4•5H2O,其反应速率将加快,且最终产生的H2与另一份相同
-
下列溶液中通入足量SO2,根据其实验现象,所得结论不正确的是
| 溶液 | 现象 | 结论 |
| A | 含HCl、BaCl2和FeCl3的溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫红色溶液褪色 | SO2有漂白性 |
| D | 加有酚酞的NaOH溶液 | 褪色 | SO2是酸性氧化物 |
A. A B. B C. C D. D


