-
金属钛性能优越,被称为继铁、铝之后的“第三金属”,工业上用钛矿石(主要成分:FeO、TiO2,SiO2等)为原料制取钛,工艺流程如下,回答下列问题:
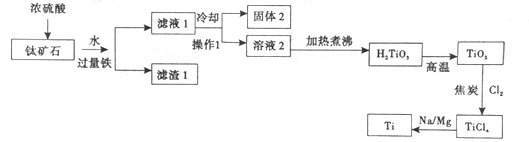
已知:TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是__________。
(2)操作1名称为_______,固体2的主要成分是______, 写出金属钠与TiCl4共热的化学反应方程式_________________。
(3)一定温度下,在一个固定容积的容器中发生反应:TiO2(s)+2Cl2(g)+2C(s) TiCl4(g)+2CO(g),反应中氧化剂是________,下列说法能够说明该反应已达化学平衡状态的是_________________。
TiCl4(g)+2CO(g),反应中氧化剂是________,下列说法能够说明该反应已达化学平衡状态的是_________________。
A.反应每断裂2个Cl一Cl键,同时生成2 个C O键
O键
B. 容器内压强不再发生变化
C. Cl2和TiCl4的浓度不再变化
D.v(TiCl4)正=2v(C)逆
(4)将50吨钛矿石经上述变化后,最终可得金属钛12吨,假设各步反应均完全,则原矿石中TiO2的百分含量为_____________。
-
(16分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:
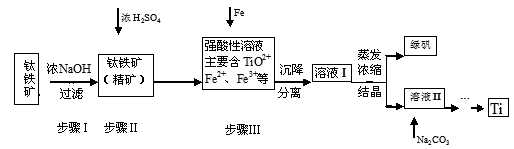
已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29

①步骤Ⅲ加入铁屑原因是 。
②TiO2+水解的离子方程式为 。向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH接近 时,TiO(OH)2已沉淀完全。
(3) 反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
| TiCl4 | Mg | MgCl2 | Ti |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
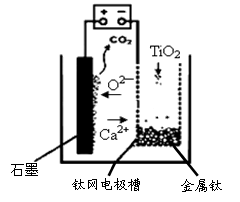
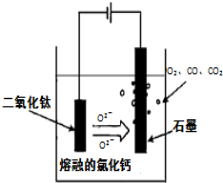
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。写出阳极上所发生的反应式: 。
-
(14分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:
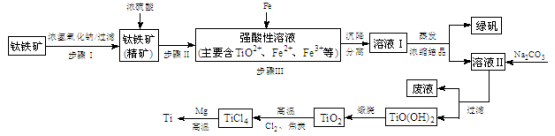
已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度与pH关系如图,

TiO(OH)2溶度积Ksp=1×10-29
①步骤Ⅲ加入铁屑原因 是 。
② TiO2+水解的离子方程式为 。
向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH= 时,TiO(OH)2已沉淀完全。
(3)TiCl4→Ti反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
| TiCl4 | Mg | MgCl2 | Ti |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(4)电解TiO2制备钛的方法如图所示。该方法由于具备生产过程简化、生产成本低、产品质量高、环境友好等诸多优点而引人注目。已知TiO2熔融状态下不发生电离,电解时阴极反应式为 。
-
金属钛在航天、潜海和医疗方面应用广泛。工业上用钛铁矿(主要成分为钛酸亚铁FeTiO3,含FeO、Fe2O3、SiO2)为原料制TiO2,再由TiO2制得金属Ti
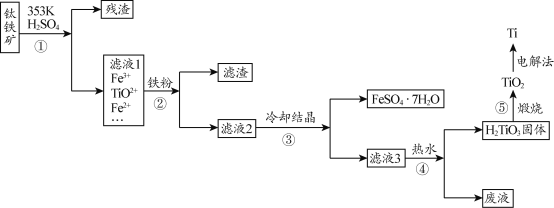
资料:TiO2+会发生水解
(1)步骤②、③、④中,均需用到的操作是_______。(填操作名称)
(2)检验滤液2中是否含Fe3+的方法是:_______。
(3)步骤1中FeTiO3溶于过量硫酸的化学方程式___________。

(4)请结合化学用语解释步骤④中加热水的原因___________。
(5)电解法获得Ti是通过图装置,以熔融CaCl2做电解质
①a为电源的_____(填“正”或“负”)
②在制备钛的过程中石墨电极附近的气泡中除了O2、CO、CO2外还可能有的气体是______________,用化学用语解释原因________________。
(6)测定废液中Fe2+浓度已确认铁元素的回收率:取25.00ml废液于锥形瓶中,用硫酸酸化的xmol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积如图所示:
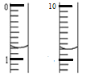
(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O).废液中c(Fe2+)=_________
-
(11分)钛是一种重要的金属,工业上用钛铁矿(主要成分为FeTiO3 ,含FeO、Al2O3、SiO2 等杂质)为原料制钛白粉(TIO2 ) , TiO2常通过两种方法可制得 Ti。
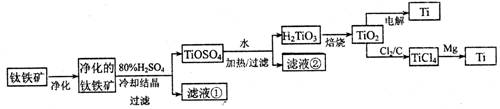
其中, 2H2SO4+ FeTiO3 = TiOSO4+ FeSO4+ 2H2O 。回答下列问题。
(l)净化钛矿石时,需用浓氢氧化钠溶液来处理,该过程中发生反应的化学方程式有:
SiO2+2NaOH =Na2SiO3 + H2O 和________
(2)滤液①中的溶质主要是 FeSO4,检验其中Fe2+的方法是:________.
(3)从 TiOSO4→H2TiO3需要加热,则加热的目的是:________。
(4)电解 TiO2来获得 Ti 是以 TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。其阴极反应的电极反应式为:________.
(5)从化学平衡的角度解释:往TiO2和Cl2反应体系中加人焦炭后,能使反应 TIO2(s) + 2C12 (g) TICl4(l) +O2 (g)顺利进行的原因是:________
TICl4(l) +O2 (g)顺利进行的原因是:________
-
金属钛被称为“21世纪金属”
(1)工业上用钛矿石(含FeTiO3,含FeO、Al2O3、SiO2等杂质)经过以下流程制得TiO2:
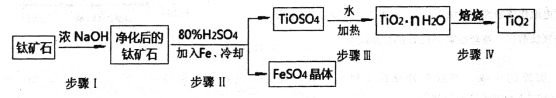
其中,步骤Ⅱ发生反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H20
①步骤I反生的化学方程式是______________________________若将所得FeSO4晶体溶于水,加热蒸干后所得的固体是_________________
②若步骤Ⅲ中是利用Ti4+在溶液中水解制得TiO2·nH2O,则该反应的离子方程式为_________________________________________________
(2)可利用TiO2通过下述两种方法制备金属钛:
方法一:将TiO2作阴极,石墨作阳极,熔融CaO为电解液,用炭块作电解槽池,电解TiO2制得钛,其阴极发生的反应:______________________________________。
方法二:通过以下反应制备金属钛
①TiO2(s)+2Cl2(g)  TiCl4(g)+O2(g) △H=+151 KJ/mol
TiCl4(g)+O2(g) △H=+151 KJ/mol
②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
在实际生产中,需在反应①过程中加入碳才能顺利制得TiCl4,其原因是_________________________,______________________________________________。(两方面)
(3)若已知:C(s)+O2(g)=CO2(g) △H=-394 KJ/mol,则由固体TiO2、固体C与Cl2反应制取气态TiCl4的热化学方程式为______________________________________________。
-
(1)工业上用钛矿石(主要成分为FeTiO3,主要含FeO、Al2O3、SiO2等杂质)经过以下流程制得TiO2:
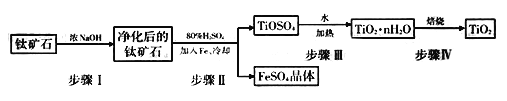
其中,步骤II发生的主要反应为:2H2SO4+ FeTiO3=TiOSO4+FeSO4+2H2O
①步骤I发生反应的离了方程式是:_____________、___________。为提高钛矿石的碱浸出速率,步骤I可采取的办法除提高碱的浓度外,还可以采取的办法有_________________、__________________________(写出两种方法)。
②步骤II中加入Fe的目的是___________________;分离出FeSO4晶体的操作是___________。
③步骤III形成的TiO2·nH2O 为胶体,其反应的化学方程式为____________________。
(2)可利用TiO2通过下述两种方法制备金属钛:
方法一: 将TiO2作阴极,石墨作阳极,熔融CaO为电解液,碳块作电解槽池,电解TiO2制得钛,阳极上一定生成的气体是____________,可能生成的气体是__________________。
方法二: 通过以下反应制备金属钛
①TiO2 (s)+2Cl2(g) TiCl4(g)+O2(g) △H=+ 151kJ/mol
TiCl4(g)+O2(g) △H=+ 151kJ/mol
②TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
实际生产中,需在反应①过程中加入碳,可以顺利制得TiCl4。碳的作用除燃烧放热外,还具有的作用是_______________________________________。
-
金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石(TiO2)为原料制取Ti的反应为:
aTiO2+bCl2+Cc=====aTiCl4+cCO ………………反应(1)
TiCl4+2Mg===========Ti+2MgCl2 ………………反应(2)
关于反应(1)、(2)的分析正确的是 ( )
A.TiCl4在反应(1)中是氧化产物,在反应(2)中是氧化剂
B.C、Mg在反应中均为还原剂,被氧化
C.在(1)反应方程式中,a一定等于2
D.每生成9.6gTi,反应(1)、(2)中共转移电子均为0.6mol
-
(15分)金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航海、化工、医疗上不可缺少的材料。
I、工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:

其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:_________(填“需要”或“不需要”)
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的离子方程式________。
II、为了提高资源的利用率,减少环境污染,可将氯碱厂、炼钛厂和甲醇厂组成产业链,其关系如下图所示。
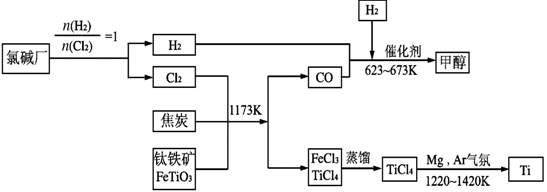
(3)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________________________。
(4)已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=一641 kJ·mol-1
②1/2Ti(s)+Cl2(g)=1/2TiCl4(l);△H=一385 kJ·mol-1
则Mg 与TiCl4反应的热化学方程式为________,
该反应在氩气氛中进行的理由是________。
(5)在上述产业链中,合成192 t 甲醇理论上需额外补充H2t (不考虑生产过程中物质的任何损失)。
-
二氧化钛(TiO2)广泛用于制造高级白色油漆,也是许多反应的催化剂.工业上用钛铁矿[主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质]作原料,制取二氧化钛及绿矾,其生产流程如下:
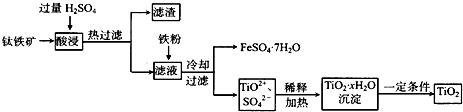
回答下列问题:
(1)Ti原子序数为22,则Ti位于周期表第________周期,第________列.
(2)FeTiO3溶于过量硫酸的离子方程式________.
(3)流程中生成TiO2•xH2O离子方程式为________.
(4)若铁粉的用量不足,可能导致产品TiO2中混有________杂质.
(5)以TiO2为原料制取金属钛的其中一步反应为TiO2+Cl2+C TiCl4+________,已知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为________.
TiCl4+________,已知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为________.
(6)TiCl4 在常温下呈液态,且极易水解,可以用作军事烟雾剂;写出其水解反应的方程式________.

TiCl4(g)+2CO(g),反应中氧化剂是________,下列说法能够说明该反应已达化学平衡状态的是_________________。
O键














