-
MnO2是重要无机材料,某小组设计了将粗MnO2(含有MnO、 MnCO3和Fe2O3等杂质)样品转化为纯MnO2实验,流程如下:
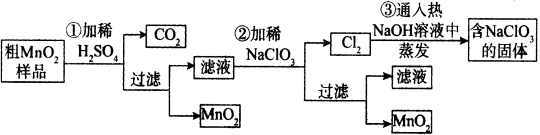
(已知:氧化性强弱顺序: ClO3- > MnO2 > Fe3+)
(1)铝与二氧化锰在高温下发生置换反应,该反应的化学方程式为 。
(2)请配平第②步反应的离子方程式:
Mn2+ + ClO3-+ H2O= MnO2↓+ Cl2↑+ H+
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、 、 ;
第③步蒸发得到的固体中除了含有NaClO3和NaOH外,还一定含有 (写化学式)。
(4)若粗MnO2样品质量为23.0g,标准状况下,第①步反应收集448mLCO2气体,则原样品中MnCO3的质量百分含量为 (MnCO3相对分子质量为115)。
-
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2 (含有较多的MnO 和MnCO3) 样品转化为纯MnO2的实验,其流程如下:
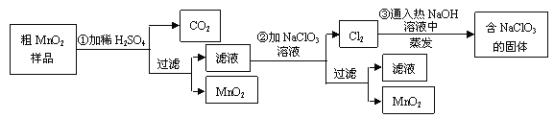
(1)第①步加稀H2SO4时,粗MnO2样品中的________(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式:___________________________________。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、______、______、______,己知蒸发得到的固体中有NaClO3 和NaOH,则一定还有含有________(写化学式)。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224LCO2 (标准状况下),则在第②步反应中至少需要___molNaClO3。
-
以下工业流程制备无机功能材料MnO2,粗MnO2的提纯是工业生产的重要环节,某研究性学习小组设计了将粗MnO2(含有较多MnO和MnCO3)样品转化为纯MnO2实验。

针对上述工业流程,下列选项错误的是( )
A.第①步加稀 时,粗MnO2样品中的MnO、MnCO3转化为可溶性物质
时,粗MnO2样品中的MnO、MnCO3转化为可溶性物质
B.不考虑操作过程中的损失,本流程中的 固体能全部循环,不需额外补充
固体能全部循环,不需额外补充
C.第②步反应的离子方程式
D.实验室模拟上述工业流程中得到MnO2固体的操作必须用到的玻璃仪器有玻璃棒、烧杯、漏斗
-
KMnO4和MnO2都是重要的化学物质,在实验室可以作氧化剂和催化剂。某化学学习小组对两种物质的制备探究如下:
Ⅰ.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2的实验,其工艺流程如下:
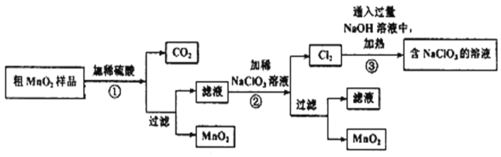
请回答下列问题:
(1)第②步操作中,NaClO3氧化MnSO4的离子方程式为______________
(2)第③步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的________(填序号)。
a.NaCl b.NaClO c.NaOH d.NaClO4
(3)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器有______________。
(4)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为__________。
Ⅱ.KMnO4的制备:
(5)实验室由二氧化锰制备高锰酸钾可分两步进行:
第一步:MnO2与KOH共熔并通入氧气:2MnO2+4KOH+O2=2K2MnO4+2H2O;
第二步:通入CO2,可使K2MnO4发生歧化反应生成KMnO4和MnO2。
第二步完成反应时,转化为KMnO4的K2MnO4占其全部的百分率约为________(精确到0.1%)。
-
某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:
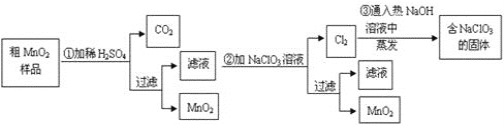
(1)第①步加稀H2SO4时,粗MnO2样品中的____(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式:_________
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯 、______、______,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有____(写物质名称)。
(4)若粗MnO2样品的质量为12.69 g,第①步反应后,过滤得到8.7 g MnO2,并收集到0.224 L CO2(标准状况),则第②步反应中至少需要_______ g NaClO3。
-
氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN + NaOH + H2O=NaAlO2+ NH3↑
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
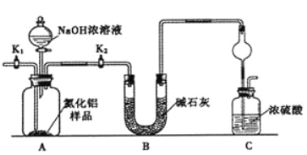
(1)上图C装置中球形干燥管的作用是________________________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置的气密性,再加入实验药品。接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是__。
(3)若去掉装置B,则导致测定结果________(填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见__________________________。
(方案2)按以下步骤测定样品中A1N的纯度:
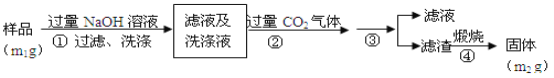
(4)步骤②生成沉淀的离子方程式为_________________________________。
(5)A1N的纯度是___________(用m1、m2表示)。
-
氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
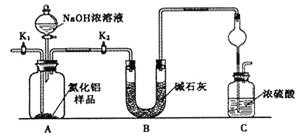
(1)上图装置中,U形管B中所装固体为________,C中球形干燥管的作用是_______________________。
(2)关闭K1打开K2,再打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________________________________。
(3)由于上述装置还存在____________缺陷,导致测定结果偏高。
【方案2】按以下步骤测定样品中AlN的纯度:
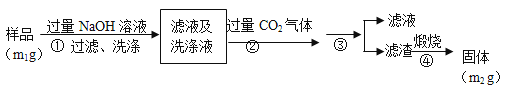
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作中用到的主要玻璃仪器是_________。AlN的纯度是__________(用m1、m2表示)。
-
氮化铝(AlN)是一种新型无机非金属材料,为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是________________________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置的气密性,再加入实验药品。接下来的实验操作是________,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________。
(3)由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_________________。
【方案2】按以下步骤测定样品中A1N的纯度:

(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作是__________。A1N的纯度是___________(用m1、m2表示)。
-
氮化铝(AlN)是一种新型无机非金属材料,为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
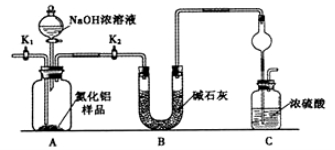
(1)上图C装置中球形干燥管的作用是________________________。
(2)完成以下实验步骤:组装好实验装置,首先检查装置的气密性,再加入实验药品。接下来的实验操作是________,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________。
(3)由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见_________________。
【方案2】按以下步骤测定样品中A1N的纯度:
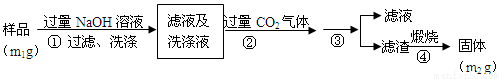
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作是__________。A1N的纯度是___________(用m1、m2表示)。
-
MnCO3可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。实验室模拟以MnO2为原料生产MnCO3的工艺流程如下:

已知:MnCO3难溶于水和乙醇,受热易分解。
(1)实验室中过滤操作所用到的玻璃仪器有漏斗、烧杯、___。
(2)①检验水洗是否合格的方法是___。
(3)MnCO3在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图所示。则300℃时,剩余固体中n(Mn)∶n(O)为___;图中点D对应固体的成分为___(填化学式)。















