-
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提炼Al2O3并制取铝的流程如下:

请回答下列问题:
(1)铝与NaOH溶液反应的离子方程式为。
(2)图中涉及分离溶液与沉淀的玻璃仪器有烧杯、玻璃棒、_________。
(3)反应1涉及的化学方程式有________、________。滤液Ⅰ中加入CaO生成的沉淀是 _________(填化学式)。
(4)向滤液Ⅱ中通入气体A为,生成沉淀B的离子方程式为。
-
(6分)铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝。上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是__________。
A.铝材 B.石墨 C.铅板 D.纯铝
(2)阳极氧化能使金属表面生成致密的氧化膜,装置如下图所示。以稀硫酸为电解液,铝阳极发生的电极反应式为__________________________________。

(3)下列说法正确的是 。
A.阳极氧化是应用原电池原理进行金属材料表面处理的技术
B.铝的阳极氧化可增强铝表面的绝缘性能
C.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D.铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
-
(12分)电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图

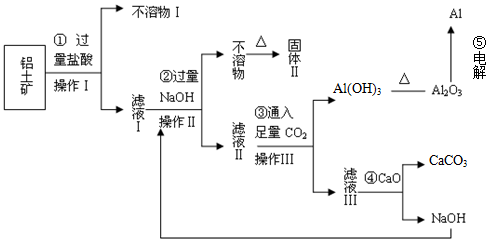
(1)固体Ⅱ的化学式为_________,该固体的颜色为________;
(2)在实际工业生产流程⑤中需加入冰晶石,目的是________;
(3)写出流程③的离子方程式________;
(4)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应________;
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是________;
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(6)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有__________;
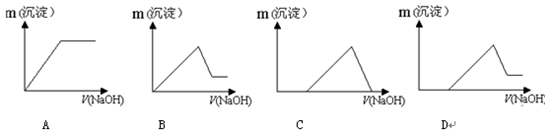
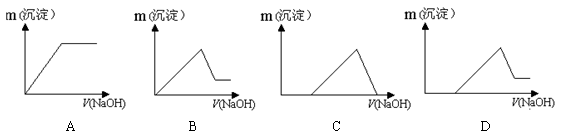
(7)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是 ________

-
(10分)电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图:
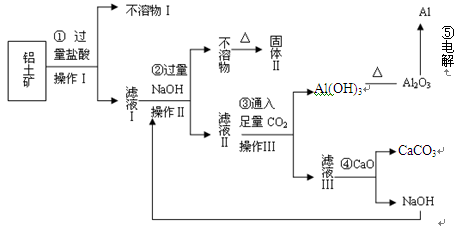


(1)固体Ⅱ的化学式为_ ,该固体的颜色为 ;
(2)写出流程③的离子方程式 ;
(3)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应 ;
(4)从铝土矿中提取铝的过程不涉及的化学反应类型是 ;
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(5)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有_ _;
(6)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是________
-
(12分)电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图

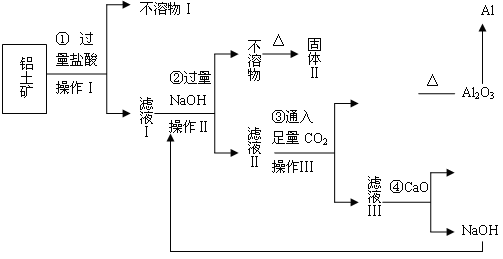
(1)固体Ⅱ的化学式为_▲ ,该固体的颜色为▲ ;
(2)在实际工业生产流程⑤中需加入冰晶石,目的是▲ ;
(3)写出流程③的离子方程式▲ ;
(4)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应▲ ;
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是▲ ;
A.复分解反应 B.氧化还原反应 C.置换反应 D.分解反应
(6)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有_▲ _;
(7)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是
-
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是____。
(2)以铝土矿(主要成分为Al2O3.含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下(已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀)。
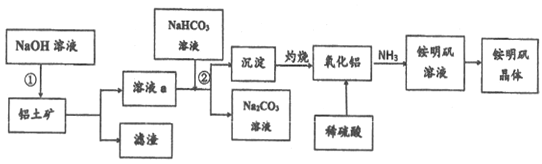
①实验前,要将铝土矿粉粹的目的是_______。
②用氧化物的形式表示铝硅酸钠的化学式________。
③步骤②涉及到的离子方程式是: _______。
④写出利用Al2O3制备金属Al的化学方程式: _______。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1 : 1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______。
-
工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。下图是从铝土矿中提纯Al2O3的简单示意图。其中涉及到的一个反应是:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。

(1)图示中(1)的实验操作是________;图示中(2)加入的试剂__________。
(2)试写出下列物质(或溶液中的溶质)的化学式:
B__________________;C__________________;H________________;F______________。
(3)写出化学方程式:
①_____________________________________。
③_____________________________________。
④_________________________________。
-
下列应用不涉及氧化还原反应的是
A.Na2O2用作呼吸面具的供氧剂
B.实验室用NH4Cl和Ca(OH)2制备氨气
C.工业上利用合成氨实现人工固氮
D.工业上用电解熔融状态的Al2O3制备Al
-
金属材料在日常生活以及生产中有着广泛的应用.下列关于金属的一些说法不正确的是( )
A.金属钠保存在煤油中
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.合金的硬度一般比各成分金属大
D.铜与氯化铁溶液的反应常用于制作印刷电路板
-
下列有关铝及其化合物的叙述正确的是C
A. 铝粉与氧化镁共热可制取金属镁
B. 足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气
C. 工业上用电解熔融Al2O3的方法冶炼铝
D. 由于铝在空气中不会锈蚀,所以铝制品的使用寿命都很长









