-
“铝热剂”能冶炼金属.焊接钢轨等,却没有“镁热剂”,其原因是 ( )
A.Mg与金属氧化物难反应 B.Mg与金属氧化物反应所需温度太高
C.Mg与金属氧化物反应放热少 D.Mg与金属氧化物反应过于剧烈
高三化学选择题简单题查看答案及解析
-
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO·Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是 。
(2)NaOH溶液可以除去铝表面的氧化膜,在处理过程中常会产生H2,产生H2的离子方程式是 。
(3)工业上以铝土矿(Al2O3·H2O)为原料生产铝,主要包括下列过程:
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH)3固体;
iii.使Al(OH)3脱水生成Al2O3;
iv.电解熔融Al2O3生成Al。
铝土矿粉粹的目的是 ,试剂A的化学式是 ,电解熔融Al2O3时,加入冰晶石,其作用是 。
(4)明矾化学式为KAl(SO4)2·12H2O,向明矾溶液中加入Ba(OH)2溶液,当溶液中的SO42-恰好沉淀时,铝元素的存在形式是 。
(5)美国普度大学研究开发出一种利用铝镓(化学式:AlGa)合金制取氢气的新工艺(如下图所示)。

i.写出常温下铝镓合金产生氢气的化学方程式 。
ii.下列有关该工艺的说法正确的是 。
A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金的熔点比金属铝低
D.该工艺可利用太阳能分解水
高三化学填空题困难题查看答案及解析
-
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO-Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是____。
(2)以铝土矿(主要成分为Al2O3.含SiO2和Fe2O3等杂质)为原料生产铝和铵明矾晶体[NH4Al(SO4)2·12H2O]的一种工艺流程如下(已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀)。
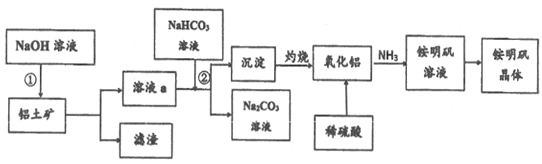
①实验前,要将铝土矿粉粹的目的是_______。
②用氧化物的形式表示铝硅酸钠的化学式________。
③步骤②涉及到的离子方程式是: _______。
④写出利用Al2O3制备金属Al的化学方程式: _______。
⑤若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1 : 1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为_______。
高三化学综合题困难题查看答案及解析
-
铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
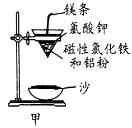
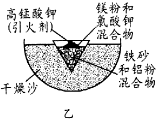

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因,除了可能混有没反应完的磁性氧化铁外,还有一个原因是 。
(2)若证明上述所得“铁块”中含有金属铝,可选择 (填试剂名称),所发生反应的离子方程式为 。
(3)为克服图甲的缺陷改用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。为测定该实验所得 “铁块”的成分,实验流程如图所示。
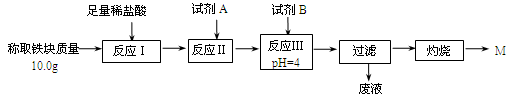
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+
Fe3+
Al3+
Mg2+
开始沉淀时的pH
7.5
2.8
4.2
9.6
沉淀完全时的pH
9.0
4.0
5
11
① 试剂A应选择 ,试剂B应选择 。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水 E.MgCO3固体
② 已知常温下Fe(OH)3的Ksp=1.1×10-36,则反应Ⅲ后溶液中c(Fe3+)= mol·L-1。
③ 灼烧完全的标志是 。
④ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是 。如果对所得过滤固体直接洗涤、烘干、称量,计算“铁块”的纯度,则计算结果会 (填“偏大”“偏小”或“无影响”),原因是 。
高三化学填空题困难题查看答案及解析
-
(10分)铝是一种重要金属:(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:
(2)工业上用铝土矿(主要成分为A12O3,还有少量的Fe2O3 ,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
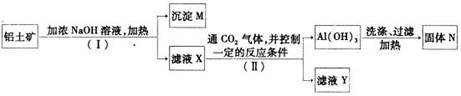
①I和II步骤中分离溶液和沉淀的操作是; ;
②沉淀M中除含有泥沙外,一定还含有 ,固体N是 ;
③滤液X中,含铝元素的溶质的化学式为 ,它属于________(填“酸”、“碱”或“盐”)类物质;
④实验室里常往AlCl3溶液中加入(填“氨水”或“NaOH溶液”)来制取
A1(OH)3。其反应的离子方程式为:___________________________________________。
高三化学填空题简单题查看答案及解析
-
下列说法正确的是
A.SiO2可溶于强碱溶液,不溶于任何酸
B.当光束通过淀粉溶液时,无法观察到丁达尔现象
C.铝热反应可用于焊接钢轨和金属的冶炼
D.漂白粉的有效成分是有强氧化性的氯化钙和次氯酸钙
高三化学选择题中等难度题查看答案及解析
-
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速。完成下列填空:
(1)在特制漏斗中将铝热剂混合均匀后,引发铝热反应的操作是:________ ;
(2)硅与铝同周期。地壳里硅、铝的含量硅________铝(填>,<或=)。SiO2是硅酸盐玻璃(Na2CaSi6O14)主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。钠长石(NaAlSi3O8)的氧化物形式________ ,长石是铝硅酸盐,不同类长石其氧原子的物质的量分数相同。由此可推知钙长石的化学式为________ ;
(3)某铝合金由Al、Si、Cu、Mg组成。①称取100g该铝合金样品,分成等质量的A、B两份。向A份加入足量NaOH溶液,B份加入足量的稀盐酸。②待两份反应物都充分反应之后,称得滤渣质量相差1.60g,收集得到的两份气体的体积相差2240mL(标准状况下)。则样品中Si和Mg的物质的量分别是________和 ________。
高三化学填空题困难题查看答案及解析
-
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速。完成下列填空:
(1)在特制漏斗中将铝热剂混合均匀后,引发铝热反应的操作是:____________。
(2)硅与铝同周期.地壳里硅铝的含量硅____________铝(填>,<或=)。工业上制备金属铝的化学方程式是:____________,工业上制备硅的化学方程式有:
a.SiO2+2C
 Si(粗)+2CO
Si(粗)+2COb.SiO2+3C
 SiC +2CO(副反应)
SiC +2CO(副反应)c.Si(粗)+ 2C12
SiCl4
d.SiC14 + 2H2
Si+4HC1
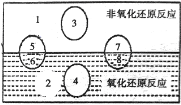
某同学将氧化还原反应、非氧化还原反应及四大基本反应绘制成上图,其中属于上图“2"区域的反应是____________(填序号)。
(3)SiO2是硅酸盐玻璃(Na2CaSi6O14)主要成分,Na2CaSi6O14也可写成Na2O•CaO•6SiO2,钠长石(NaAlSi3O8)的氧化物形式____________,长石是铝硅酸盐,不同类长石其氧原子的物质的量分数相同.由此可推知钙长石的化学式为____________。
(4)某铝合金由Al、Si、Cu、Mg组成。①称取100g该铝合金样品,分成等质量的A、B两份。向A份加入足量NaOH溶液,B份加入足量的稀盐酸。②待两份反应物都充分反应之后,称得滤渣质量相差1.60g,收集得到的两份气体的体积相差2240mL(标准状况下)。则样品中Si和Mg的物质的量分别是n(Si)____________和n(Mg)____________。
高三化学填空题困难题查看答案及解析
-
化学与生产生活密切相关,下列有关说法中不正确的是( )
A.工业上可利用铝热反应冶炼金属或焊接钢轨 B.84 消毒液与洁厕灵混合使用易产生有毒气体
C.为增强洗涤效果可用热的纯碱溶液洗涤餐具上的油污 D.硅胶、六水氯化钙都是常用的食品干燥剂
高三化学单选题中等难度题查看答案及解析
-
化学在生产和日常生活中有着重要的应用。下列说法中不正确的是( )
A.铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀
B.铝热反应不仅被用于焊接钢轨,而且还常被用于冶炼熔点较高的金属
C.电解AlCl3饱和溶液,可制得金属铝
D.Al2O3、MgO的熔点很高,可用于制作耐高温材料
高三化学选择题简单题查看答案及解析