-
关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是( )
A.25 ℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6 mol·L-1
B.向溶液中加入少量CH3COONa固体,溶液中的 值变小
值变小
C.向溶液中加入10 mL 0.1 mol·L-1 HCl,所得溶液中离子浓度大小顺序为c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.向溶液中加入5 mL 0.1 mol·L-1 HCl,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
-
关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是( )
A.25 ℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6mol·L-1
B.向溶液中加入少量CH3COONa固体,溶液中的 值变小
值变小
C.向溶液中加入10 mL 0.1 mol·L-1HCl,所得溶液中离子浓度大小顺序为c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.向溶液中加入5 mL 0.1 mol·L-1HCl,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
-
关于10 mL 0.1 mol·L-1的NH3·H2O溶液,下列说法正确的是
A.25℃时,若溶液的pH=11,则Kb(NH3·H2O)=1×10-6
B.向溶液中加入少量CH3COONa固体,溶液中 的值变小
的值变小
C.向溶液中加入10 mL 0.1 mol·L-1盐酸,所得溶液中离子浓度大小顺序为:c(NH4+)>(Cl-)>c(H+)>c(OH-)
D.向溶液中加入5 mL 0.1 mol·L-1盐酸,所得溶液中离子的浓度一定符合:c(NH4+) + c(H+) = c(Cl-) + c(OH-)
-
关于10mL0.1 mol.·L-1的NH3 • H2O溶液,下列说法正确的是
A.25°C时,若溶液的 pH=11,则 Kb(NH3 • H2O) = 1X10-6 mol.L-1
B.向溶液中加入少量CH3COONa固体,溶液中 的值变小
的值变小
C.向溶液中加入10mL 0.1 mol.L-1HC1,所得溶液中离子浓度大小顺序为C(NH4+)>C(Cl-)>C(H+)>C(OH-)
D.向溶液中加入5mL0.1mol/LHC1,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
-
向20mL0.1mol/L的NaHCO3溶液中滴加0.1mol/L氨水(已知室温下H2CO3Ka1=4.2×10-7,Ka2=5.6x10-11),NH3•H2O(Kb=1.78×10-5),下列说法错误的是( )
A.0.1mol/L的NaHCO3溶液中:c(OH-)+c(CO )=c(H2CO3)+c(H+)
)=c(H2CO3)+c(H+)
B.无论滴加多少氨水,溶液中一定满足:c(HCO )+c(CO
)+c(CO )+c(H2CO3)=c(Na+)
)+c(H2CO3)=c(Na+)
C.当滴入10mL氨水时,发生反应的离子方程式为:HCO +NH3·H2O=CO
+NH3·H2O=CO +NH
+NH +H2O,该反应的平衡常数约为0.1
+H2O,该反应的平衡常数约为0.1
D.当滴入20mL NH3·H2O时,c(Na+)=c(NH )+c(NH3·H2O)=0.1mol/L
)+c(NH3·H2O)=0.1mol/L
-
常温下,用0.1mol·L-1HCl溶液滴定0.1mol·L-1 NH3·H2O溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。下列说法不正确的是
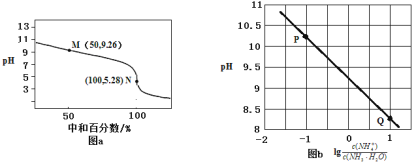
A.Kb(NH3·H2O)的数量级为10-5
B.P到Q过程中,水的电离程度逐渐增大
C.当滴定至溶液呈中性时,c(NH4+)>c(NH3·H2O)
D.N点,c(Cl- ) - c(NH4+)=
-
已知:25℃时,氨水的电离常数Kb(NH3·H2O) = 1.8×10-5。该温度下,用0.1 mol·L-1的氨水滴定10.00 mL 0.1 mol·L-1的HA溶液,溶液的pH与所加氨水的体积(V)的关系如图所示。下列说法正确的是( )
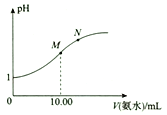
A. HA为弱酸
B. M点溶液中存在c(A-)=c(NH4+)+c(NH3·H2O)
C. M、N两点溶液中水电离出来的c(H+):M<N
D. 25℃时,NH4+的水解平衡常数为1.8×10-9
-
下列关于电解质溶液的叙述正确的是( )
A. 若常温下0.1mol/L的氨水pH为11, 则NH3·H2O电离常数约为10-6
B. 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8
C. 某温度下纯水中c(OH-)=2×10—7mol/L,该温度下0.1mol/L的盐酸的pH=1
D. 用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaOH溶液的体积前者小于后者的10倍
-
常温向20mL 0.1mol·L-1 氨水中滴加0.1mol·L-1 盐酸,溶液pH随滴加盐酸溶液体积的变化如图2 所示。下列说法正确的是

A. a点时,c(NH3·H2O)>c(C1-)>c(NH4+)>c(OH-)>c(H+)
B. a~b区域内c(NH4+)+ c(NH3·H2O) =0.1mol· L-1
C. 当V(HC1)=10 mL时,c(NH4+)-c(NH3·H2O) =2[c(OH-)-c(H+)]
D. 当V(HCl) =20 mL时,c(H+)+c(C1-)>c(NH4+)+c(NH3·H2O) +c(OH-)
-
关于常温下0.1 mol/L氨水(pH=11.12)的下列说法不正确的是
A. 加水稀释过程中,c(H+)/c(OH-) 的值增大
B. 根据以上信息,可推断NH3·H2O为弱电解质
C. 与pH=11.12的 NaOH溶液相比,NaOH溶液中c(Na+) 大于氨水中c(NH )
)
D.加入少量NH4Cl 固体,溶液中水的电离平衡:H2O ⇌ H+ + OH-正向移动
的值变小


