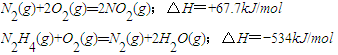-
N2H4(肼)可作用制药的原料,也可作火箭的燃料。
(1)肼能与酸反应。N2H6C12溶液呈弱酸性,在水中存在如下反应:
①N2H62++H2O N2H5++H3O平衡常数K1
N2H5++H3O平衡常数K1
②N2H5++H2O N2H4+H3O平衡常数K2
N2H4+H3O平衡常数K2
相同温度下,K1>K2,其主要原因有两个:
①电荷因素,N2H5+水解程度小于N2H62+;
② ___________________________________________;
(2)工业上,可用次氯酸钠与氨反应制备肼,副产物对环境友好,该反应化学方程式是___________________________________________________。
(3)气态肼在催化剂作用下分解只产生两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝色。在 密闭容器中发生上述反应,平衡体系中肼的体积分数与温度关系如图所示。
①P2 _____P1(填:<、>或=,下同)。
②反应I:N2H4(g) N2(g)+4NH3(g) ΔH1;
N2(g)+4NH3(g) ΔH1;
反应II:N2(g)+3H2(g) Δ2NH3(g) ΔH2。
Δ2NH3(g) ΔH2。
ΔH1________ΔH2
7N2H4(g) 8NH3(g)+3N2(g)+2H2(g) ΔH
8NH3(g)+3N2(g)+2H2(g) ΔH
ΔH=____________(用ΔH1、ΔH2表示)。
③向1L恒容密闭容器中充入0.1 mol N2H4,在30℃、Ni-Pt催化剂作用下发生反应N2H4(g) N2(g)+2H2(g),测得混合物体系中(只含N2、H2、N2H4),n(N2)+n(H2)/n(N2H4)(用y表示)与时间的关系如图所示。
N2(g)+2H2(g),测得混合物体系中(只含N2、H2、N2H4),n(N2)+n(H2)/n(N2H4)(用y表示)与时间的关系如图所示。

4分钟时反应到达平衡,0~4.0 min时间内H2的平均生成速率v(H2)=_____________________。
(4)肼还可以制备肼—碱性燃料电池,氧化产物为稳定的对环境友好的物质。该电池负极的电极反应式为______________;若以肼—氧气碱性燃料电池为电源,以NiSO4溶液为电镀液,在金属器具上镀镍,开始两极质量相等,当两极质量之差为1.174g时,燃料电池中内电路至少有_________mol OH-迁移通过阴离子交换膜。
-
肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。回答下列问题:
(1)已知反应的热化学方程式如下:
①N2H4(g) N2(g)+2H2(g) △H1;
N2(g)+2H2(g) △H1;
②N2(g)+3H2(g) 2NH3(g) △H2。
2NH3(g) △H2。
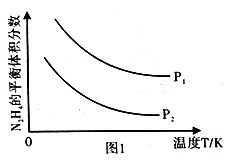
反应热△H1 _____(填“大于”或“小于”) △H2。向2 L的恒容密闭容器中充入1 mol N2H4,发生反应①, (用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
(用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
(2)肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系。
①该反应的化学方程式为________________________________________。
②p2_______ (填“大于”或“小于”) p1。
③图中N2H4的平衡体积分数随温度升高而降低,其原因是__________________________________。
-
肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。回答下列问题:
(1)已知反应的热化学方程式如下:
①N2H4(g) N2(g)+2H2(g) △H1;
N2(g)+2H2(g) △H1;
②N2(g)+3H2(g) 2NH3(g) △H2。
2NH3(g) △H2。
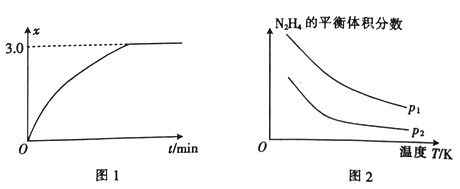
反应热△H1 _____(填“大于”或“小于”) △H2。向2 L的恒容密闭容器中充入1 mol N2H4,发生反应①, (用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
(用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
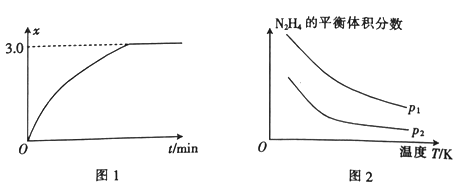
(2)肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系。
①该反应的化学方程式为________________________________________。
②p2_______ (填“大于”或“小于”) p1。
③图中N2H4的平衡体积分数随温度升高而降低,其原因是__________________________________。
-
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面。请回答下列问题:
(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
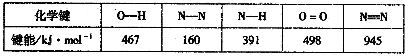
①N2H4中氮元素的化合价为__________。
②气态N2H4在氧气中燃烧的热化学方程式为__________。
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为__________。
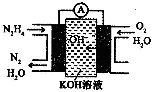
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为__________.
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解。
①写出盐酸肼第一步水解的离子方程式__________。
②盐酸肼水溶液中离子浓度的关系为__________ (填序号)。
A.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C.c(N2H62+)+ c([N2H5·H2O+]) +c(H+)= c(Cl-)+c(OH-)
(5〕常温下,将0.2 mol/L盐酸与0.2 mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕。若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为__________。
-
(14分)肼(N2H4)与N2O4,是火箭发射中最常用的燃料与助燃剂。
(1)已知

则使1 mol N2O4 (l)完全分解成相应的原子时需要吸收的能量是 。
(2)800℃时,某密闭容器中存在如下反应: ,若开始向容器中加入1 mol/L的NO2,反应过程中NO的产率随时间的变化如下图曲线I所示。
,若开始向容器中加入1 mol/L的NO2,反应过程中NO的产率随时间的变化如下图曲线I所示。

①反应Ⅱ相对于反应I而言,改变的条件可能是 。
②请在图中绘制出在其它条件与反应I相同时,反应在820℃时进行,NO的产率随时间的变化曲线。
③800℃时,若开始时向容器中同时加入1 mol/L NO、0.2 mol/L O2、0.5 mol/L NO2,则v(正)____v(逆)。
(3)己知 ,t时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
,t时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
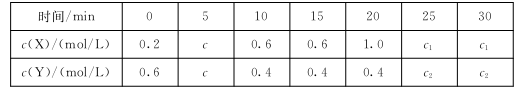
①c( X)代表 (填化学式)的浓度,该反应的平衡常数K= 。
②前10 min内用NO2表示的反应速率为 ,20 min时改变的条件是 ;重新达到平衡时,NO2的百分含量 (填选项前字母)。
a.增大 b.减小 c.不变 d.无法判断
-
2008年9月我国“神七”发射升空,中国航天员实现首次太空行走.运载火箭的原料用肼(N2H4)作为发动机的燃料,NO2为氧化剂,反应生成氮气和水蒸气.已知:
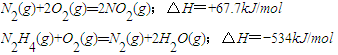
下列判断正确的是( )
A..所有物质与氧气发生的化学反应都是放热反应
B..N2H4的燃烧热为534kJ/mol
C.肼与NO2反应的热化学方程 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g);△H=-1135.7kJ/mol
D..3.2g肼完全反应转移的电子数为0.6mol
-
(8分)肼(N2H4)是火箭发射常用的燃料。一种以肼(N2H4)为燃料的电池装置如图所示。 该燃料电池的电极材料采用多孔导电材料,以提高电极反应物在电极表面的吸附量,并使它们与电解质溶液充分接触,以空气中的氧气作为氧化剂,KOH溶液作为电解质。

(1)负极上发生的电极反应为_________________;
(2)电池工作时产生的电流从_______电极经过负载后流向________电极(填“左侧”或“右侧”)。
(3)放电一段时间后,右侧溶液的pH (填“变大”或“变小”)
-
氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。

①下列能说明反应达到平衡状态的是____(选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为 ___(选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=____。
②已知该反应 ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时, =_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
=_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
-
氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
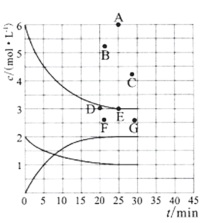
①下列能说明反应达到平衡状态的是____(选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为 ___(选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=____。
②已知该反应 ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时, =_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
=_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
-
氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
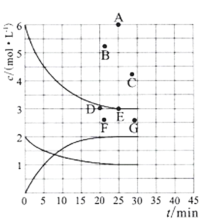
①下列能说明反应达到平衡状态的是____(选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为 ___(选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 |
| φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=____。
②已知该反应 ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时, =_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
=_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
N2H5++H3O平衡常数K1
N2H4+H3O平衡常数K2

N2(g)+4NH3(g) ΔH1;
Δ2NH3(g) ΔH2。
8NH3(g)+3N2(g)+2H2(g) ΔH
N2(g)+2H2(g),测得混合物体系中(只含N2、H2、N2H4),n(N2)+n(H2)/n(N2H4)(用y表示)与时间的关系如图所示。








 ,t时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
,t时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示: