-
粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13+3Na2CO3→2NaAlSiO4+4NaAlO2+3CO2 ↑ ①
Al6Si2O13+5Na2CO3→2Na2SiO3+6NaAlO2+5CO2 ↑ ②
SiO2+Na2CO3→Na2SiO3+CO2 ↑ ③
(1)粉煤灰中铝的质量分数为________%。
(2)用l mol Al6Si2O13和4mol SiO2制得5mol NaAlO2、lmolNaAlSiO4,还应制得Na2SiO3 mol,共消耗Na2CO3________mol(得到的固体中无SiO2)。
(3)若粉煤灰中Al6Si2O13与SiO2的物质的量之比为1:2,则1妇粉煤灰与6molNa2CO3反应(反应物全部都参与反应),可制得NaAlO2 mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2)=x,消耗Na2CO3 ymol,试确定y与x的关系式。
高三化学填空题中等难度题查看答案及解析
-
粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为43.4%,还有含量较多的SiO2(其他成分不含Al和Si)。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有关化学方程式为:
Al6Si2O13 + 3Na2CO3 → 2NaAlSiO4+ 4NaAlO2 + 3CO2↑ ①
Al6Si2O13 + 5Na2CO3 → 2Na2SiO3 + 6NaAlO2 + 5CO2↑ ②
SiO2 + Na2CO3 → Na2SiO3 + CO2↑ ③
(1)粉煤灰中铝的质量分数为________% 。
(2)用1 mol Al6Si2O13 和 4 mol SiO2制得5mol NaAlO2、1mol NaAlSiO4,还应制得Na2SiO3____________mol,共消耗Na2CO3 mol(得到的固体中无SiO2)。
(3)若粉煤灰中 Al6Si2O13 与 SiO2的物质的量之比为1:2,则1kg粉煤灰与6mol Na2CO3反应(反应物全部都参与反应),可制得NaAlO2_________________mol。
(4)若用100 mol Al6Si2O13同时生产NaAlSiO4和NaAlO2,且n(NaAlSiO4):n(NaAlO2) = x,消耗Na2CO3 y mol,试确定y与x的关系式。
高三化学计算题困难题查看答案及解析
-
(12分)粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
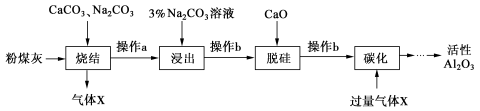
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
高三化学填空题中等难度题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
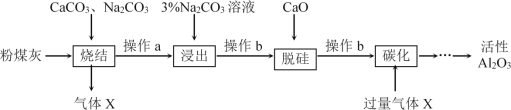
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式___________。
(2)操作a为冷却、研磨,其中研磨的目的是___________________________。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为_____________。
(4)操作b的名称是_______,所用的玻璃仪器有_______、_________和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为__________________。
(6)上述过程中循环使用的物质是______________________。
高三化学实验题中等难度题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
(6)上述过程中循环使用的物质是 。
高三化学实验题困难题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
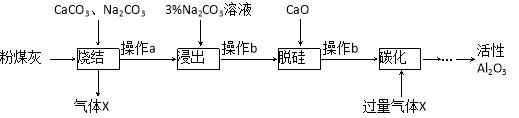
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
(6)上述过程中循环使用的物质是 。
高三化学实验题中等难度题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
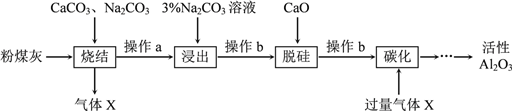
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式_________________________。
(2)操作a为冷却、研磨,其中研磨的目的是________________________。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为_______________。
(4)操作b的名称是_________,所用的玻璃仪器有___________、__________和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为________________。
(6)上述过程中循环使用的物质是_______________。
高三化学实验题中等难度题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
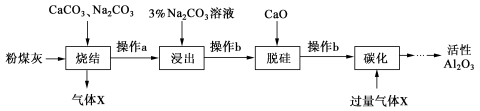
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为 。
高三化学实验题简单题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
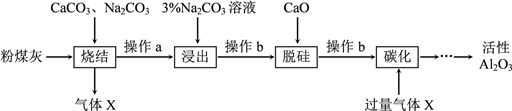
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式_________________________。
(2)操作a为冷却、研磨,其中研磨的目的是________________________。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为_______________。
(4)操作b的名称是_________,所用的玻璃仪器有___________、__________和烧杯。
(5)“碳化”时生成沉淀,沉淀的化学式为________________。
(6)上述过程中循环使用的物质是_______________。
高三化学实验题困难题查看答案及解析
-
粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如图:
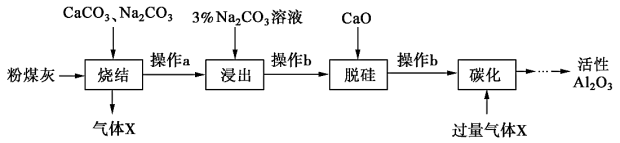
已知烧结过程的产物主要是:NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式 。
(2)操作a为冷却、研磨,其中研磨的目的是 。
(3)浸出过程中,NaFeO2可完全水解,水解反应的离子方程式为 。
(4)操作b的名称是 ,所用的玻璃仪器有 、 和烧杯。
(5)“碳化”时生成沉淀的化学式为 。
高三化学实验题困难题查看答案及解析