-
下列物质与用途对应关系不正确的是
选项
A
B
C
D
物质
单质碘
苯甲酸钠
聚乙烯
二氧化硅
用途
食盐添加剂
食品防腐剂
食品保鲜膜
光导纤维
高三化学选择题简单题查看答案及解析
-
下列有关物质的性质或应用的说法不正确的是( )
A.二氧化硅是生产光纤制品的基本原料 B.水玻璃可用于生产黏合剂和防火剂
C.亚硝酸钠可以用作食品添加剂 D.石油分馏可获得乙烯、丙烯和丁二烯
高三化学选择题简单题查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A.硅酸钠溶液呈碱性,可用作木材防火剂
B.氧化铝的熔点很高,可用于制作耐高温材料
C.二氧化硫具有漂白性,可用作制溴工业中溴的吸收剂
D.乙烯具有还原性,可用作水果的催熟剂
高三化学单选题中等难度题查看答案及解析
-
下列物质的性质与用途具有对应关系的是( )
A.碳酸钠溶液呈碱性,可用于去油污
B.氧化铝的熔点很高,可用于熔融状态下电解制备铝单质
C.二氧化硫具有漂白性,可用作葡萄酒中的抗氧化剂
D.氨气具有还原性,可用作制冷剂
高三化学单选题简单题查看答案及解析
-
(原创)下列各组物质与其用途的关系正确的是
A.碘化钾——食盐中的加碘物质 B.二氧化硅——太阳能电池
C.福尔马林——食品保鲜剂 D.水玻璃——耐火材料
高三化学选择题简单题查看答案及解析
-
(20分)亚硝酸钠是一种工业盐,用途广泛,外观与食盐非常相似,但毒性较强,食品添加亚硝酸钠必须严格控制用量。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
(一)鉴别NaCl和NaNO2
(1)测算溶液pH
常温下,用pH试纸分别测定0.1 mol·L-1两种盐溶液的pH,测得NaNO2溶液呈碱性。
NaNO2溶液呈碱性的原因是________________(用离子方程式解释)。
NaNO2溶液中HNO2的准确浓度为________mol·L-1(测得NaNO2溶液pH=b,用含b的代数式表示)。
(2)沉淀法
取2 mL 0.1mol·L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两只试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=1.8×10-8(mol2/L2);Ksp(AgCl)=1.8×10-10(mol·L-1)2
则反应AgNO2(s)+Cl-(aq)
AgCl(s)+NO2-(aq)的化学平衡常数K=________。
(3)氧化法
取2 mL 0.1mol·L-1两种盐溶液于试管中,分别滴加几滴酸性KMnO4溶液,使酸性KMnO4溶液褪色的是NaNO2溶液。该反应的离子方程式为______________________________。
(二)NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应及气体产物成分。
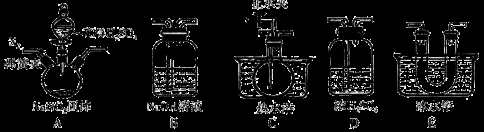
已知:气体的液化温度:NO221℃、NO–152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→_______→_________→_________→_________;组装好仪器后,接下来须进行的操作是_________________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气。
(3)关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸溶液后,A中产生红棕色气体。
①如何验证A中产生的气体中含有NO_________。(写出实验操作、现象和结论)
②装置E的作用是_____________________________。
③A装置中发生反应的化学方程式为_________________________________________。
高三化学实验题极难题查看答案及解析
-
亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强,食品添加亚硝酸钠必须严格控制用量。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液PH
用PH试纸分别测定0.1mol·L-1两种盐溶液的PH,测得NaNO2溶液呈碱性。NaNO2溶液呈碱性的原因是 ________________________(用离子方程式解释)。NaNO2溶液中c(HNO2)=_____________(用溶液中其它离子的浓度关系式表示)
(2)沉淀法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液。两只试管均产生白色沉淀。分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=2×10-8(mol·L-1)2; Ksp(AgCl)=1.8×10-10(mol·L-1)2
则反应AgNO2(s) +Cl-(aq)
AgCl(s)+ NO2-(aq)的化学平衡常数K=__________
(3)氧化法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴酸性KMnO4溶液。使酸性KMnO4溶液褪色的是NaNO2溶液。该反应的离子方程式为____________。
㈡NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应及气体产物成分。
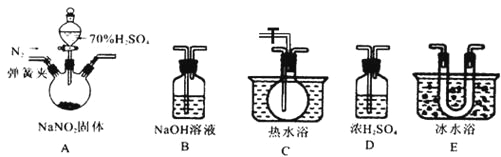
已知: 气体液化的温度:NO221℃ 、 NO –152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→______→ ______→_______→_______;组装好仪器后,接下来进行的操作是________________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①如何确认A中产生气体是否含有NO _________。(写出实验操作、现象和结论)
②装置E的作用是_______________________。
③若向D中通入过量O2,则装置B中发生反应的化学方程式为____________。
高三化学实验题困难题查看答案及解析
-
亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强,食品添加亚硝酸钠必须严格控制用量。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液PH
用PH试纸分别测定0.1mol·L-1两种盐溶液的PH,测得NaNO2溶液呈碱性。NaNO2溶液呈碱性的原因是 ________________________(用离子方程式解释)。NaNO2溶液中c(HNO2)=_____________(用溶液中其它离子的浓度关系式表示)
(2)沉淀法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液。两只试管均产生白色沉淀。分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=2×10-8(mol·L-1)2; Ksp(AgCl)=1.8×10-10(mol·L-1)2
则反应AgNO2(s) +Cl-(aq)
AgCl(s)+ NO2-(aq)的化学平衡常数K=__________
(3)氧化法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴酸性KMnO4溶液。使酸性KMnO4溶液褪色的是NaNO2溶液。该反应的离子方程式为____________。
㈡NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应及气体产物成分。
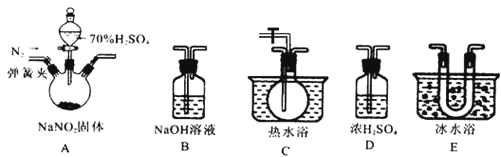
已知: 气体液化的温度:NO221℃ 、 NO –152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→______→ ______→_______→_______;组装好仪器后,接下来进行的操作是________________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①如何确认A中产生气体是否含有NO _________。(写出实验操作、现象和结论)
②装置E的作用是_______________________。
③若向D中通入过量O2,则装置B中发生反应的化学方程式为____________。
高三化学实验题困难题查看答案及解析
-
亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强,食品添加亚硝酸钠必须严格控制用量。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液PH
用PH试纸分别测定0.1mol·L-1两种盐溶液的PH,测得NaNO2溶液呈碱性。NaNO2溶液呈碱性的原因是 ________________________(用离子方程式解释)。NaNO2溶液中c(HNO2)= (用溶液中其它离子的浓度关系式表示)
(2)沉淀法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液。两只试管均产生白色沉淀。分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=2×10-8 (mol·L-1)2; Ksp(AgCl)=1.8×10-10(mol·L-1)2
则反应AgNO2(s) +Cl-(aq)
AgCl(s)+ NO2-(aq)的化学平衡常数K=
(3)氧化法
取2mL0.1 mol·L-1两种盐溶液于试管中,分别滴加几滴酸性KMnO4溶液。使酸性KMnO4溶液褪色的是NaNO2溶液。该反应的离子方程式为 。
㈡NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应及气体产物成分。
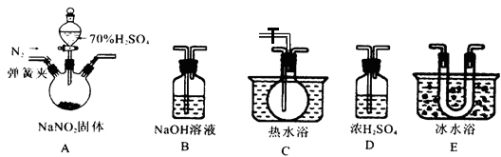
已知: 气体液化的温度:NO2 21℃ 、 NO –152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→ → ______→_______→_______;组装好仪器后,接下来进行的操作是________________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①如何确认A中产生气体是否含有NO _________。(写出实验操作、现象和结论)
②装置E的作用是_______________________。
③若向D中通入过量O2,则装置B中发生反应的化学方程式为____________。
高三化学实验题极难题查看答案及解析
-
下列生活用品与其主要成分对应正确的是( )
A. 煤炭——单质碳 B. 常用食品包装袋——聚苯乙烯
C. 肥皂——高级脂肪酸钠 D. 明矾——十二水合硫酸铝
高三化学单选题简单题查看答案及解析