-
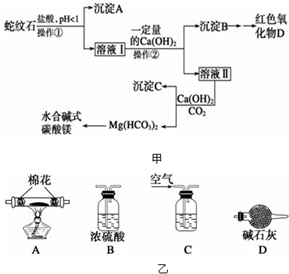
蛇纹石是一种富镁硅酸盐矿物的总称,因其颜色青绿相间酷似蛇皮而得名。蛇纹石可以看作由MgO、FeO和Fe2O3、Al2O3、SiO2组成。工业上由蛇纹石制取碱式碳酸镁产品的流程如下:
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+、Al3+外,还含有的金属离子是________。
(2)向Ⅰ中加入H2O2的作用是 ,有关离子方程式 ,加入Ca(OH)2时, 需要控制溶液pH在7~8之间(有关氢氧化物沉淀的pH见下表)。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
若pH>8可能导致的后果 。
(3)沉淀物A可作为提取红色颜料的原料,若向沉淀物A中加入 溶液,然后过滤、洗涤、 _________(填写实验操作名称),即可获得红色颜料,实现废物的综合利用。
(4)若产品的化学式用aMgCO3·bMg(OH)2·cH2O表示,现称取18.2 g产品并使之完全分解,收集到3.36L CO2(标准状况下)和8.0 g MgO,通过计算确定产品的化学式中:a=________,b=________,c=________。
-
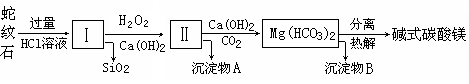
(10分)蛇纹石是一种含水的富镁硅酸盐矿物的总称,可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 3.3 | 9.4 |
| 完全沉淀的pH | 3.7 | 5.2 | 11.0 |
实验步骤如下:

⑴ 实验室完成操作①所用到的玻璃仪器有:_______________________________。
⑵ 操作②中应控制溶液pH的合理范围是___________(填序号)。
A. 小于1.5 B. 1.5~3.3 C. 7~8 D. 大于9.4
⑶ 检验溶液Ⅱ中是否含有Fe3+的操作与结论是:_____________________________________
⑷ 从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为:_______________________________,再进行____________、洗涤 、___________(依次填写实验操作名称)。
-
蛇纹石是一种含水的富镁硅酸盐矿物的总称,可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 3.3 | 9.4 |
| 完全沉淀的pH | 3.7 | 5.2 | 11.0 |
实验步骤如下:

(1)实验室完成操作①所用到的玻璃仪器有:________。
(2)操作②中应控制溶液pH的合理范围是________(填序号)。
A.小于1.5 B.1.5~3.3 C.7~8 D.大小9.4
(3)检验溶液Ⅱ中是否含有Fe3+的操作与结论是______________________。
(4)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为________,再进行________、洗涤、________(依次填写实验操作名称)。
-
(16分)蛇纹石因其花纹似蛇皮而得名,某地蛇纹石大约含MgO38%,另外除了含SiO2外,还含有CaO、Fe2O3、Al2O3等氧化物,由蛇纹石矿制备MgO的工艺流程如下。
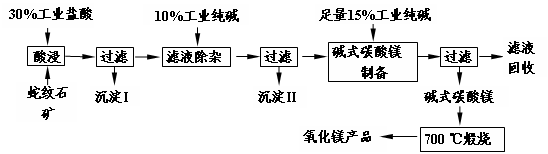
(1)写出酸浸过程中的一个离子方程式________。若在实验室进行酸浸过程,需要的仪器有烧杯、________。
(2)沉淀I的成分是________(写化学式)。写出它的一个用途________。
(3)沉淀II的成分是________。
(4)从滤液中能回收的物质有。
(5)写出碱式碳酸镁700 ℃煅烧产生氧化镁的化学方程式________。
-
(7分)蛭石为一种层状结构的含镁的铝硅酸盐,是黑云母等天然矿物风化蚀变的产物,因为其受热膨胀时呈挠曲状,形态酷似水蛭,故此得名蛭石。膨化后的蛭石呈颗粒状,有隔热、耐冻、抗菌、防火、吸声等优异性能,但不耐酸。
(1)某硅酸盐矿石的组成可以看作SiO2中有1/4的Si被Al置换,再由Mg平衡其电荷形成的。该矿石的组成以氧化物形式表示为________。
(2)某校研究性学习小组取得了某种牌号的膨化蛭石样品,其成分可以用氧化物(MgO、Fe2O3、Al2O3、SiO2、H2O)的形式表示。为研究蛭石的组成,拟进行实验探究,实验流程及相关数据如下:

①固体A的化学式是________;
②固体F的物质的量是;
③通过计算,给出用氧化物的形式表示某种膨化蛭石组成的化学式。
-
【化学-选修2:化学与技术】(15分)
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成的。由蛇纹石制取碱式碳酸镁的实验步骤如下:
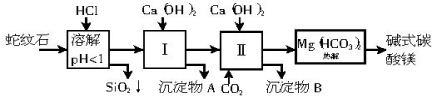
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是_ 。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),则沉淀物A的主要成份为 ,沉淀物B的主要成份为 。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的PH值 | 1.5 | 3.3 | 9.4 |
(3)若要从沉淀物A中提取出某种可用于工业冶炼铝的原料,应先向A中加入 溶液(填物质化学式)再过滤,然后向滤液中通入过量CO2,过滤、灼烧。请写出通入CO2时发生反应的离子方程式 。
(4)为确定产品aMgCO3・bMg(OH)2・cH2O中a、b、c的值,称取18.2g样品完全分解后,测得产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中a=______、b=_______、c=______。
-
(17分)蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
实验步骤如下:
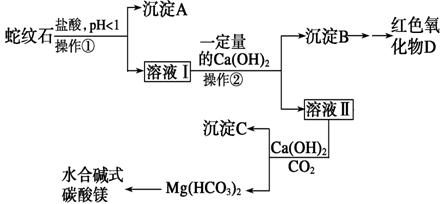
请回答下列问题:
(1)实验室完成操作①所用到的玻璃仪器有________________________。
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是___________________________
_____________________________________________________________________。
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为________________________________________________________________________,
再进行__________、________、________(依次填写实验操作名称)。
(4)操作②中应控制溶液pH的合理范围是____(填序号)。
A.小于1.5 B.1.5~3.3
C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O]的组成,取样7.28 g于装置A的玻璃管中,请按由左―→右顺序将下列装置连接好(填序号,装置可重复使用):________________________________________________________________________,
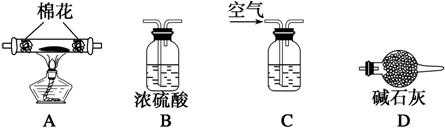
装置C应盛的试剂是______________________。
-
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下
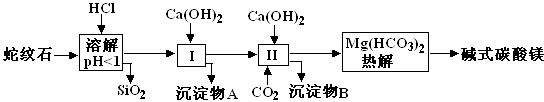
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是______.
(2)进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致______溶解、______沉淀.
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入______ (填入物质的化学式),然后______ (依次填写实验操作名称).
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是______(填写物质化学式).
(5)现设计一个实验,确定产品aMgCO3•bMg(OH)2•cH2O中a、b、c的值(已知均为正整数),请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):①样品称量 ②高温分解 ③______ ④______ ⑤称出MgO的质量.
-
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下
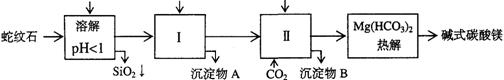
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是_____________
(2)进行Ⅰ操作时,控制溶液pH=7-8(有关氢氧化物沉淀的pH见上表)
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致_________溶解、_________沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填入物质的化学式),然后__________________________________ (依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是_____________(填写物质化学式)。
(5)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式________。
(6)若热分解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数 (填 “升高”、“降低”或“不变”)。
-
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
实验步骤如图甲:
请回答下列问题:
(1)操作①的名称______
(2)检验溶液Ⅱ中是否含有Fe3+的方程式 (最优方法)______
(3)沉淀A与萤石(CaF2)在硫酸酸化下可以制备石膏,写出反应方程式______
(4)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为______
(5)操作②中应控制溶液pH的合理范围是______(填序号).
A.小于1.5B.1.5~3.3 C.7~8 D.大于9.4
(6)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样18.2g g于装置A的玻璃管中,请按由左-→右顺序将下列装置连接好(如图乙)(填序号,装置可重复使用):______,装置C应盛的试剂是______. 充分反应后,如果实验测得硬质玻璃管中剩余固体8.0g,共放出6.6gCO2气体,则x:y:z=______.