-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题简单题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景.下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇
B.天然气
C.液化石油气
D.氢气高三化学选择题中等难度题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题中等难度题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题简单题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题中等难度题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题简单题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是
A.甲醇 B.天然气 C.液化石油气 D.氢气
高三化学选择题简单题查看答案及解析
-
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列电池均可用作燃料电池的燃料,其中最环保的是
A.氢气 B.天然气 C.液化石油气 D.甲醇
高三化学选择题简单题查看答案及解析
-
Ⅰ.甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径。由CO2制备甲醇的过程可能涉及反应如下:
反应Ⅰ:CO2(g)+H2(g)
CO (g)+H2O(g) ΔH
1=41.19 kJ·mol-1
反应Ⅱ:CO(g)+2H2(g)
CH3OH(g) ΔH2
反应Ⅲ:CO2(g)+3H2(g)
CH3OH(g)+H2O(g)ΔH3=-49.58 kJ·mol-1
回答下列问题:
(1)反应Ⅲ的ΔS________(填“<”“=”或“>”)0;反应Ⅱ的ΔH2=__________________。
(2)在恒压密闭容器中,充入一定量的H2和CO2(假定仅发生反应Ⅲ),实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图1所示。

反应过程中,不能判断反应Ⅲ已达到平衡状态的标志是________(填字母)。
A.断裂3 mol H—H键,同时生成2 mol H—O键
B.CH3OH的浓度不再改变
C.容器中气体的平均摩尔质量不变
D.容器中气体的压强不变
Ⅱ.电化学原理在化学工业中有广泛的应用。请根据下图回答问题:


(3)根据图2,若装置B中a
为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.16 g,则流经电路的电子的物质的量为____________。
(4)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含N
H4F等的无水熔融物生产NF3,其电解原理如图3所示。写出a电极的电极反应式:_____________________。
高三化学简答题中等难度题查看答案及解析
-
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2 加氢合成甲醇是合理利用CO2的有效途径。由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+ H2(g)
CO (g)+H2O(g) △H1=+41.19kJ•mol-1
反应Ⅱ:CO(g)+2H2(g)
CH3OH(g) △H 2
反应Ⅲ:CO2(g)+3H2(g)
CH3OH(g) +H2O(g) △H3=-49.58kJ•mol-1
回答下列问题:
(1)反应Ⅲ的△S (填“<”、“=”或“>”)0;反应Ⅱ的△H2= 。
(2)在恒压密闭容器中,充入一定量的H2和CO2(假定仅发生反应Ⅲ),实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图1所示。
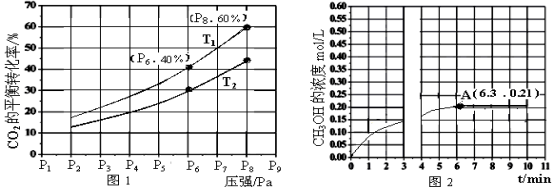
①反应过程中,不能判断反应Ⅲ已达到平衡状态的标志是
A.断裂3molH-H键,同时断裂2molH-O键 B.CH3OH的浓度不再改变
C.容器中气体的平均摩尔质量不变 D.容器中气体的压强不变
②比较T1与T2的大小关系:T1 T2(填“<”、“=”或“>”),理由是: 。
③在T1和P6的条件下,往密闭容器中充入3mol H2和1mol CO2,该反应在第5min时达到平衡,此时容器的体积为1.8L;则该反应在此温度下的平衡常数为 。
a.若此条件下反应至3min时刻,改变条件并于A点处达到平衡,CH3OH的浓度随反应时间的变化趋势如图2所示(3~4min的浓度变化未表示出来);则改变的条件为 。
b.若温度不变,压强恒定在P8的条件下重新达到平衡时,容器的体积变为 L;
高三化学填空题困难题查看答案及解析