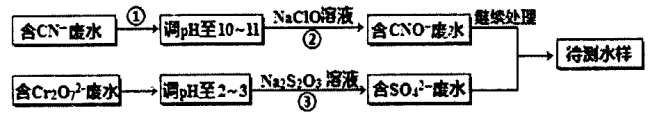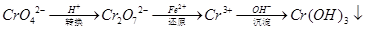-
含铬(Ⅵ)废水能诱发致癌,对人类和自然环境有严重的破坏作用。利用Cu2O光催化可以处理含有Cr2O72-的废水。
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计)。
①阳极材料是_________。
②阴极的电极反应式是_________;电解总反应为:_________。
(2)还原法
①工业上可用肼(N2H4)与新制的Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为_________。
②控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体。反应过程中需要不断地加入烧碱,其原因是_________。
Ⅱ.利用Cu2O光催化处理含有Cr2O72-的废水的研究。
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如下图所示。
在图中用短线和箭头画出电子移动的方向,写出Cr2O72-转化Cr3+的电极反应_________。
(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O 与Cr2O72-发生氧化还原反应。
已知:Cu2O的添加量是1.74×10-4 mol/L,Cr2O72-的初始浓度是9.60×10-4 mol/L;对比实验,反应1.5小时结果如下图所示。结合试剂用量数据和实验结果可得到的结论和依据是_______。
(3)溶液的pH对Cr2O72-降解率的影响如下图所示。
已知:Cu2O  Cu +CuSO4;酸性越大,Cr2O72-被还原率越大。
Cu +CuSO4;酸性越大,Cr2O72-被还原率越大。

①由上图可知,pH分别为2、3、4时,Cr2O72-的降解率最好的是_________,其原因是_________。
②已知pH=5时,会产生Cr(OH)3沉淀。pH=5时,Cr2O72-的降解率低的原因是_______。
-
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应
Cr2O72–+6Fe2++14H+ 2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
A.阳极反应为Fe-2e- Fe2+
Fe2+
B.电解过程中溶液pH不会变化
C.反应过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原
-
【化学-化学与技术】
铬元素被人体吸收后具有致癌作用.某工业废水中含有Cr2O72-的酸性废水,可采用如下工艺处理:向废水中加入适量的NaCl,用Fe做电极进行电解,Cr2O72-还原为Cr3+然后生成Cr(OH)3沉淀除去.
(1)电解时加入适量NaCl的目的是______.
(2)电解时发生的电极反应为:阳极反应为______,阴极反应为______.
(3)Cr2O72-转化为Cr3+的原理是______.
(4)与Cr(OH)3同时生成的沉淀还有______(填化学式).
-
电镀等工业废水中常含有剧毒、致癌的Cr2O72-.该废水处理的一种方法是:利用还原剂把Cr2O72-还原成毒性较低的Cr3+,再加碱生成沉淀.另一种方法是:向废水中加入适当的NaCl,用Fe作电极进行电解.下列说法错误的是( )
A.电解时,阳极反应为:Fe-2e-=Fe2+
B.电解过程中阴极能产生氢气
C.电解法中,转化Cr2O72-的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
D.电解过程中,阳极附近生成Cr(0H)3和Fe(0H)3沉淀
-
铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72–的酸性废水通过铁炭混合物,在微电池正极上Cr2O72–转化为Cr3+,其电极反应式为_____________。
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。
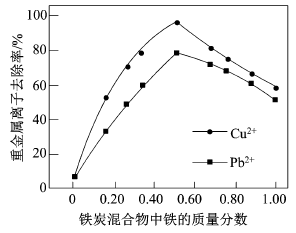
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是__________。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________。
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4–(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为 。
②纳米铁粉与水中NO3-反应的离子方程式为4Fe+NO3–+10H+===4Fe2++NH4++3H2O
研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是 。
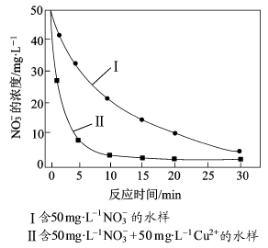
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见图),产生该差异的可能原因是 。
-
某电镀铜厂有两种废水需要处理,一种废水中含有CN﹣离子,另一种废水中含有Cr2O72﹣离子。该厂拟定如图所示的废水处理流程。
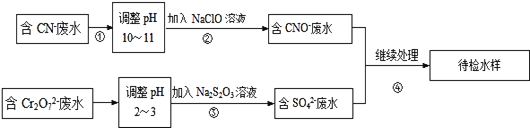
回答以下问题:
(1)电镀铜时的阳极材料是_______。
(2)②中使用的NaClO溶液呈碱性,用离子方程式解释原因__________。
(3)②中反应后无气体放出,该反应的离子方程式为_________。
(4)③中反应时,每0.4mol Cr2O72﹣转移2.4mol e﹣,该反应的离子方程式为______。
(5)铜是与人类关系非常密切的有色金属,已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生:2Cu+=Cu+Cu2+。大多数+1价铜的化合物是难溶物,如:Cu2O、CuI、CuCl、CuH等。
①写出CuH在过量稀盐酸中有气体生成的离子方程式______________。
②将CuH溶解在适量的稀硝酸中,完成下列反应的化学方程式:___CuH +___HNO3 = __Cu(NO3)2 +____H2↑ +___NO +___H2O。
-
【选修2 :化学与技术】
某工厂的镀铜废水中含有CN-和Cr2O72一离子,需要处理达标后才能排放。该厂拟用下列流程进行废水处理,回答下列问题:
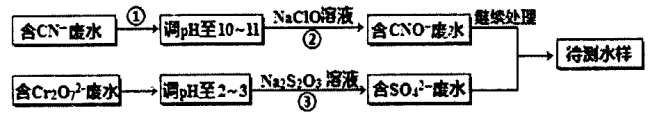
(1)流程中可用pH 试纸测定溶液的pH,pH试纸的使用方法是_______________;
(2)步骤②中反应无气体放出,该反应的离子方程式为____________;
(3)步骤③中,每处理1.0molCr2O7—时转移电子数为6NA,该反应的离子方程式为_____________;
(4)取少量待测水样于试管中,加入NaOH 溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,产生该现象对应的离子方程式为_________。
(5)含氰化物的废水必须经检测达标后(排放标准为CN—的含量<0.5mg/L)才能排放。现取该法处理后的废水100.0mL,用“试银灵”为指示剂、1.0×10-4mol/L的AgNO3标准溶液滴定,终点时溶液由黄色变为橙红色,消耗标准液的体积为5.00mL,反应的离子方程式为Ag + 2CN—=[Ag(CN)2]一,该水样中CN-的含量为________mg/L(不考虑Cr等元素的干扰)。该厂处理后的废水能否合法排放________。
-
某工业废水含有CN﹣和Cr2O72﹣等离子,需经污水处理达标后才能排放,污水处理拟用下列流程进行处理:
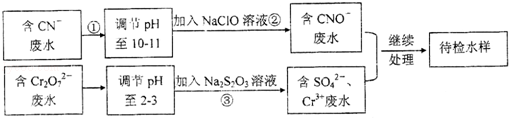
回答下列问题:
(1)步骤②中,CN﹣被ClO﹣氧化为CNO﹣的离子方程式为 .
(2)步骤③的反应方程式为S2O32﹣+Cr2O72﹣+H+→SO42﹣+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72﹣,反应中S2O32﹣失去e﹣ mo1.
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是 .
(4)在25℃下,将a mol•L﹣1的NaCN溶液与0.01mol•L﹣1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示CN﹣的水解常数Kh= mol•L﹣1.若25℃时将浓度均为0.1mol•L﹣1的NaCN、HCN溶液等体积混合后,溶液呈碱性,则关于该溶液的说法不正确的是(填字母).
a.此溶液一定有c(Na+)+c(H+)=c(OH﹣)+c(CN﹣)
b.此溶液一定有c(Na+)=c(HCN)+c(CN﹣)
C.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)利用Cr2O72﹣通过下列方法测定某锡粉的纯度(杂质不参与反应):取ag锡粉溶于盐酸中,向生成的SnCl2中加入过量的FeCl3溶液,用b mol/L K2Cr2O7滴定生成的Fe2+(已知酸性环境下,Cr2O72﹣可被还原为Cr3+),共用去K2Cr2O7溶液m mL.则锡粉中锡的质量分数是 .(Sn的摩尔质量为M g/mol,用含a、b、m、M的代数式表示)
-
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:

己知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
A.溶液颜色保持不变,说明上述可逆反应达到达平衡状态
B.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6
D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
-
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:
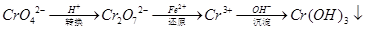
己知转化过程中的反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是( )
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是( )
A.转化过程中,增大c(H+),平衡向正反应方向移动,CrO42﹣的转化率提高
B.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
C.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
D.常温下转化反应的平衡常数K=104,则转化后所得溶液的pH=1
Cu +CuSO4;酸性越大,Cr2O72-被还原率越大。