-
铝碳酸镁[AlaMgb·(CO3)c·(OH)d·eH2O]用于慢性胃炎,称取3.0g铝碳酸镁样品,溶于50mL 2mol/L的盐酸(过量),收集到气体112mL(标准状况);往所得溶液中加入40mL 3mol/L的NaOH溶液,过滤,将所得沉淀洗涤、干燥、称量得固体1.74g;再将滤液稀释到100mL,测得溶液中OH-的浓度为0.1mol/L,由计算可以确定e的值为
A.4 B.5 C.7 D.8
高三化学选择题简单题查看答案及解析
-
碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,有效成分碳酸镧难溶于水,可用于慢性肾衰患者高磷血症的治疗。
Ⅰ.碳酸镧可由LaCl3和碳酸氢铵为原料来制备,避免生成碱式碳酸镧[La(OH)CO3],整个反应需在较低的pH条件下进行。化学兴趣小组利用下列装置在实验室中制备碳酸镧。

(1)仪器X的名称是_____。
(2)如下左图装置是启普发生器,常用于实验室制取CO2、H2等气体,具有“随开随用、随关随停”的功能。右图装置与启普发生器原理类似,也可用于实验室制取CO2的装置的是______(填选项字母)。
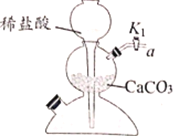 A
A B
B C
C
(3)关闭活塞K2,______,说明如下装置气密性良好。

(4)装置乙用于制备氨气,可以选用的试剂是____(填选项字母)。
A、NH4Cl固体和Ca(OH)2固体 B、生石灰和浓氨水 C、碱石灰和浓氨水 D、无水CaCl2和浓氨水
(5)实验装置接口的连接顺序是:a接____。为制得纯度较高的碳酸镧,实验过程中需要注意的问题是__。
II.可用碳酸氢钠溶液代替碳酸氢铵溶液,与氯化镧反应制备碳酸镧。
(6)精密实验证明:制备过程中会有气体逸出,则制备过程总反应的离子方程式是________。
(7)制备时,若碳酸氢钠滴加过快,会降低碳酸镧的产率,可能的原因是_____。
III、碳酸镧咀嚼片中有效成分测量。
(8)准确称取碳酸镧咀嚼片ag,溶于10.0 mL稀盐酸中,加入10 mL NH3-NH4C1缓冲溶液,加入0.2 g紫脲酸铵混合指示剂,用0.5 mo1·L-1,EDTA (Na2H2Y)标准溶液滴定至呈蓝紫色(La3++ H2y2-= LaY-+2H+),消耗EDTA标准溶液VmL。则咀嚼片中碳酸镧(摩尔质量为458 g/mol)的质量分数w=____。
高三化学实验题中等难度题查看答案及解析
-
碳酸镧能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组对碳酸镧的实验室制备进行了探究:
已知:ⅰ.La2(CO3)3难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[La(OH)CO3]。
ⅱ.LaCl3与易溶的碳酸盐或碳酸氢盐反应可制备La2(CO3)3。
(1)甲组同学利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
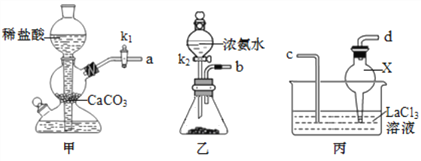
①仪器X的作用为__________;锥形瓶中可选用的试剂为__________(填化学式)。
②实验中 K1、 K2打开的先后顺序为______________;为保证碳酸镧的纯度,实验过程中需要注意的问题有_____________________。
(2)乙组同学对碳酸钠和碳酸氢钠与氯化镧反应制备碳酸镧进行了探究。
①通过实验发现用碳酸氢钠溶液制备碳酸镧的纯度高,理由是__________ (任写一条)。
②请写出用碳酸氢钠溶液制备碳酸镧的离子方程式_____________________________。
③所制碳酸镧需经洗涤,才能达到医用要求,请写出对碳酸镧沉淀洗涤的方法:
___________________________________________________。
(3)碳酸镧(式量为458)质量分数的测定:准确称取 10.0g 产品试样,溶于10.0mL稀盐酸中,加入10mL NH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 40.00mL。则产品中碳酸镧的质量分数 w=___________。
高三化学实验题困难题查看答案及解析
-
碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3 为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
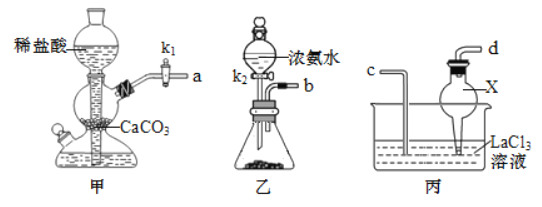
①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2 打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7 mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
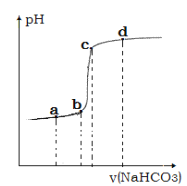
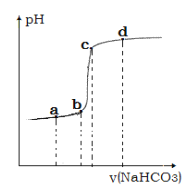
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
高三化学实验题中等难度题查看答案及解析
-
碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3 为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。

①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2 打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7 mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
高三化学实验题中等难度题查看答案及解析
-
达喜【AlaMgb(OH)c(CO3)d ·xH2O】常用于中和胃酸。

(1)1 mol达喜与足量的盐酸完全反应后生成水的物质的量为 mol(用含x等字母的代数式表示)。
(2)达喜化学式中a、b、c、d的关系为a+b c+d(填“>”、“=”或“<”)。
(3)已知在常温下溶液中Al3+、Mg2+、AlO2-的浓度与溶液pH的关系如上图所示。为测定达喜的组成,进行了下列实验:
① 取达喜6.02 g研碎,缓慢加入2.00 mol·L-1盐酸使其溶解,当加入盐酸85.00 mL时开始产生CO2,加入盐酸至90.00 mL时正好反应完全。
② 在①所得溶液中加入适量的 (填“氨水”、“氢氧化铝”或“氯化镁”)以调节溶液的pH至5.0~7.8,使有关离子完全沉淀。
③ 将②产生的全部沉淀过滤、洗涤,灼烧至恒重,称量为1.02 g。确定达喜的化学式为___________,并简要写出计算过程。
高三化学填空题简单题查看答案及解析
-
(12分)达喜[AlaMgb(OH)c(CO3)d·xH2O]常用于中和胃酸。
(1)1 mol达喜与足量的盐酸完全反应后生成水的物质的量为________(用含x等字母的代数式表示)。
(2)达喜化学式中a、b、c、d的关系为a+b________c+d(填“>”、“=”或“<”)。
(3)已知在常温下溶液中Al3+、Mg2+、AlO2-的浓度与溶液pH的关系如图所示。为测定达喜的组成,进行了下列实验:

①取达喜6.02 g研碎,缓慢加入2.00 mol·L-1盐酸使其溶解,当加入盐酸85.00 mL时开始产生CO2,加入盐酸至90.00 mL时正好反应完全。
②在①所得溶液中加入适量的________(填“氨水”、“氢氧化铝”或“氯化镁”)以调节溶液的pH至5.0~7.0,使有关离子完全沉淀。
③将②产生的全部沉淀过滤、洗涤,灼烧至恒重,称量为1.02 g。
请通过计算确定达喜的化学式(写出计算过程)。
高三化学计算题极难题查看答案及解析
-
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·eH2O]在一定条件下的转化如下图所示,下列说法不正确的是
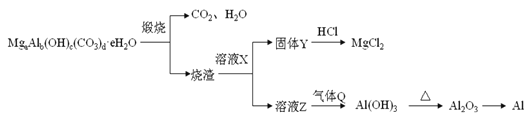
A. Q可能为NH3 B. a、b、c、d符合关系式:2a+3b=c+2d
C. X可能为NaOH D. 碱式碳酸铝镁医疗上可用做抗酸剂,工业上可用做阻燃剂
高三化学单选题中等难度题查看答案及解析
-
用沉淀法测定NaHCO3和K2CO3混合物的组成.实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液500mL,每次实验均充分反应.实验记录如下:
回答下列问题:实验次数 样品质量/g 沉淀质量/g 1 1.716 2.758 2 2.574 ______ 3 3.432 5.516 4 4.290 5.516
(1)第2次实验中产生沉淀质量是多少,将结果填入表格空白处.
(2)Ba(OH)2溶液中溶质的物质的量浓度是______.
(3)第2次实验样品中NaHCO3的物质的量是______.
(4)室温下取第2组实验所得溶液体积的,加水配成500mL溶液,求稀释以后溶液的pH?(要求书写计算过程)
高三化学解答题中等难度题查看答案及解析
-
碱式碳酸铋片[主要成分(BiO)2CO3]可用于治疗慢性胃炎及缓解胃酸过多引起的胃病。由菱铋矿(主要成分为nBi2O3·mCO2·H2O,含杂质SiO2、CuS等)制备(BiO)2CO3的一种工艺如图:
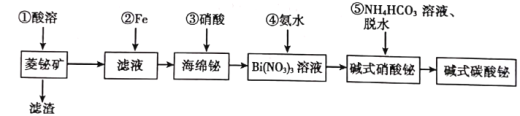
试回答下列问题:
(1)为提高①的“酸溶”速率,可以采取的措施是__________(任写一种)。
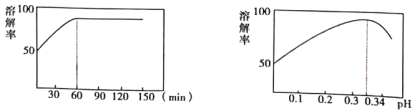
(2)①中酸溶解率与接触时间及溶液的pH之间的关系如图,据此分析,“酸溶”的最佳条件为__________;滤渣的主要成分是__________。
(3)“酸溶”后溶液必须保持强酸性,以防止铋元素流失,原理是__________。
(4)②中得到“海绵铋”的离子方程式为__________。
(5)④中反应的化学反应方程式为__________。
(6)25℃时,向浓度均为0.1mol·L-1的Fe2+、Cu2+、Bi3+的混合溶液中滴加Na2S溶液,当Fe2+恰好沉淀完全时,所得溶液c(Cu2+):c(Bi3+)=__________。(忽略Na2S溶液所带来的体积变化)。
资料:①有关溶度积数据见表:
难溶物质
FeS
CuS
Bi2S3
Ksp(25℃)
6.3×10-18
6.3×10-36
1.6×10-20
②溶液中的离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。
高三化学工业流程困难题查看答案及解析