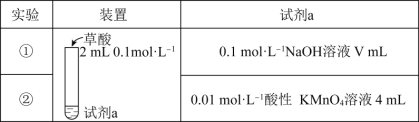-
已知草酸为二元弱酸,在25℃时,草酸的两步电离常数为: Ka1=5.0×10-2,Ka2=m。实验测得在该温度下改变0.1mol· L-1的H2C2O4溶液的pH 值时,溶液中主要微粒的物质的量分数δ(X) 随pH值的变化如图所示[已知:①δ( H2C2O4)= 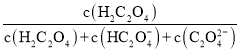 ②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
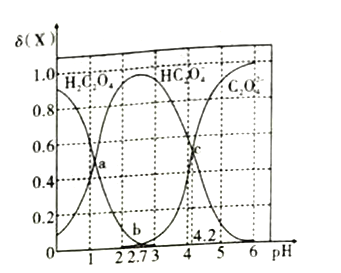
A. 在a点,溶液对应的pH值为1.3 B. pH= 2.8 时,c(HC2O4-)>c(C2O42-)+c(H2C2O4)
C. pH=4.2时,c(HC2O4-)=c(C2O42-)=c(H+) D. lgKa2=-4.2
-
已知,25 ℃时几种弱酸的电离常数如表所示:
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 | Ka1=4.3×10-7 Ka2=5.6×10-11 | H2C2O4 (草酸) | Ka1=5.9×10-2 Ka2=6.4×10-5 |
| H3PO4 | Ka1=7.1×10-3 Ka2=6.3×10-8 Ka3=4.2×10-13 | H3C6H5O7 (柠檬酸) | Ka1=7.4×10-4 Ka2=1.7×10-5 Ka3=4.0×10-7 |
下列有关推断正确的是( )
A. 溶液pH的大小关系为K3PO4>K2HPO4>KH2PO4
B. 在Na2CO3溶液中存在:c(OH-)- c(H+)=c(HCO3-)+ c(H2CO3)
C. 等浓度的NaHCO3、NaHC2O4溶液中前者pH较大
D. H3C6H5O7与Na2CO3溶液反应的产物为Na3C6H5O7、CO2、H2O
-
探究草酸(H2C2O4)的性质,室温下进行以下两组实验:(已知:室温下,H2C2O4的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5)
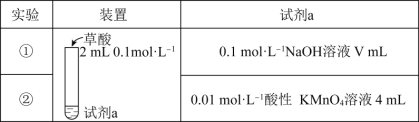
下列有关实验说法正确的是( )
A.若实验①中V=2,则混合后溶液中:c(C2O42-)>c(H2C2O4)
B.若实验①中V=4,则混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-)
C.实验②反应的离子方程式为5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O
D.若实验②测得KMnO4溶液的褪色时间为40s,则这段时间内的平均反应速率v(KMnO4)=2.5×10-4mol•L-1•s-1
-
已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25 ℃) | Ka=1.8×10-5 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
请回答下列问题:
(1)25 ℃时,在某二元酸 H2A 溶液中存在的所有微粒为:H+、OH-、HA-、A2-、H2O,写出 H2A 的 电离方程式_____。
(2)25 ℃时,在 0.5 mol·L-1 的醋酸溶液中由醋酸电离出的[H+]约是_________,是该溶液 中由水电离出的[H+]的_____倍,醋酸的电离度为_____(填百分数)
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:______________________________。
(4)25 ℃时,CH3COOH 与 CH3COONa 的混合溶液,若测得混合液 pH=6,则溶液中[CH3COO-]-[Na+]=_____(填准确数值)。
(5)25 ℃时,将 a mol·L-1 的醋酸与 b mol·L-1 氢氧化钠溶液等体积混合,反应后溶液恰好显中性, 用 a、b 表示醋酸的电离常数为_____。
-
二元弱酸是分步电离的,25时碳酸和草酸的 如下表:
如下表:
| H2CO3 | Ka1=4.3×10-7 | H2C2O4 | Ka1=5.6×10-2 |
| Ka2=5.6×10-11 | Ka2=5.42×10-5 |
(1)设有下列四种溶液:
A.0.1 mol/L的Na2C2O4溶液 B.0.1 mol/L的NaHC2O4溶液
C.0.1 mol/L的Na2CO3溶液 D.0.1 mol/L的NaHCO3溶液
其中,c(H+)最大的是_________,c(OH-)最大的是_________ 。
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插人pH传感器,测得pH变化曲线如图所示。
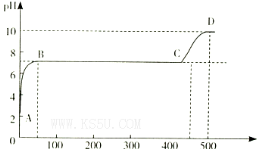
刚开始滴人碳酸钠溶液时发生反应的离子方程式为_________,BC段发生反应的离子方程式为_____,D点时混合溶液中由水电离产生的c(H+)=_________ mol/L。
-
二元弱酸是分步电离的,25时碳酸和草酸的 如下表:
如下表:
| H2CO3 | Ka1=4.3×10-7 | H2C2O4 | Ka1=5.6×10-2 |
| Ka2=5.6×10-11 | Ka2=5.42×10-5 |
(l)设有下列四种溶液:
A.0.1 mol/L的Na2C2O4溶液 B.0.1 mol/L的NaHC2O4溶液
C.0.1 mol/L的Na2CO3溶液 D.0.1 mol/L的NaHCO3溶液
其中,c(H+)最大的是_________,c(OH-)最大的是_________ 。
(2)某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示。
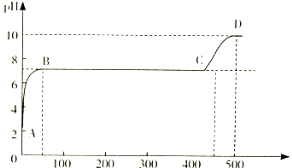
刚开始滴入碳酸钠溶液时发生反应的离子方程式为 ,BC段发生反应的离子方程式为 ,D点时混合溶液中由水电离产生的c(H+)=_________ mol/L。
-
已知草酸(H2C2O4)为二元弱酸,25℃时,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。用NaOH溶液滴定草酸氢钾(KHC2O4)溶液,混合溶液的相对导电能力随加入NaOH体积的变化如图所示(忽略混合时溶液温度的变化),其中N点为反应终点。下列有关描述中正确的是
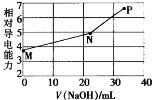
A.M点粒子浓度:c(K+)>c( )>c(
)>c( )>c(H2C2O4)
)>c(H2C2O4)
B.N点时存在:c(Na+)+c(K+)<2c( )+2c(
)+2c( )
)
C.从N点到P点的过程中溶液中一定存在:c(Na+)+c(H2C2O4)>c( )
)
D.水的电离程度大小顺序:P>N>M
-
草酸(H2C2O4)是生物体的一种代谢产物,广泛分布于植物、动物和真菌中,并在不同的生物体中发挥着不同的作用。
(Ⅰ)草酸是一种二元有机弱酸,具有还原性。
(1)已知:25℃时,草酸的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5;碳酸(H2CO3)的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11。
①向Na2CO3溶液中加入少量草酸溶液,发生反应的离子方程式为___。
②常温下,用0.01mol•L-1的NaOH标准溶液滴定20mL0.01mol•L-1的草酸溶液,滴定曲线如图所示。
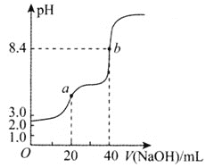
a点溶液呈___(填“酸”“碱”或“中”)性;b点溶液中各离子浓度的大小关系为___。
(2)酸性KMnO4溶液可将草酸氧化为CO2,还原产物为Mn2+,该反应的离子方程式为___。
(Ⅱ)草酸分解生成CO和CO2,以CO或CO2,为原料均可制得甲醇。
(3)已知:i.2H2(g)+O2(g)=2H2O(l) ΔH1=-285.0kJ·mol-1;ii.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为___。
O2(g)=CO2(g)+2H2O(l) ΔH2=-726.0kJ·mol-1。则二氧化碳与氢气反应生成液态甲醇和液态水(该反应为可逆反应)的热化学方程式为___。
(4)利用CO与H2合成甲醇的反应原理为CO(g)+2H2(g)⇌CH3OH(g)。现向一容积可变的密闭容器中充入10molCO(g)和20molH2(g)发生上述反应,CO的平衡转化率(α)与温度(T)、压强(p)的变化关系如图所示。

①该反应为___(填“放热”或“吸热”)反应,A、B、C三点的平衡常数K(A)、K(B)、K(C)的大小关系为___,压强的大小关系为p1___(填“大于”“小于”或“等于”)p2。
②若A点时,保持容器容积和温度不变,向容器中再充入2molCO(g)、4molH2(g)和2molCH3OH(g),则v正___(填“>”或“<”)v逆。
-
研究含硒工业废水的处理工艺,对控制水体中硒超标具有重要意义。
(1)已知:H2SeO3为二元弱酸,Ka1(H2SeO3)=3.5×10-3,Ka2(H2SeO3)=5.0×10-8。用离子交换树脂处理含Na2SeO3浓度较高的废水时,发生的交换反应为SeO32-+2RCl=R2SeO3+2Cl- (R为离子交换树脂的树脂骨架)。经离子交换法处理后,废水的pH将________(填“增大”“减小”或“不变”)。
(2)木炭包覆纳米零价铁除硒法是一种改良的含硒废水处理方法。
①以木屑和FeCl3·6H2O为原料,在N2氛围中迅速升温至600 ℃,保持2 h,过程中木屑先转化为木炭,最终制得木炭包覆纳米零价铁。制备木炭包覆纳米零价铁过程中,木炭的作用有吸附和________________________________________。
②木炭包覆纳米零价铁在碱性废水中形成许多微电池,加速SeO32-的还原过程。SeO32-在微电池正极上转化为单质Se,其电极反应式为________。
(3) 绿锈[FeaⅡFebⅡ(OH)cXd](X代表阴离子,Ⅱ、Ⅲ表示铁元素的价态)中铁元素以结构态和游离态两种形式存在。由于结构态的双金属氢氧化物层间存在较大的空隙,形成了巨大的比表面积,同时结构态的FeⅡ还原能力优于游离态的FeⅡ,使得绿锈成为一种良好的除硒剂。
①结构态的绿锈具有优异的吸附性能,而且游离态的Fe3+还易水解生成Fe(OH)3胶体进一步吸附SeO32-。写出Fe3+水解的离子方程式:________。
②不同FeⅡ/FeⅢ组成的绿锈对SeO32-去除效果的影响结果如图1所示。随着绿锈组成中FeⅡ/FeⅢ比值的增大,绿锈的除硒效果先减小后增大的原因可能是________。
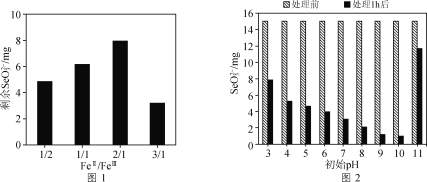
③废水的初始pH会对绿锈去除SeO32-的效果产生影响,关系如图2所示。当初始pH增大至11时,SeO32-的去除效果突然迅速减小的原因是________。
-
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO +2HClO
+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2 CO =SO
=SO +2HCO3-
+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
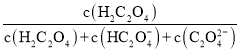 ②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )
②1g5=0.7;③图中b点对应的pH值为2.7]。则下列说法不正确的是( )