-
【化学--选修物质结构与性质】
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
| 元素 | A | B | C | D |
性质
结构
信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104s2 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)写出B原子的基态电子排布式______.
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”),其原因是______.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点______(填“高”或“低”);D元素在形成最简单氢化物时所采取的杂化类型是______.
(4)A、B两元素第一电离能______>______.(填元素符号)
(5)C元素的原子能形成多种配合物.形成配合物的条件是:一方能够提供孤对电子,另一方______.
-
【化学选修3:物质结构与性质】
四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
| 元素 | A | B | C | D |
| 性质 结构信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为________(用元素符号表示);试解释其原因________。
(2)B元素的低价氧化物分子中心原子的杂化方式为________,B元素的最高价氧化物分子VSEPR模型为________,B元素与D元素形成分子空间构型为________。
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点________(填“高”或“低”),其原因是________。
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为________;后一现象的化学反应方程式为________。
(5)某同学根据上述信息,推断A基态原子的核外电子排布为: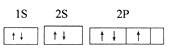 该同学所画的电子排布图违背了___________________。
该同学所画的电子排布图违背了___________________。
(6)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为________________,C晶体的密度为______________g•cm-3(要求写表达式,可以不化简)。
-
【化学选修2:物质结构与性质】四种常见元素的性质或结构信息如下表,根据信息回答有关问题。
| 元素 | A | B | C | D |
| 性质或结 构信息 | 原子核外有两个电子层,最外层有3个未成对电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为:[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中一种是冶炼金属工业的常用还原剂 |
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为 (用元素符号表示);试解释原因 。
(2)B元素的低价氧化物分子中心原子的杂化方式为 ,B元素的最高价氧化物分子的VSEPR构型为 ;B元素与D元素形成分子空间构型为 ;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点 (填“高”或“低”),其原因是 ;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为 ;后一现象的离子方程式为: 。
(5)C晶体的堆积方式如图所示,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为 ,C晶体的密度为 g·cm—3(要求写表达式,可以不简化)。
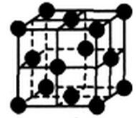
-
(选考)【选修3:物质结构与性质】(10分)
四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
| 元素 | A | B | C | D |
| 性质 结构 信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为 (用元素符号表示);
(2)B元素的低价氧化物分子中心原子的杂化方式为 ,B元素与D元素形成分子空间构型为 ;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点 (填“高”或“低”),其原因是______________________________________;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,
观察到的现象为 ;
(5)C晶体的堆积方式如图所示,设C原子半径为r cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为_______,C晶体的密度为 g·cm-3(要求写表达式,可以不化简)。

-
[化学--物质结构与性质]
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
| 元素 | A | B | C | D |
结构性质
信息 | 基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 | 原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有2对成对的p电子 | 其原子序数比A、B、C三种元素原子的质子数总和还少1,有+1、+2两种常见化合价 |
(1)写出D原子的外围电子排布式______,A、B、C、D四种元素的第一电离能最小的是______(用元素符号表示).
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”).
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
| A-O | A=O | F-O | F=O |
| 键能(KJ/mol) | 360 | 803 | 464 | 640 |
在A和O之间通过双键形成AO2分子,而F和O则不能和A那样形成有限分子,原因是______.
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是______(填序号).a.离子键 b.极性键c.非极性键d.配位键 e.金属键
(5)下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.
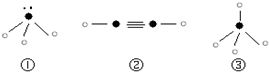
则在以上分子中,中心原子采用sp3杂化形成化学键的是______(填序号);在②的分子中有______个σ键和______个π键.
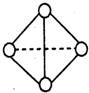
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=______KJ/mol.
-
物质结构
四种常见元素的性质或结构信息如下表.试根据信息回答有关问题.
| 元素 | A | B | C | D |
性质
结构
信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,
有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(1)写出B原子的电子排布式______.
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”),其原因是______.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点______(填“高”或“低”),其原因______.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为______,简要描述该配合物中化学键的成键情况______.
(5)下列分子结构图中的“ ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
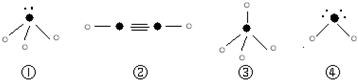
则在以上分子中,中心原子采用sp3杂化形成化学键的是______(填写序号);在②的分子中有______个σ键和______个π键.
-
四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
| 元素 | A | B | C | D |
| 性质、结构信息 | 价电子数为5的短周期元素;该元素形成的双原子分子一般情况下很稳定。 | 基态原子的M层有1对成对的p电子。 | 第三周期中电离能最小的元素。 | 原子最外电子层上s电子数等于p电子数。 其一种单质为自然界中硬度最大的非金属单质。 |
(1)写出元素B基态原子的电子排布图 。
(2)元素A形成的气态氢化物的空间构型为 。(3)元素B和C形成的化合物的电子式是 。
(4)元素D形成的化合物D2H2属于 (填“极性”或“非极性”)分子。
(5)A、C、D三种元素的电负性由小到大的顺序是_________(用元素符号表示)。
-
【选修3:物质结构与性质】(13分)原子序数逐渐增大的元素A,B,C,D,E,F的有关信息如下:

根据以上表格信息回答:
(1)元素F在周期表中的位置是 ,E形成的低价离子的电子排布式为 。
(2)A、C的氢化放沸点较高的是(用所形成的氢化物表示) ,A,B,C的第一电离能大小顺序是(用元素符号表示) .
(3)A与氢元素形成的A2H2含有的 键数目之比为 。
键数目之比为 。
(4)KCl的晶胞如图:则该晶胞中含有K+为 个.已知晶胞参数为:629.8pm(lpm=10-12m),求KCl晶体的密度为 g/cm3(只写出表达式,不要求计算结果).
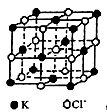
(5)用惰性电极电解FCl2溶液时,在阴极除了析出红色固体外,还析出白色固体,经检验白色固体为FCl。请写出析出白色固体的阴极反应式 .
-
[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
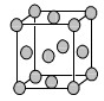
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
-
[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
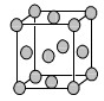
A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
 该同学所画的电子排布图违背了___________________。
该同学所画的电子排布图违背了___________________。







