实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:
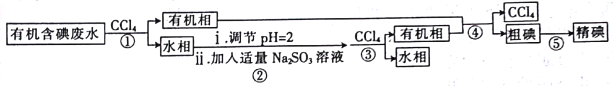
已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行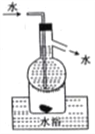
高三化学单选题困难题
实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:

已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行
高三化学单选题困难题
实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:
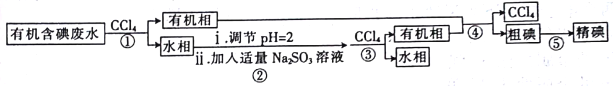
已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行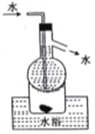
高三化学单选题困难题查看答案及解析
实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:
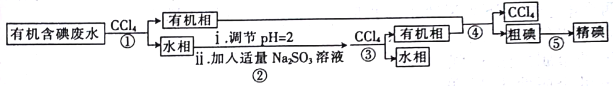
已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行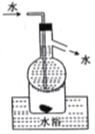
高三化学选择题困难题查看答案及解析
实验室用有机含碘(主要以I2和IO3-的形式存在)废水制备单质碘的实验流程如下:

已知:碘的熔点为113℃,但固态的碘可以不经过熔化直接升华。下列说法错误的是
A. 操作①和③中的有机相从分液漏斗下端放出
B. 操作②中发生反应的离子方程式为2IO3- +5SO32-+2H+=I2+5SO42-十H2O
C. 操作④中用到的玻璃仪器仅需温度计、球形冷凝管、酒精灯、接引管及锥形瓶
D. 操作⑤可用如图所示的水浴装置进行
高三化学单选题困难题查看答案及解析
实验室用有机含碘主要以I2和IO3-的形式存在
废水制备单质碘的实验流程如下:
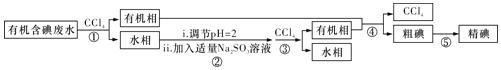
已知:Ⅰ.碘的熔点为113℃,但固态的碘可以不经过熔化直接升华;
Ⅱ.粗碘中含有少量的硫酸钠杂质。
下列说法正确的是( )
A.操作②中发生反应的离子方程式为IO3-+3SO32-=I-+3SO42-
B.操作①和③中的有机相从分液漏斗上端倒出
C.操作④为过滤
D.操作⑤可用如图所示的水浴装置进行
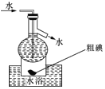
高三化学单选题中等难度题查看答案及解析
实验室用有机含碘主要以
和
的形式存在
废水制备单质碘的实验流程如下:
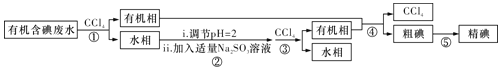
已知:Ⅰ碘的熔点为
,但固态的碘可以不经过熔化直接升华;
Ⅱ粗碘中含有少量的
杂质。
下列说法正确的是( )
A.操作中发生反应的离子方程式为
B.操作和
中的有机相从分液漏斗上端倒出
C.操作为过滤
D.操作可用如图所示的水浴装置进行
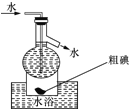
高三化学单选题中等难度题查看答案及解析
下列说法不正确的是
A.固态氨基酸主要以内盐形式存在,熔点较高,易溶于有机溶剂
B.可用苯将含苯酚废水中的苯酚萃取出来
C.溴苯中混有的少量溴单质,可加入足量的 10﹪NaOH 溶液,经分液除去
D.用新制氢氧化铜悬浊液(必要时可加热)能鉴别丙三醇、乙醇、乙醛和乙酸
高三化学单选题中等难度题查看答案及解析
实验室用软锰矿(主要成分为MnO2)和黄铁矿(主要成分为FeS2)为原料制取Mn2O3和单质硫,其实验流程如下:
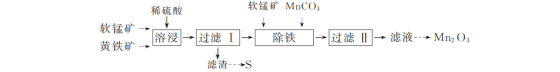
已知:① 在碱性条件下,二价锰以Mn(OH)2形式稳定存在,三价锰以MnOOH形式稳定存在。Mn(OH)2和MnOOH均难溶于水和碱性溶液。
②无水MnSO4晶体熔点700 ℃,在不同温度下它和MnOOH固体受热发生分【解析】
4MnSO42Mn2O3+4SO2↑+O2↑;2MnOOH
Mn2O3+H2O↑。
(1)溶浸过程中生成MnSO4、Fe2(SO4)3及单质S,该反应的化学方程式为________。
(2)室温下,为使杂质离子浓度小于1×10-6mol·L-1,除铁步骤中需调节溶液pH范围为________(已知:Ksp[Fe(OH)2]=1.0×10-16、Ksp[Fe(OH)3]=1.0×10-39,pH=7.1时Mn(OH)2开始沉淀)
(3)为提高Mn2O3的产率,流程中两次过滤操作后均需对滤渣进行洗涤,并________。
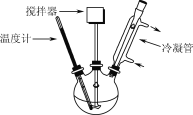
(4)(NH4)2S溶液浸取过滤Ⅰ得到的滤渣时发生反应:(NH4)2S +xS(NH4)2Sx+1,单质硫转化为多硫化铵[(NH4)2Sx+1]转移到液相中。实验时采用过量的饱和(NH4)2S溶液浸取的目的是________。将多硫化铵溶液置于如图所示的装置中,控制在90 ℃条件下分解,单质硫的提取率可达98%。实验中适宜的加热方式为____________________。
(5)请补充完整由MnSO4溶液制备较纯净Mn2O3的实验方案:向MnSO4溶液中________,72 h后得到产品Mn2O3。(须使用的试剂:0.2 mol·L-1氨水、3%H2O2溶液、BaCl2溶液、热水)
高三化学工业流程中等难度题查看答案及解析
工业上利用含有一定浓度的I2和CuSO4溶液的工业废水制备饲料添加剂Ca(IO3)2,其生产流程如下:
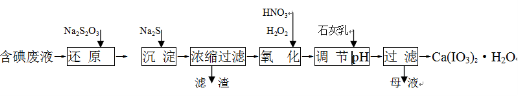
已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3—>H2O2
(1)“还原”过程中主要反应的化学方程式为:2Na2S2O3+I2 = + 2NaI。
(2)在还原过程还伴随有CuI生成,写出加入Na2S的离子反应方程式 。
(3)在氧化过程中先加入H2O2再加入浓硝酸,而不直接加入浓硝酸的目的是 。
(4)加入的石灰乳在溶液中反应而得到Ca(IO3)2,则要调节pH至 (填“酸性” 或“中性”或“碱性”),原因是 。
(5)Ca(IO3)2也可用电化学氧化法制取:先充分电解KI溶液,然后在电解后的溶液中加入CaCl2,最后过滤得到Ca(IO3)2。写出电解时阳极发生的电极反应方程式 ,用该方法制取Ca(IO3)2,每1kg碘化钾理论上可生产纯度为97.8%Ca(IO3)2的质量为 ____kg(计算结果保留3位有效数字)。
高三化学填空题极难题查看答案及解析
某化学实验兴趣小组的同学从海带中提取碘单质的实验流程图如下:

依据实验下列说法不正确的是( )
A. 从上述实验可以得出海带中含有可溶性的含碘化合物
B. 步骤⑤中可能发生的反应为:5I- + IO3- +6H+ ===3I2 +3H2O
C. 若步骤④中用CCl4做萃取剂,步骤⑥应取上层溶液得到后续的混合物C
D. 整个过程中的操作是利用了物质的溶解性实现了碘元素的富集、分离与提纯
高三化学单选题中等难度题查看答案及解析
利用某冶金行业产生的废渣(主要含,还有少量
、
等杂质)可以制备
,生产流程如下:
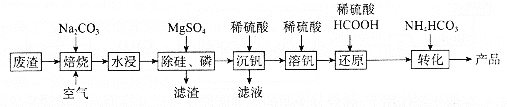
已知:微溶于水、溶于碱生成
(加热生成
),具有强氧化性。向
溶液中加酸,不同
对应的主要存在形式如表:
| | | 10.6~12 | 约8.4 | 3~8 | 约2 | <1 |
| 存在形式 | | | | | | |
回答下列问题:
(1)“焙烧”后V元素转化为,
元素转化为________(写化学式)。
(2)欲除尽磷元素(即),最终溶液中
的浓度至少为________
(已知
)。
(3)“沉钒”过程中,由8.5到5.0发生反应的离子方程式为________;最终需要控制
约为________;“沉钒”最终得到的主要含钒物质是________(写化学式)。
(4)“还原”和“转化”过程中主要反应的离子方程式分为________、________。
高三化学工业流程中等难度题查看答案及解析