-
光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为 ,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
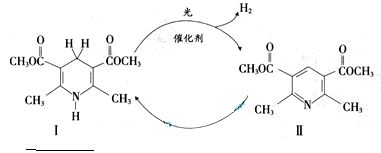

(1)化合物II的分子式为______________。
 (2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
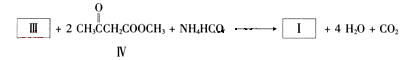
 化合物III的名称是________________。
化合物III的名称是________________。
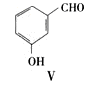
(3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为___________________。

(4)下列说法正确的是_____________(填字母)
 A. 化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛
A. 化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛
B. 化合物I具有还原性;II具有氧化性,但能被酸性高锰酸钾溶液氧化
 C. 化合物I、II、IV都可发生水解反应
C. 化合物I、II、IV都可发生水解反应
D. 化合物V遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应
 (5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为_________________;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有_________________种。
(5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为_________________;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有_________________种。

-
光催化制氢是化学研究的热点之一.科学家利用含有呲啶环(呲啶的结构式为
 ,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
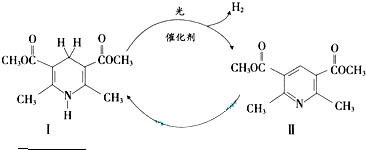
(1)化合物II的分子式为______.
(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);

化合物III的名称是______.
(3)用化合物V(结构式见右图) 代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为______.
代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为______.
(4)下列说法正确的是______(填字母)
A.化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛
B.化合物I具有还原性;II具有氧化性,但能被酸性高锰酸钾溶液氧化
C.化合物I、II、IV都可发生水解反应
D.化合物V遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应
(5)呲啶甲酸酯可作为金属离子的萃取剂.2-呲啶甲酸正丁酯(VI)的结构式见右图,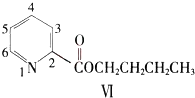 其合成原料2-呲啶甲酸的结构式为______;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有______种.
其合成原料2-呲啶甲酸的结构式为______;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有______种.
-
制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。一定条件下,如图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其他有机物生成)。电流效率=(生成目标产物消耗的电子数/转移的电子总数)×100%,则下列说法错误的是( )
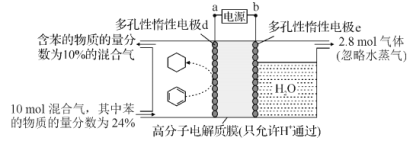
A.电子移动方向为:a→d;e→b
B.d电极反应式为C6H6+6H++6e-=C6H12
C.该储氢装置的电流效率明显小于100%,其原因可能是除目标产物外,还有H2生成
D.由图中数据可知,此装置的电流效率约为32.1%
-
研究氮及其化合物的性质及转化,对研究自然界中氮的循环有着重大的意义。
I.合成氨反应历程研究
(1)科学家研究利用铁触媒合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
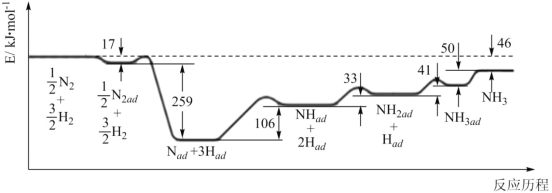
由图可知合成氨反应N2(g)+3H2(g) 2NH3(g)的∆H=__kJ·mol-1。该历程中速率最慢的一步的化学方程式为__。
2NH3(g)的∆H=__kJ·mol-1。该历程中速率最慢的一步的化学方程式为__。
II.对NO与O2反应的研究
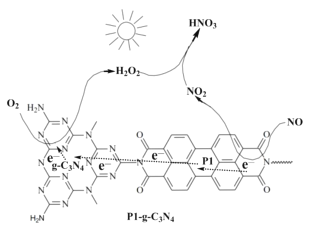
(2)用Pl-g-C3N4光催化氧化法脱除NO的过程如图所示。在酸性水溶液中,光催化脱除原理和电化学反应原理类似。g-C3N4端的反应为O2+2H++2e-=H2O2,则Pl端的反应为__。
(3)在一定条件下,将2molNO和1molO2通入恒容密闭容器中进行反应。在不同温度下,测得平衡时体系中NO、O2、NO2的物质的量与温度的关系如图所示。
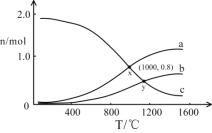
(已知:容器中发生两个反应2NO(g)+O2(g) 2NO2(g) ∆H˂0和2NO2(g)
2NO2(g) ∆H˂0和2NO2(g) N2O4(g) ∆H˂0)
N2O4(g) ∆H˂0)
①曲线c代表__的物质的量与温度的关系,x点对应的O2的转化率为__。
②下列说法正确的是__。
A.2NO+O2 2NO2的平衡常数:x点>y点
2NO2的平衡常数:x点>y点
B.y点时2NO+O2 2NO2的反应速率:v正<v逆
2NO2的反应速率:v正<v逆
C.x点对应的NO的物质的量分数为
D.400~1200℃时,随温度升高,N2O4体积分数不断增大
III.对NO与Cl2物反应及产物NOCl(亚硝酰氯)的研究
(4)NOCl可由NO与Cl2制得,化学方程式为2NO(g)+Cl2(g) 2NOCl ΔH=-111kJ/mol。在295K时,其反应物浓度与反应速率关系的数据如下:
2NOCl ΔH=-111kJ/mol。在295K时,其反应物浓度与反应速率关系的数据如下:
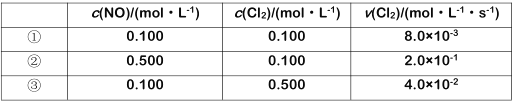
反应物浓度与反应速率关系式为v(Cl2)=k·cm(NO)cn(Cl2),式中速率常数k=Ae-Ea/RT,其中Ea为活化能,A、R均为大于0的常数,T为温度)。则此条件下k的数值为__,若要使k增大,可采取的措施有__、__。
-
铁—末端亚胺基物种被认为是铁催化的烯烃氮杂环丙烷化、C—H键胺化反应以及铁促进的由氮气分子到含氮化合物的转化反应中的关键中间体。对这类活性金属配合物的合成、谱学表征和反应性质的研究一直是化学家们关注的重点。我国科学家成功实现了首例两配位的二价铁—末端亚胺基配合物的合成。回答下列有关问题。
(1)Fe2+的价电子排布式___。
(2)1molNH4BF4(氟硼酸铵)中含有的配位键数是___。
(3)pH=6时,EDTA可滴定溶液中Fe2+的含量,EDTA的结构如图所示。

①结构中电负性最大的元素是___,其中C、N原子的杂化形式分别为___、___。
②EDTA可与多种金属阳离子形成稳定配合物的原因是___。
(4)我国科学家近年制备了热动力学稳定的氦-钠化合物,其晶胞结构如图所示。

①该化合物的化学式为___。
②其晶胞参数为a=395pm,晶体密度为___g/cm3(NA表示阿伏加德罗常数数值,列出计算式即可)
-
氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s)  Fe3O4(s)+4H2(g) △H=akJ/mol (I)
Fe3O4(s)+4H2(g) △H=akJ/mol (I)
2Fe3O4(s)  6FeO(s)+O2(g) △H=bkJ/mol (II)
6FeO(s)+O2(g) △H=bkJ/mol (II)
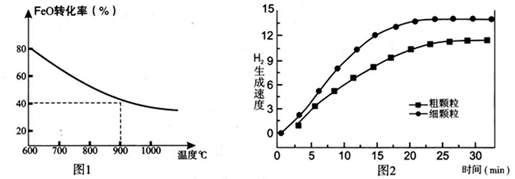
下列坐标图分别表示FeO的转化率(图-1 )和一定温度时,H2出生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图-2)。
(1)反应:2H2O(g)=2H2(g)+O2(g) △H=________(用含a、b代数式表示);
(2)上述反应b>0,要使该制氢方案有实际意义,从能源利用及成本的角度考虑,实现反 应II可采用的方案是:________;
(3)900°C时,在两个体积均为2.0L密闭容器中分别投人0.60molFeO和0.20mol H2O(g)甲容器用细颗粒FeO、乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是:________;
②细颗粒FeO时H2O(g)的转化率比用粗颗粒FeO时 H2O(g)的转化率________ (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计箅过程,保留两位有效数字)。
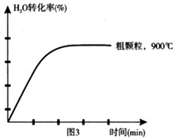
(4)在下列坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注)。
-
(16分)氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。 利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) Fe3O4(s) + H2(g) △H=a KJ/mol (Ⅰ)
Fe3O4(s) + H2(g) △H=a KJ/mol (Ⅰ)
2Fe3O4(s)=6FeO(s) + O2(g) △H=b KJ/mol (Ⅱ)
下列坐标图分别表示FeO的转化率(图1)和一定温度时,H2生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图2)。
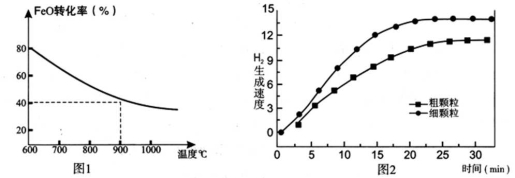
(1)反应:2H2O(g)=2H2(g) + O2(g) ΔH= (用含a、b代数式表示);
(2)在上述循环制氢的过程中FeO的作用是: ;
(3)900°C时,在两个体积均为2L密闭容器中分别投入0.60molFeO和0.20mol H2O(g),甲容器用细颗粒FeO,乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②用细颗粒FeO时,H2O (g)的转化率比用粗颗粒FeO时H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计算过程)。
(4)在坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注):
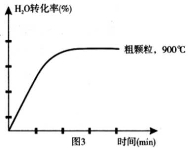
-
中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如下图所示。
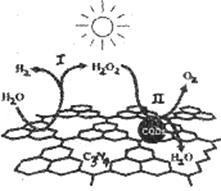
下列说法不正确的是
A. 该催化反应实现了太阳能向化学能的转化
B. 阶段I中,H2O2是氧化产物
C. 每生成1molO2,阶段II中转移电子2 mol
D. 反应的两个阶段均为吸热过程
-
中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如下图所示。
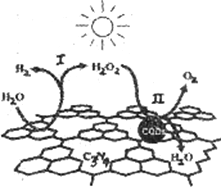
下列说法不正确的是
A. 该催化反应实现了太阳能向化学能的转化
B. 阶段I中,H2O2是氧化产物
C. 每生成1molO2,阶段II中转移电子2 mol
D. 反应的两个阶段均为吸热过程
-
氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。
(1)已知;  (g)+H2(g)→
(g)+H2(g)→ (g) ∆H=-119.6kJ/mol
(g) ∆H=-119.6kJ/mol
 (g)+2H2(g)→
(g)+2H2(g)→ (g) ∆H=-237.1kJ/mol
(g) ∆H=-237.1kJ/mol
 (g)+3H2(g)→
(g)+3H2(g)→ (g) ∆H=-208.4kJ/mol
(g) ∆H=-208.4kJ/mol
请求出 (g)+H2(g)→
(g)+H2(g)→ (g) ∆H=________kJ/mol
(g) ∆H=________kJ/mol
(2)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。
 (g)
(g)
 (g)+3H2(g)
(g)+3H2(g)
在某温度下,向恒容容器中加入环已烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=_______(用含a、b的关系式表达)。
(3)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。

①实现有机物储氢的电极是__________;A 正极 B 负极 C 阴极 D 阳极
其电极反应方程为:___________。
②实验研究表明,当外加电压超过一定值以后,发现电极D产物中苯(g)的体积分数随着电压的增大而减小,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是__________。已知单质气体为2 mol,求此装置的电流效率η=__________。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):

(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
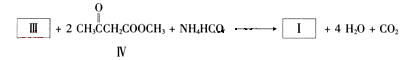
化合物III的名称是________________。

A. 化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛
C. 化合物I、II、IV都可发生水解反应
(5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为_________________;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有_________________种。



 其合成原料2-呲啶甲酸的结构式为______;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有______种.
其合成原料2-呲啶甲酸的结构式为______;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有______种. 












