25℃时,用0.10 mol • L-1的氨水滴定10.00 mL a mol • L-1的盐酸,溶液的pH与氨水的体积(V)的关系如图所示。已知:N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法正确的是
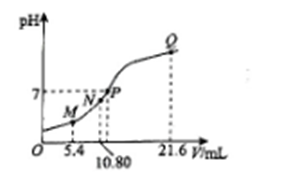
A. M点溶液中存在:c(H+)=c(OH-)+2c(NH3·H2O)+ c(NH4+)
B. N、Q两点溶液中NH3 • H2O的电离常数:N<Q
C. P 点氨水过量,c(NH4+)> c(Cl-)
D. a=0.054
高三化学选择题困难题
25℃时,用0.10 mol • L-1的氨水滴定10.00 mL a mol • L-1的盐酸,溶液的pH与氨水的体积(V)的关系如图所示。已知:N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法正确的是

A. M点溶液中存在:c(H+)=c(OH-)+2c(NH3·H2O)+ c(NH4+)
B. N、Q两点溶液中NH3 • H2O的电离常数:N<Q
C. P 点氨水过量,c(NH4+)> c(Cl-)
D. a=0.054
高三化学选择题困难题
25℃时,用0.10 mol • L-1的氨水滴定10.00 mL a mol • L-1的盐酸,溶液的pH与氨水的体积(V)的关系如图所示。已知:N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法正确的是

A. M点溶液中存在:c(H+)=c(OH-)+2c(NH3·H2O)+ c(NH4+)
B. N、Q两点溶液中NH3 • H2O的电离常数:N<Q
C. P 点氨水过量,c(NH4+)> c(Cl-)
D. a=0.054
高三化学选择题困难题查看答案及解析
25℃时,用0.10 mol • L-1的氨水滴定10.00 mL a mol • L-1的盐酸,溶液的pH与氨水的体积(V)的关系如图所示。已知:N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法正确的是
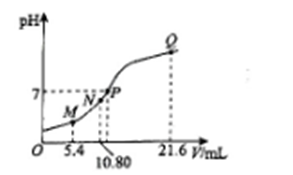
A. M点溶液中存在:c(H+)=c(OH-)+2c(NH3·H2O)+ c(NH4+)
B. N、Q两点溶液中NH3 • H2O的电离常数:N<Q
C. P 点氨水过量,c(NH4+)> c(Cl-)
D. a=0.054
高三化学选择题困难题查看答案及解析
25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL a mol·L-1的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。已知N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法不正确的是( )
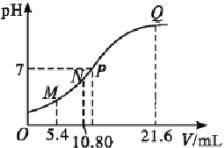
A. 图上四点分子种类相同
B. a=0.1
C. N、Q两点的 :N=Q
D. P点溶液中存在:c(Cl-)=c(NH4+)
高三化学单选题困难题查看答案及解析
25℃时,用0.10mol/L的氨水滴定10.00mL a mol/L的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。已知N点溶液中存在:c(H+)=c(0H-)+c(NH3•H2O),下列说法不正确的是
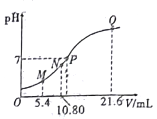
A. 图上四点离子种类相同
B. a=0.108
C. N、Q两点的: N>Q
D. M点溶液中存在:c(H+)=c(OH-)+2(NH3•H2O) +c(NH4+)
高三化学单选题中等难度题查看答案及解析
(题文)25℃时,用0.10 mol/L的氨水滴定10.00 mL 0.05 mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是
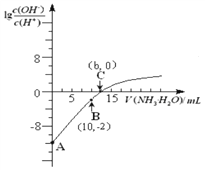
A. H2A的电离方程式为H2AH++HA -
B. B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C. C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D. 25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析
25℃时,用0.10 mol/L的氨水滴定10.00 mL 0.05 mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是
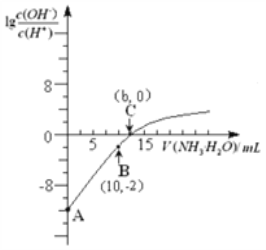
A. H2A的电离方程式为H2AH++HA -
B. B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C. C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D. 25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析
25℃时,用0.10 mol/L的氨水滴定10.00 mL 0.05 mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是
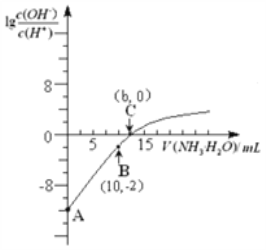
A. H2A的电离方程式为H2AH++HA -
B. B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C. C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D. 25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析
25℃时,用0.10 mol/L的氨水滴定10.00mL0.05mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是( )
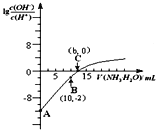
A.H2A的电离方程式为H2AH++HA -
B.B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C.C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D.25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析
25℃时,用0.10 mol/L的氨水滴定10.00mL0.05mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是( )
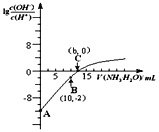
A.H2A的电离方程式为H2AH++HA -
B.B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C.C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D.25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析
25℃时,用0.10 mol/L的氨水滴定10.00mL0.05mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中的关系如图所示。下列说法正确的是( )
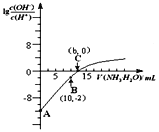
A.H2A的电离方程式为H2AH++HA -
B.B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C.C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D.25℃时,该氨水的电离平衡常数为
高三化学单选题困难题查看答案及解析