-
不溶于水的氧化亚铜可溶于含硫酸铁的硫酸溶液中,这时生成的硫酸亚铁可用酸性高锰酸钾溶液滴定,从而测定氧化亚铜的量:Cu2O+Fe2(SO4)3+H2SO4——FeSO4+CuSO4+H2O FeSO4+KMnO4+H2SO4——Fe2(SO4)3+MnSO4+K2SO4+H2O 由上述反应知;0.1mol/L的KMnO4溶液1mL相当于氧化亚铜的量是( )
 A. 360mg B. 3.6g C. 0.36g D. 2.5×10-4mol
A. 360mg B. 3.6g C. 0.36g D. 2.5×10-4mol
-
硫酸铵是常见的化肥,是强酸弱碱盐,室温下,可用酸碱滴定法测定其氮元素的含量,但由于NH4+的酸性太弱(Ka=5.6×10-10),直接用NaOH标准溶液滴定有困难,生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于甲醛与一定量铵盐作用,生成酸(H+)和六次甲基四铵盐(Ka=7.1×10-6)反应如下:4NH4++ 6HCHO=(CH2)6N4H++ 6H2O+ 3H+,生成物可用酚酞为指示剂,用NaOH标准溶液滴定[在室温下(25℃),通常Ka表示弱酸的电离平衡常数,Kb表示弱碱的电离平衡常数]。硫酸铵含氮量的测定步骤如下:
①准确称取1.800g (NH4)2SO4于烧杯中。
②用适量蒸馏水溶解,然后定量地移至250mL容量瓶中,并用蒸馏水稀释至刻度,摇匀备用。
③用移液管移取试液25mL于锥形瓶中,加入8mL 1:1的甲醛溶液,再加入1~2滴酚酞指示剂摇匀,静置一分钟后,用0.100 mol/L NaOH标准溶液滴定至溶液呈浅红色持续半分钟不褪色,即为终点。
④记录读数,平行做2~3次,NaOH标准溶液滴定消耗的平均体积为27.00mL。
根据实验回答下列问题:
(1)硫酸铵水溶液呈酸性的原因是__________________________________。(用离子方程式说明)
(2)步骤①称取硫酸铵固体样品是否能使用托盘天平______________(填“是”或“否”)。
(3)步骤③加入的甲醛溶液使用前需要加入一定量的NaOH,原因是________________________。
(4)NH4NO3中氮的百分含量是否能用该方法测定______________(填“是”或“否”)。原因是
_________________________________。
(5)据题目给出的信息计算样品中氮的百分含量为_________________ ____。
(6)若室温下,C mol/L氨水的电离平衡常数为Kb,则该氨水的电离度a=_________ ____。(用C
和Kb表示),由此在恒定温度下,你能得出的结论为_________________ ____。
-
硫酸亚铁晶体在医药上作补血剂.某课外小组拟用KMnO4溶液滴定的方法,测定该补血剂中铁元素的含量,进行了如下实验:
[查阅资料]
在酸性条件下,用KMnO4标准溶液进行氧化还原滴定,可以测定Fe2+的含量.反应的离子方程式是:Fe2++MnO4-+H+--Fe3++Mn2++H2O(未配平)
[准备实验用品]
①仪器:a.电子天平,b.滴定管,c.100mL量筒,d.烧杯,e.漏斗,f.250mL容量瓶,g.锥形瓶,h.玻璃棒,i.药匙,j.烧瓶,k.铁架台(带滴定管夹),l.胶头滴管.
②试剂:a.硫酸亚铁补血剂药片,b.高锰酸钾晶体,c.酚酞溶液,d.KSCN溶液,e.稀硫酸,f.稀盐酸,g.蒸馏水.
[实验步骤]
①称取0.474g KMnO4晶体,配成250.00mL水溶液;
②取5片除去糖衣(非还原糖)后的硫酸亚铁补血剂药片(1.500g),研细后加稀硫酸溶解,配成100.00mL水溶液.
③用酸式滴定管取待测“补血剂”溶液20.00mL于某容器中.
④盛装标准KMnO4溶液,静置后,读取数据,记录为KMnO4标准溶液体积的初读数.
⑤滴定,并记录KMnO4标准溶液的终读数.再重复滴定2次.
[实验记录]
滴定次数
实验数据 | 1 | 2 | 3 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 |
| V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
| V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
[交流与讨论]
(1)准备的实验用品中,不需要的仪器有(填序号)______;不需要的试剂有(填序号)______.
(2)本实验所用的KMnO4标准溶液的物质的量浓度为______.
(3)课外小组里有位同学设计了下列四种滴定方式(夹持部分略去),引起了同学们的讨论,最后取得共识,认为最合理的是______(填字母序号).
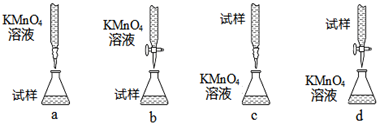
(4)判断滴定终点的依据是______.
(5)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的补血剂中铁元素的含量会______(偏大、偏小、无影响).
(6)根据实验数据,计算该补血剂中铁元素的含量______.
-
KMnO4是一种典型的强氧化剂。请回答下列问题:
(1)实验室中可用已知浓度的酸性高锰酸钾溶液滴定含Fe2+的溶液,从而测定溶液中Fe2+的浓度,离子反应方程式如下,请在空格内填上缺少的反应物,并配平:
_______-Fe2++_______MnO +_______
+_______ ===_______Fe3++_______Mn2++_______H2O
===_______Fe3++_______Mn2++_______H2O
(2)在稀硫酸中,MnO 和H2O2也能发生氧化还原反应:
和H2O2也能发生氧化还原反应:
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
①写出该氧化还原反应的化学方程式:__________________。
反应中若有0.5 mol H2O2参加此反应,转移电子的个数为________。
②实验中发现,当加入的少量KMnO4完全反应后,H2O2仍能发生反应快速放出气体。其可能的原因是__________________
-
下列有关仪器的使用方法或实验操作正确的是( )
A.用碱式滴定管量取13.60mL酸性高锰酸钾溶液
B.测定硫酸铜晶体结晶水含量时,加热后的坩埚须在干燥器中冷却,再称量
C.蒸馏时,应使温度计水银球置于蒸馏液体中
D.过滤时,先将滤纸湿润,然后再将滤纸放入漏斗中
-
下列现象或事实可用同一原理解释的是( )
A.SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
B.浓硫酸和浓盐酸长期暴露在空气中浓度降低
C.不能用pH试纸测定浓硫酸和新制氯水的pH
D.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
-
下列实验装置进行相应的实验,能达到实验目的的是
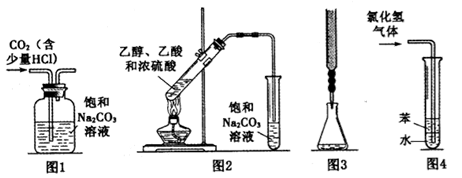
A.图1装置:除去二氧化碳中的少量氯化氢气体
B.图2装置:加热乙醇、乙酸和浓硫酸的混合液制取乙酸乙酯
C.图3装置:用酸性高锰酸钾溶液滴定过氧化氢溶液
D.图4装置:用水吸收氯化氢气体
-
(9分)某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物。
己知:①Cu2O溶于稀硫酸生成Cu和CuSO4,②Cu2O在空气中加热生成CuO。
(1)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为__________。
(2)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | 供选择试剂 |
| Fe3+ | 1.9 | 3.7 | A.氯水, B.H2O2, C.NaOH, D.氨水, E.CuO, F.Cu2(OH)2CO3 |
| Fe2+ | 7.5 | 11 |
| Cu2+ | 6.0 | 10 |
实验小组设计如右图实验方案:
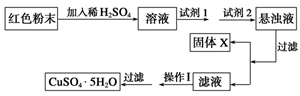
试回答:
①试剂1可以为________________,试剂2可以为________________。
②固体X的化学式为____________。
③操作Ⅰ为____________________。
-
下列有关物质性质的叙述正确的是
A.浓硫酸能干燥氢气、氯气、一氧化碳等气体,说明浓硫酸具有吸水性
B.SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物
C.乙炔能使溴水、酸性高锰酸钾溶液褪色,说明乙炔具有漂白性
D.纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖
-
研究不同 pH 时 CuSO4 溶液对 H2O2 分解的催化作用。资料:a.Cu2O 为红色固体,难溶于水,能溶于硫酸,生成 Cu 和Cu2+。b.CuO2 为棕褐色固体,难溶于水,能溶于硫酸,生成 Cu2+和 H2O2。c.H2O2 有弱酸性:H2O2  H+ +HO2-,HO2-
H+ +HO2-,HO2-  H+ +O22-。
H+ +O22-。
| 编号 | 实验 | 现象 |
| Ⅰ | 向 1 mL pH=2 的 1 mol·L− 1 CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 出现少量气泡 |
| Ⅱ | 向 1 mL pH=3 的 1 mol·L− 1 CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 立即产生少量棕黄色沉淀,出现较明显气泡 |
| Ⅲ | 向 1 mL pH=5 的 1 mol·L− 1CuSO4溶液中加入 0.5 mL 30% H2O2 溶液 | 立即产生大量棕褐色沉淀,产生大量气泡 |
(1) 经检验生成的气体均为 O2,Ⅰ中 CuSO4 催化分解 H2O2 的化学方程式是__。
(2)对Ⅲ中棕褐色沉淀的成分提出 2 种假设:ⅰ.CuO2,ⅱ.Cu2O 和CuO2 的混合物。为检验上述假设,进行实验Ⅳ:过滤Ⅲ中的沉淀,洗涤,加入过量硫酸,沉淀完全溶解,溶液呈蓝色,并产生少量气泡。
①若Ⅲ中生成的沉淀为 CuO2,其反应的离子方程式是__。
②依据Ⅳ中沉淀完全溶解,甲同学认为假设ⅱ不成立,乙同学不同意甲同学的观点,理由是__。
③为探究沉淀中是否存在 Cu2O,设计如下实验:
将Ⅲ中沉淀洗涤、干燥后,取 a g 固体溶于过量稀硫酸,充分加热。冷却后调节溶液 pH,以 PAN 为指示剂,向溶液中滴加 c mol·L − 1EDTA 溶液至滴定终点,消耗 EDTA 溶液 V mL。V=__,可知沉淀中不含 Cu2O,假设ⅰ成立。(已知:Cu2++EDTA= EDTA-Cu2+,M(CuO2)=96 g·mol − 1,M(Cu2O)=144 g·mol−1)
(3)结合方程式,运用化学反应原理解释Ⅲ中生成的沉淀多于Ⅱ中的原因__ 。
(4)研究Ⅰ、Ⅱ、Ⅲ中不同 pH 时 H2O2 分解速率不同的原因。
实验Ⅴ:在试管中分别取 1 mL pH=2、3、5 的 1 mol·L−1 Na2SO4 溶液,向其中各加入 0.5 mL 30% H2O2 溶液,三支试管中均无明显现象。
实验Ⅵ:__(填实验操作和现象),说明 CuO2 能够催化 H2O2 分解。
(5)综合上述实验,Ⅰ、Ⅱ、Ⅲ中不同 pH 时 H2O2 的分解速率不同的原因是__。
A. 360mg B. 3.6g C. 0.36g D. 2.5×10-4mol


