-
(16分)印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
(1)测得某废腐蚀液中含CuCl2 1.5 mol·L-1、FeCl23.O mol·L-1、FeCl3 1.0 mol·L-1、HCl3.0 mol·L-1。取废腐蚀液200mL按如下流程在实验室进行实验:
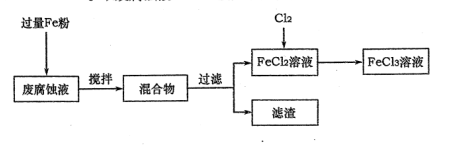
回答下列问题:
① 废腐蚀液中加入过量铁粉后,发生反应的离子方程式为________ 。
② 检验废腐蚀液中含有Fe3+的实验操作是________;
在上述流程中,“过滤”用到的玻璃仪器有烧杯、玻璃棒、________。
③由滤渣得到纯铜,除杂所需试剂是 ________ 。
(2)某化学兴趣小组利用下图装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。
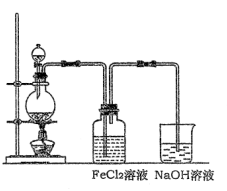
①实验开始前,某同学对实验装置进行了气密性检查,方法是________。
②浓盐酸与二氧化锰反应的化学方程式为;
烧杯中NaOH溶液的作用是 ________ 。
③参考(1)中数据,按上述流程操作,需称取Fe粉的质量应不少于________g,
需通入Cl2的物质的量应不少于________mol.
-
印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.
(1)测得某废腐蚀液中含CuCl2 1.5mol•L-1、FeCl23.0 mol•L-1、FeCl3 1.0mol•L-1、HCl3.0mol•L-1.取废腐蚀液200mL按如下流程在实验室进行实验:
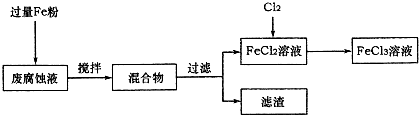
回答下列问题:
①废腐蚀液中加入过量铁粉后,发生反应的离子方程式为________;
②检验废腐蚀液中含有Fe3+的实验操作是________;
在上述流程中,“过滤”用到的玻璃仪器有烧杯、玻璃棒、________.
③由滤渣得到纯铜,除杂所需试剂是________.
(2)某化学兴趣小组利用如图装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液.
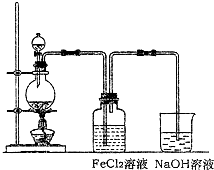
①实验开始前,某同学对实验装置进行了气密性检查,方法是________.
②浓盐酸与二氧化锰反应的化学方程式为________;
烧杯中NaOH溶液的作用是________.
③参考(1)中数据,按上述流程操作,需称取Fe粉的质量应不少于________g,需通入Cl2的物质的量应不少于________mol.
-
印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol•L-1、FeCl2 3.0mol•L-1、FeCl3 1.0mol•L-1、HCl 3.0mol•L-1.取废腐蚀液200mL按如下流程在实验室进行实验:
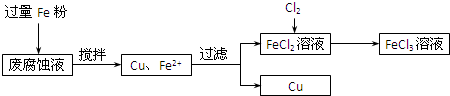
回答下列问题:
(1)在上述流程中,“过滤”用到的玻璃仪器:普通漏斗、玻璃棒、______;用上述方法获得的铜粉中含有杂质,除杂所需试剂是______(填化学式).
(2)实验室可用浓盐酸和固体KMnO4直接反应制备Cl2.此反应的离子方程式为______.此反应中体现了盐酸的______性质.利用图1制备Cl2并通入到FeCl2溶液中获得FeCl3溶液.

请从图2中挑选所需的仪器,完成图1装置简图(可添加必要的塞子、玻璃导管、胶皮管.不画固定装置),并标明容器中所装试剂名称.
(3)按上述流程操作,需称取Fe粉的质量应不少于______g,需通入Cl2的物质的量不少于______mol.
-
印刷电路的废腐蚀液中含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
(1)测得某废腐蚀液中含CuCl2 1.5 mol·L-1、FeCl2 3.0 mol·L-1、FeCl3 1.0 mol·L-1、HCl 3.0 mol·L-1。
取废腐蚀液200 mL按如下流程在实验室进行实验:
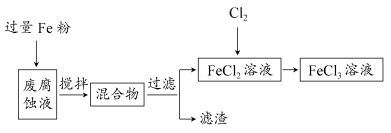
回答下列问题:
①废腐蚀液中加入过量铁粉后,发生反应的离子方程式为________。
②检验废腐蚀液中含有Fe3+的实验操作是________;在上述流程中,“过滤”用到的玻璃仪器有烧杯、玻璃棒、________。
③由滤渣得到纯铜,除杂所需试剂是________。
(2)某化学兴趣小组利用下图所示装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。

①实验开始前,某同学对实验装置进行了气密性检查,方法是________。
②浓盐酸与二氧化锰加热反应的化学方程式为________;烧杯中NaOH溶液的作用是________。
③参考(1)中数据,按上述流程操作,需称取Fe粉的质量应不少于________g,需通入Cl2的物质的量应不少于________ mol。
-
(18分)电子工业常用30﹪的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,应考虑回收利用。按如下流程在实验室进行实验:从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
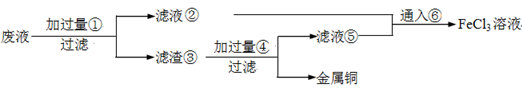
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:________。
(2)检验废腐蚀液中含有Fe3+的实验操作是________
(3)“过滤”用到的玻璃仪器有:普通漏斗、________。
(4)废液中加入过量①后,发生反应的离子方程式:
(5)上述流程中取废液200 mL,其中含CuCl2 1.5 mol·L—1、FeCl2 3.0 mol·L—1、FeCl3 1.0 mol·L—1,若要将铜全部回收,需加入Fe粉的质量应不少于_____________g;将铁的化合物全部转化为FeCl3溶液需通入Cl2的物质的量不少于_______________mol。
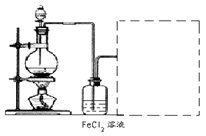
(6)某化学兴趣小组利用在下图装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。
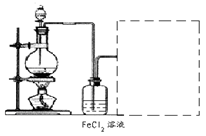
制备Cl2的化学方程式为:
该装置不完整,请在所给虚线框内画出所缺部分,并标注试剂。
-
电子工业常用30﹪的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,应考虑回收利用。按如下流程在实验室进行实验:从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:。
(2)检验废腐蚀液中含有Fe3+的实验操作是________
(3)“过滤”用到的玻璃仪器有:普通漏斗、________。
(4)废液中加入过量①后,发生反应的离子方程式:________
(5)上述流程中取废液200 mL,其中含CuCl2 1.5 mol·L—1、FeCl2 3.0 mol·L—1、FeCl3 1.0 mol·L—1,若要将铜全部回收,需加入Fe粉的质量应不少于_____________g;将铁的化合物全部转化为FeCl3溶液需通入Cl2的物质的量不少于_______________mol。
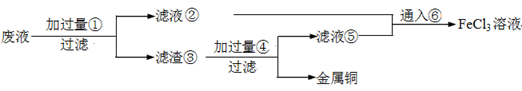
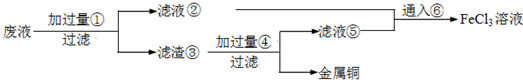
(6)某化学兴趣小组利用在下图装置制取氯气并通入到FeCl2溶液中获得FeCl3溶液。
制备Cl2的化学方程式为:________
该装置不完整,请在所给虚线框内画出所缺部分,并标注试剂。
-
电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费,应考虑回收利用.按如下流程在实验室进行实验:从废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:______.
(2)检验废腐蚀液中含有Fe3+的实验操作是______.
(3)“过滤”用到的玻璃仪器有:普通漏斗、______.
(4)废液中加入过量①后,发生反应的离子方程式:______.
(5)上述流程中取废液200mL,其中含CuCl2 1.5mol•L-1、FeCl2 3.0mol•L-1、FeCl3 1.0mol•L-1,若要将铜全部回收,需加入Fe粉的质量应不少于______g;将铁的化合物全部转化为FeCl3溶液需通入Cl2的物质的量不少于______mol.
-
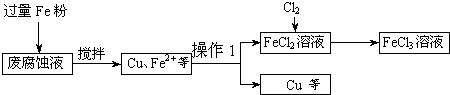
印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______ KCl+3Cl2↑+3H2O
-
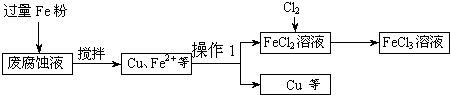
印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______ KCl+3Cl2↑+3H2O
-
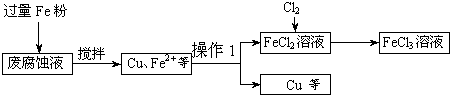
印刷电路的废腐蚀液含有大量CuC12、FeC12和FeC13,任意排放将导致环境污染及资源的浪费.可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L.取废腐蚀液200mL按如下流程在实验室进行实验:
回答下列问题:
(1)上述方法获得的铜粉中含有杂质,除杂质所需试剂是______(填化学式).
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物.反应的化学方程式为______ KCl+3Cl2↑+3H2O
















