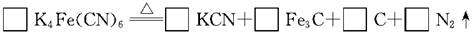-
铁是目前应用最多的金属,铁的单质及其化合物用途非常广泛。
(1)K4[Fe(CN)6]可用作食盐的抗结剂。基态钾原子的电子排布式为_______________。
(2)Na2[Fe(CN)5(NO)] 可用作治疗高血压急症。
①Na、N、O的第一电离能有小到大的顺序为_______________。
②CN-中碳原子的杂化类型是_______________。
(3)过氧化氢在FeCl3催化作用下分解生成水和氧气。
①1molH2O2中σ键的数目为_______________。
②H2O的沸点比H2S高的原因是_______________。
(4)铁触媒是重要的催化剂。CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学方程式为[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
①与CO互为等电子体的分子为_____________。配合物[Cu(NH3)2]OOCCH3中不存在的的作用力是_______(填字母)。
a.离子键 b.金属键 c.配位键 d.极性共价键
②Fe(CO)5在空气中燃烧的化学方程式为4Fe(CO)5+13O2  2Fe2O3+20CO2,Fe2O3的晶体类型是___________。
2Fe2O3+20CO2,Fe2O3的晶体类型是___________。
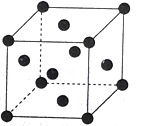
③铁的晶胞如图所示,若该晶体的密度是ag·cm-3,则两个最近的Fe原子间的距离为_____cm(设NA为阿伏伽德罗常数的值)。
-
(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是____。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_____ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(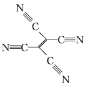 )。
)。
①CH3CN中碳原子的杂化方式是 ____ 和_____ 。
②TCNE中第一电离能较大的是 ___(填元素符号),分子中所有原子____(填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是 ___。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为 ___(列出计算式)g·cm-3。
-
(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是____。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_____ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(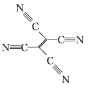 )。
)。
①CH3CN中碳原子的杂化方式是 ____ 和_____ 。
②TCNE中第一电离能较大的是 ___(填元素符号),分子中所有原子____(填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是 ___。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为 ___(列出计算式)g·cm-3。
-
K4[Fe(CN)6]可用作食盐的抗结剂,高温下K4[Fe(CN)6]会分解生成(CN)2、KCN、N2、Fe3C、C等物质。
(1)基态铁原子的价电子排布式为___;上述物质中涉及的几种元素的第一电离能由大到小的顺序为___;[Fe(CN)6]4-中,铁提供的空轨道数目是___。
(2)(CN)2分子中存在碳碳键,则(CN)2的立体构型是__,分子中σ键与π键数目之比为___;KCN与盐酸作用可形成HCN,HCN的中心原子的杂化轨道类型为___。
(3)已知Fe3C的晶胞结构中碳原子的配位数为6,与碳原子紧邻的铁原子的空间构型为___,铁原子的配位数是___。
(4)碳元素可形成多种结构和性质不同的单质,其中金刚石的熔点为3550℃,C60的熔点约为280℃,导致这种差异的原因是___。
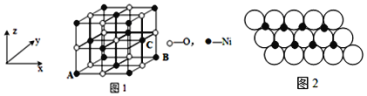
(5)铁、镍位于同一族,若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为___。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为___g。(用a、NA表示)
-
我国许可使用的食盐抗结剂目前有:亚铁氰化钾、磷酸钙、二氧化硅和微晶纤维素。卫生部规定食盐中亚铁氰化[K4Fe(CN)6]的最大使用量为10mg•kgˉ1.
(1)基态钾原子核外能量最高的电子所在能级的轨道数目为__________,K4Fe(CN)6中Fe2+的外围电子排布图为_________________。
(2)K4Fe(CN)6中存在_____________(填序号)。
A.离子键 B.非极性键 C.配位键 D.σ键 E.π 键
(3)写出和CN-互为等电子体的离子的电子式为______________________
(4)磷酸钙中磷酸根的空间构型为______________,二氧化硅晶体中硅原子的杂化方式为_____
(5)亚铁氰化钾溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与CN-是等电子体的气态化合物,反应化学方程式为_______________ 。
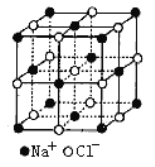
(6)FeO晶体的晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为428pm,则该晶体的密度为____g/cm3 (列出计算式即可,用NA 表示阿伏伽德罗常数的值)。
-
(7分)黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg·kgˉ1。黄血盐易溶于水,在水溶液中会电离出K+和[Fe(CN)6]4ˉ,其中CNˉ的电子式为 。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O
。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
(1)上述反应是否为氧化还原反应?______ (填“是”或“不是”)。
(2)食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过4000C时会分解,试配平该反应的化学方程式:
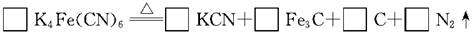
(3) 黄血盐可与高锰酸钾溶液反应,其化学方程式为
K4Fe(CN)6+ KMnO4+ H2SO4→KHSO4+ Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平)
①该反应的氧化产物有______________(填化学式)。
②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为______________mol。
-
黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg•kgˉ1.黄血盐易溶于水,在水溶液中会电离出K+和[Fe(CN)6]4ˉ,其中CNˉ的电子式为
 .它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O
.它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
(1)上述反应是否为氧化还原反应?______ (填“是”或“不是”).
(2)食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过400C时会分解,试配平该反应的化学方程式:______K4Fe(CN) ______KCN+______Fe3C+5C+3N2↑
______KCN+______Fe3C+5C+3N2↑
(3)黄血盐可与高锰酸钾溶液反应,其化学方程式为:
K4Fe(CN)6+KMnO4+H2SO4→KHSO4+Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平)
①该反应的氧化产物有______(填化学式).
②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为______mol.
-
黄血盐[亚铁氰化钾,K4[Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg•kgˉ1。一种制备黄血盐的工艺如下:
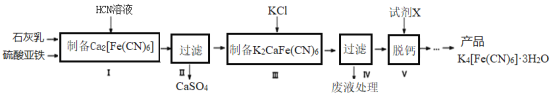
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为____________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为(填化学式)___________________。
(3)步骤Ⅴ所用的试剂 X 是______________________。
-
黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg·kg-1。一种制备黄血盐的工艺如下:
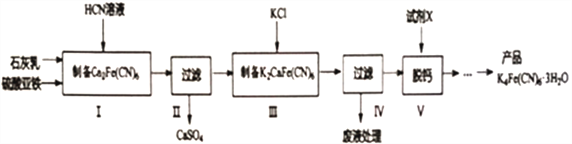
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为_____________________________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为_______________________。(填化学式)
(3)步骤Ⅴ所用的试剂X是_________________。
(4)工艺中用到剧毒的HCN 溶液,含CN-的废水必须处理后才能排放。己知氢氰酸是一种具有苦杏仁特殊气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①NaCN 的电子式为_________________,反应CNˉ +H2O HCN+OHˉ在25℃时的平衡常数 K= _________________。(填数值)
HCN+OHˉ在25℃时的平衡常数 K= _________________。(填数值)
②处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-“不完全氧化”为OCN-;第二步控制 pH为7.5~8.5,用NaClO“不完全氧化”OCNˉ生生成N2和两种盐。
第一步控制强碱性的主要目的是__________________________________。
第二步反应的离子方程式为______________________________。
-
黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),制备黄血盐的一种工艺如下:
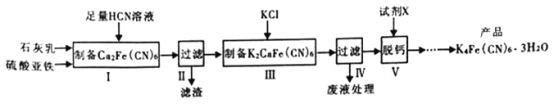
回答下列问题:
(1)实验室用绿矾晶体配制硫酸亚铁溶液时,为了防止其变质需要添加的试剂为__________________。
(2)步骤Ⅱ中滤渣的主要成分是_______________,步骤Ⅴ所用的试剂X可以是________________。
(3)步骤Ⅲ反应的化学方程式为_______________________________________。
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。25℃时,Ka(HCN) =6.25×10-10。
①HCN的电子式为__________________。
②25℃时,反应CN-+H2O HCN+OH-的平衡常数K=_____________________。
HCN+OH-的平衡常数K=_____________________。
③含CN-废水的处理方法之一是:pH控制在11左右,用氯气将废水中CN-氧化成CO2和N2,该反应的离子方程式为_____________________________________。
(5)近日,一条“盐里面加进了亚铁氰化钾”危害身体健康的信息在网上流传。已知K4Fe(CN)6 4KCN+FeC2+N2↑,氰化钾的半数致死量(LD50)为6.4 mg·kg-1 (即每1kg体重6.4 mg),我国卫生部规定食盐中黄血盐的最大使用量为10 mg·kg-1。假设烹饪过程中黄血盐发生上述分解,一名60Kg男子每天摄入60g食盐是否达到氰化钾的半数致死量?_________________________________。(列式计算说明)。
4KCN+FeC2+N2↑,氰化钾的半数致死量(LD50)为6.4 mg·kg-1 (即每1kg体重6.4 mg),我国卫生部规定食盐中黄血盐的最大使用量为10 mg·kg-1。假设烹饪过程中黄血盐发生上述分解,一名60Kg男子每天摄入60g食盐是否达到氰化钾的半数致死量?_________________________________。(列式计算说明)。
2Fe2O3+20CO2,Fe2O3的晶体类型是___________。

 )。
)。
 )。
)。