-
下列关于化学与生活的说法不正确的是
A. 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
B. 高纯硅可以将太阳能直接转化为电能
C. 化学药品着火,都要立即用水或泡沫灭火器灭火
D. 工业上Cl2用与石灰乳反应制备漂白粉
高三化学选择题简单题查看答案及解析
-
化学与人类生活、生产和社会可持续发展密切相关。下列说法不正确的是( )
A. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒
B. 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验是否酒后驾车
C. 水泥冶金厂常用高压电除尘,是因为烟尘在空气中形成胶体且发生丁达尔效应
D. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是产生雾霾天气的主要因素
高三化学单选题中等难度题查看答案及解析
-
化学与人类生活、生产和社会可持续发展密切相关。下列说法不正确的是
A. 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验是否酒后驾车
B. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是产生雾霾天气的主要因素
C. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒
D. 煤经过气化和液化两个物理变化过程后变为清洁能源。这是煤的综合利用的方法
高三化学单选题简单题查看答案及解析
-
化学与生产、生活密切相关,下列说法错误的是( )
A.在花生油中添加抗氧化剂(TBHQ)可延缓其酸败过程
B.利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验是否酒后驾车
C.生石灰、硅胶、无水CaCl2、P2O5 等均可作食品干燥剂
D.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是产生雾霾天气的主要因素
高三化学单选题简单题查看答案及解析
-
下列说法正确的是( )
A. CH3(C2H5)CHCH(CH3)2的系统命名为2—甲基—3—乙基丁烷
B. 苯甲酸的结构简式为
C. 利用乙醇的还原性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
D. C5H10的同分异构体中属于烯烃的有6种
高三化学选择题中等难度题查看答案及解析
-
下列说法中正确的是
A. 植物油中由于含有碳碳双键,因此在空气中长时间放置容易氧化变质
B. 利用乙醇的氧化性以及Cr3+、Cr2O72-的颜色差异来检验酒后驾车
C. 石油可以通过裂解、裂化等物理变化获得重要化工原料乙烯
D. 黄河入海口沙洲的形成体现了胶体电泳的性质
高三化学选择题简单题查看答案及解析
-
下列说法中错误的是
A.淀粉、纤维素和蛋白质均属于高分子化合物
B.用漂白粉漂白时,向水溶液中加几滴白醋,会增强漂白效果
C.利用乙醇的还原性以及Cr3+、Cr2O7-的颜色差异来检验酒后驾车
D.合成纤维和光导纤维都是新型无机非金属材料
高三化学选择题简单题查看答案及解析
-
交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐(Cr2O72-橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等。重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬。方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬。请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是________。
(2)写出碳和重铬酸钠高温反应的化学方程式________。
Cr2O3经铝热法还原制得金属铬的化学方程式是________。
(3)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是 ________。
(4)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为________。
高三化学选择题简单题查看答案及解析
-
化学已渗透到人类生活的各个方面,下列说法不正确的是( )
A.交警检查司机是否酒后驾车的原理中体现了乙醇的还原性
B.硅胶多孔,吸附水分能力强,常用作袋装食品、瓶装药品的干燥剂
C.铜的金属活动性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀
D.以石油、煤和天然气为原料通过聚合反应可以获得用途广泛的高分子合成材料
高三化学选择题中等难度题查看答案及解析
-
化学与生活密切相关。
I.K2Cr2O7曾用于检测司机是否酒后驾驶:Cr2O72-(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH(未配平)
(1)基态Cr原子的价电子轨道表达式为__。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为__,碳原子的轨道杂化类型为__,所含σ键与π键的数目之比为__。
(3)已知Cr3+等过渡元素水合离子的颜色如表所示:
离子
Sc3+
Cr3+
Fe2+
Zn2+
水合离子的颜色
无色
绿色
浅绿色
无色
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因为__。
II.ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4)Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有__(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为__。
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。
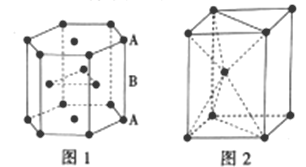
(5)锌的堆积方式为__,配位数为__。
(6)若锌原子的半径为apm,阿伏加德罗常数的值为NA,则锌晶体的密度为___g/cm3(用含a的代数式表示)。
高三化学综合题困难题查看答案及解析