-
侯氏制碱法中可循环利用的物质是
A. CO2、NaCl B. NH3、NaCl C. NH3、CO2 D. CaO、NH3
高三化学单选题困难题查看答案及解析
-
年,比利时人索尔维
用氨碱法生产碳酸钠.反应原理如下:
时一些物质在水中的溶解度
NaCl
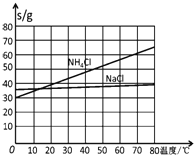
(1)氨碱法生成纯碱的原料是____________,可循环利用的物质有____________.
(2)饱和NaCl溶液通
和
能生成
的原因有:____________.
Ⅲ
我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(3)生产中需向分离出
后所得的溶液中加入NaCl固体并通入
,在____________
填温度范围
下析出____________
填化学式
高三化学工业流程中等难度题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业作出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、NH3和CO2为原料制得NaHCO3,进而生产出纯碱。相关的化学反应有:①NH3+CO2+H2O===NH4HCO3;②NH4HCO3+NaCl===NaHCO3↓+NH4Cl;③2NaHCO3
Na2CO3+CO2↑+H2O↑。某研究性学习小组的同学模拟“侯氏制碱法”,提出下列三种制备NaHCO3的实验方案。
方案1:分别将CO2和NH3通入到饱和食盐水中;
方案2:将CO2通入到含NH3的饱和食盐水中;
方案3:将NH3通入到含CO2的饱和食盐水中。
(1)经过讨论,大家一致认为方案2较合理,请说明方案3的不足之处
________________________________________________________________________。
(2)根据方案2,某同学设计了如下实验步骤和装置图:
步骤1:配制含氨的饱和食盐水。在100 mL锥形瓶中加入20 mL氨水(体积比1∶1),再加入8 g食盐,塞紧橡皮塞,振荡几分钟,过滤除去不溶物,得到含氨的饱和食盐水。
步骤2:制备NaHCO3。按图组装实验装置,先检查装置的气密性,再向各仪器中加入相应的试剂制备NaHCO3。实验过程中,需要控制温度在30~35 ℃(大于35 ℃时NH4HCO3会分解)和CO2的通入速度(以出现能数得清的连续气泡为宜)。反应结束后,把锥形瓶浸入冷水中,使较多的晶体析出,过滤、洗涤。
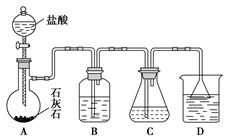
请回答下列问题:
①为控制反应温度在30~35 ℃,应采用的操作方法是________________________。
②装置B中的试剂是__________________,它的作用是__________________________。
③检验步骤2中所得晶体是NaHCO3而不是NaCl的实验方法和现象是
________________________________________________________________________
________________________________________________________________________。
④设计一个简单的实验方案证明Na2CO3溶液呈碱性是由CO32-引起的
________________________________________________________________________
________________________________________________________________________。
高三化学填空题中等难度题查看答案及解析
-
利用食盐水制取ClO2的工业流程如图所示。

装置①中的反应:
装置②中的反应:
下列关于该流程的说法正确的是
A.该流程中仅NaCl可循环利用
B.装置①中H2是阴极产物
C.装置②中Cl2是还原产物
D.为使H2完全转化为HCl,还应向装置③中再补充Cl2
高三化学多选题中等难度题查看答案及解析
-
实验室利用下列反应装置模拟侯氏制碱法制备NaHCO3,反应原理为:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,下列说法错误的是( )
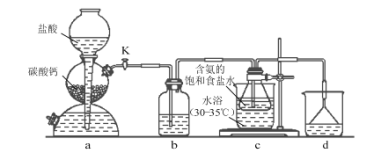
A.通过活塞K可控制CO2的流速
B.装置b、d依次盛装饱和Na2CO3溶液、稀硫酸
C.装置c中含氨的饱和食盐水提高了CO2吸收效率
D.反应后将装置c中的锥形瓶浸入冷水充分冷却,过滤得到NaHCO3晶体
高三化学单选题中等难度题查看答案及解析
-
某小组以石膏(CaSO4·2H2O)为主要原料制备(NH4)2SO4的流程如下:
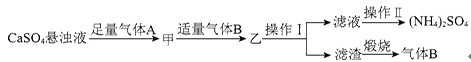
下列说法正确的是
A. 气体B是NH3,可循环利用
B. 操作Ⅰ中,所用的主要玻璃仪器为烧杯、玻璃棒、分液漏斗
C. 操作Ⅱ中,可用蒸发结晶的方法得到纯净的(NH4)2SO4
D. 整个过程的总反应方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
高三化学选择题困难题查看答案及解析
-
“侯德榜制碱法”首先需制备碳酸氢钠:NaCl(饱和)+NH3+CO2+H2O =NaHCO3 ↓ +NH4C1。下列装置能达到实验目的的是
A.
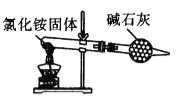 B.
B.  C.
C. 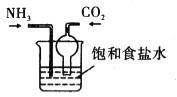 D.
D. 
高三化学单选题简单题查看答案及解析
-
某学习小组的同学根据“侯氏制碱法”的原理:
①NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl
②2NaHCO3
Na2CO3+H2O+CO2↑
利用如下实验装置制备Na2CO3。
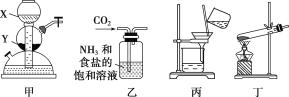
下列叙述正确的是( )
A.若X为稀硫酸,Y为碳酸钙,则可用装置甲制取CO2
B.装置乙中会有白色沉淀析出
C.将装置丙中所得滤液蒸干可得到NH4Cl固体
D.用装置丁加热NaHCO3固体可制得Na2CO3
高三化学单选题中等难度题查看答案及解析
-
侯氏制碱法在我国工业发展中具有重要作用。现某学习小组在实验室中利用下列反应装置模拟侯氏制碱法制备 NaHCO3,反应原理为 NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。下列说法正确的是
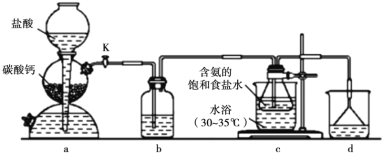
A.装置 a 中可改用碳酸钙粉末提高反应速率
B.装置 b、d 依次盛装饱和 Na2CO3 溶液、稀硫酸
C.装置 c 中含氨的饱和食盐水提高了 CO2 吸收效率
D.反应后将装置 c 中的锥形瓶充分冷却,蒸发结晶得到 NaHCO3 晶体
高三化学单选题中等难度题查看答案及解析
-
著名的“侯氏制碱法”第一步反应是向饱和氨化盐水中通入二氧化碳,该反应可表示为NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl有关物质的溶解度数据如下(g/100g水):
NaCl NaHCO3 NH4Cl
10℃35.8 8.15 33.0
45℃37.0 14.0 50.0
现在45℃时,向434g饱和食盐水中通入适量氨气,再向其中通入二氧化碳后,按上述反应进行完全.试计算并回答下列问题(计算结果保留三位有效数字).
(1)反应完全后45℃时析出的晶体的化学式是________,并计算析出晶体的质量.
(2)过滤除去晶体后再降温至10℃,此时析出的晶体是(填化学式)________,计算所析出晶体的质量.高三化学填空题中等难度题查看答案及解析