-
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是
A. 阳极反应为Fe - 2e- = Fe2+ B. 过程中有Fe(OH)3沉淀生成
C. 电路中每转移12mol电子,最多有1mol Cr2O72-被还原 D. 如果石墨做阴阳极,电解过程不变
高二化学选择题困难题查看答案及解析
-
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确是
A.阳极反应为Fe-2e- =Fe2+
B.电解过程中溶液pH不会变化
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原
高二化学选择题中等难度题查看答案及解析
-
电解法处理酸性含铬废水(主要含有Cr2O
)时,以铁板作阴、阳极,处理过程中存在反应Cr2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是( )
A. 阳极反应为Fe-2e-===Fe2+
B. 电解过程中溶液pH不会变化
C. 处理过程中有Fe(OH)3沉淀生成
D. 每转移12 mol电子,有1 mol Cr2O
被还原
高二化学null中等难度题查看答案及解析
-
电解法处理酸性含铬废水(主要含有
)时,以铁板作阴、阳极,处理过程中存在反应
+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是 ( )
A.阳极反应为Fe-2e-=Fe2+
B.电解过程中溶液c(H+)不会变化
C.处理过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol
被还原
高二化学单选题中等难度题查看答案及解析
-
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如下,下列说法不正确的是
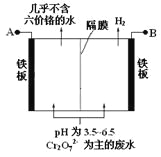
A.A为电源正极
B.阳极区溶液中发生的氧化还原反应为:Cr2O72-+6Fe2++14H+= 2Cr3++6Fe3++ 7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原
高二化学单选题简单题查看答案及解析
-
利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示;电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O

(1)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨Ⅱ是电池的 极;石墨Ⅰ附近发生的电极反应式为 。
(2)工作时,甲池内的NO3-离子向 极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的O2和NO2的体积比为 。
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为 。
(4)若溶液中减少了0.01 mol Cr2O72-,则电路中至少转移了 mol电子。
(5)向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s)
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
高二化学选择题简单题查看答案及解析
-
(1)利用电化学原理,将 NO2、O2 和熔融 KNO3 制成燃料电池,模拟工业电解法来处理含 Cr2O72-废水,如下图所示;电解过程中溶液发生反应: Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2 O。
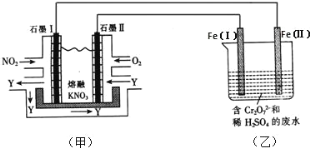
①甲池工作时,NO2 转变成绿色硝化剂 Y,Y 是 N2O5,可循环使用,则石墨Ⅱ附近发生的电极反应式为______。
②向完全还原为 Cr3+的乙池工业废水中滴加 NaOH 溶液,可将铬以 Cr(OH)3 沉淀的形式除去,已知 Cr(OH)3 存在以下溶解平衡:Cr(OH)(s)
Cr3+(aq)+3OH-(aq),常温下 Cr(OH)3 的溶度积 K=c(Cr3+)•c(3OH-)=1.0×10-32,要使 c(Cr3+)降至 10-5mol•L-1,溶液的 pH 应调至___________。
(2)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行: Cd+2NiO(OH)+H2O
Cd(OH)2+2Ni(OH)2
回答下列问题:
①放电时,金属 Cd 作______极;
②充电时的阳极电极反应式为。_____
③充电时,当电路中通过 0.2moleˉ,阴极质量将___________(填“增加”、“减少”)___________。
高二化学综合题困难题查看答案及解析
-
如图所示,某工厂采用电解法处理含铬(Cr2O72﹣)酸性废水,其中,耐酸电解槽以铁板作阴、阳极,电解后,溶液中的Cr2O72﹣全部变为Cr3+,下列说法不正确的是
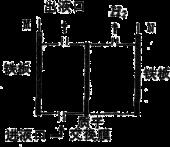
A.M与电源的正极相连 B.出液口排出的溶液中还含有Fe3+
C.N极电极反应为2H++2e﹣==H2↑ D.阴极区附近溶液pH降低
高二化学选择题中等难度题查看答案及解析
-
(1)用电解法分开处理含有Cr2O72-及含有NO2-的酸性废水[最终Cr2O72-转化为Cr3+,NO2-转化为无毒物质],其装置如图所示。
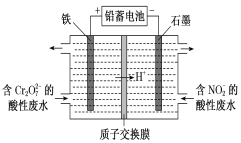
①阴极电极反应:________________________,
左池中Cr2O72-转化为Cr3+的离子方程式是_________________________________________。
②当阴极区消耗2 mol NO2-时,右池减少的H+的物质的量为________ mol。
③若将铁电极换成石墨棒,阳极电极反应式为:_________________________________。
(2)由甲醇(CH3OH)、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为___________________________________________,正极电极反应式_____________________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有2mol·L-1HCl与0.5mol·L-1CuSO4的混合溶液。当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上收集到氧气的质量为_____g,总共转移_____mol电子。
高二化学综合题中等难度题查看答案及解析
-
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右,下列说法不正确的是

A.A为电源正极
B.阴极区附近溶液pH降低
C.阳极区溶液中发生的氧化还原反应为Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O
D.若不考虑气体的溶解,当收
集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O72-被还原
高二化学选择题困难题查看答案及解析