-
在酸性介质中,向MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下离子反应:
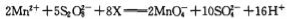 ,下列说法正确的是:
,下列说法正确的是:A.X是 H2O
B.还原性:SO42->Mn2+
C.该反应中酸性介质可以为盐酸
D.每生成0.1 molSO42-转移电子0.05 mol
高三化学选择题中等难度题查看答案及解析
-
(1)在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(连二硫酸铵)溶液会发生如下离子反应(未配平):
Mn2++S2O82—+H2O→MnO4—+SO42—+H+;
①该反应常用于检验Mn2+的存在,其特征现象是___________________________________。
②若反应中有0.1 mol还原剂参加反应,则转移电子数为________NA,消耗氧化剂的物质的量______________mol。
③写出该反应的离子方程式_________________________________。
(2)①向CuSO4溶液中通入硫化氢生成黑色沉淀CuS的离子方程式为___________________________________;
②向FeCl3溶液中加入过量的碘化钠溶液的离子方程式为_____________。
(3)在碱性介质中,H2O2有较强的还原性,可与Ag2O反应,该反应中氧化剂与还原剂的物质的量之比为___________________。
(4)为测定大气中的臭氧(O3)含量,将0℃、1.01×105 Pa的空气V L慢慢通入足量KI溶液,使臭氧完全反应;然后将所得溶液用a mL c mol·L-1的Na2S2O3溶液进行滴定,恰好达到终点。已知:2Na2S2O3+I2=Na2S4O6+2NaI。
①该滴定过程中可选择的指示剂为________。
②O3与KI溶液反应生成两种单质,则反应的化学方程式为___________________________。
③空气中臭氧的体积分数为________(用含“a、c、V”的字母表示)。
高三化学填空题困难题查看答案及解析
-
(8分)在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(连二硫酸铵)溶液会发生如下离子反应:
(1)配平:
(2)该反应常用于检验Mn2+的存在,其特征现象是___________________________________。
(3)若反应中有0.1 mol还原剂参加反应,则转移电子数为________NA,消耗氧化剂的物质的量______________mol。
高三化学填空题中等难度题查看答案及解析
-
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++S2O82﹣+H2O→MnO4﹣+SO42﹣+H+,下列说法不正确的是( )
A. 可以利用该反应检验Mn2+
B. 氧化性比较:S2O82﹣>MnO4﹣
C. 该反应中酸性介质可以为盐酸
D. 若有0.1mol氧化产物生成,则转移电子0.5mol
高三化学单选题中等难度题查看答案及解析
-
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应:Mn2++S2O
+H2O→MnO
+SO
+H+,下列说法不正确的是( )
A.可以利用该反应检验Mn2+
B.配平后的系数为2、5、8、2、10、16
C.该反应中酸性介质不能为盐酸
D.若有0.1mol还原产物生成, 则转移电子0.5mol
高三化学选择题简单题查看答案及解析
-
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应(未配平):Mn2+ +S2O82 一+H2O→ MnO4一+SO42 一+H+,下列说法不正确的是( )
A.氧化性比较:S2O82 一>MnO4一
B.氧化剂S2O82 一的摩尔质量为 192 g/mol
C.该反应中酸性介质可以为盐酸
D.若有0.1 mol氧化产物生成,则转移电子 0.5 mol
高三化学选择题困难题查看答案及解析
-
已知在酸性介质中,MnSO4 与(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82-→MnO4-+SO42-,下列说法正确的是,
A. 反应过程中,因消耗溶液中的H+反应后溶液pH 增大
B. 氧化性:S2O82->MnO4-
C. 该反应中酸性介质可以为盐酸
D. 0.1mol氧化剂参加反应,转移电子0.5mol
高三化学单选题困难题查看答案及解析
-
在酸性介质中,向MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下离子反应:2Mn2++5S2O82﹣+8X=2MnO42﹣+10SO42﹣+16H+,下列说法正确的是
A.X是H2O
B.还原性:SO42﹣>Mn2+
C.该反应中酸性介质可以为盐酸
D.每生成0.1molSO42﹣,转移电子0.05mol
高三化学选择题困难题查看答案及解析
-
已知在酸性介质中,MnSO与(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82—→MnO4—+SO42—,下列说法正确的是,
A. 反应过程中,因消耗溶液中的H+反应后溶液pH增大
B. 氧化性:S2O82—> MnO4—
C. 该反应中酸性介质可以为盐酸
D. 0.1mol氧化剂参加反应,转移电子0.5mol
高三化学单选题困难题查看答案及解析
-
向酸化过的MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82—+H2O―→MnO4—+SO42—+H+。下列说法不正确的是 ( )。
A.可以利用该反应检验Mn2+
B.氧化性比较:S2O82—>MnO4—
C.MnSO4溶液可以使用盐酸酸化
D.若有0.1 mol氧化产物生成,则转移电子0.5 mol
高三化学选择题中等难度题查看答案及解析