-
羰基硫COS的结构与CO2相似,广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。羰基硫的氢解反应和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g)  H2S(g)+ CO(g) △H=+7 kJ/mol
H2S(g)+ CO(g) △H=+7 kJ/mol
②水解反应: COS(g)+H2O(g)  H2S(g)+ CO2(g) △H = ?
H2S(g)+ CO2(g) △H = ?
已知反应中相关的化学键键能数据如下:
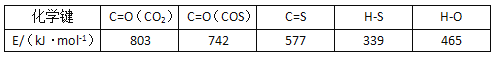
回答下列问题:
(1)羰基硫的结构式为:___________,
(2)已知热化学方程式CO(g)+H2O(g)  H2(g)+ CO2(g) △H3 则△H3 =__________kJ/mol。
H2(g)+ CO2(g) △H3 则△H3 =__________kJ/mol。
(3)COS的氢解反应的平衡常数K与温度T具有如下的关系式  ,式中a和b均为常数。
,式中a和b均为常数。
①如图中,表示COS氢解反应的直线为__________;
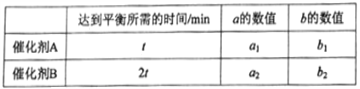

②一定条件下,催化剂A和B对COS的氢解反应均具有催化作用,相关数据如表所示:
则a1____a2 (填“>”或“<”或“=”)。
③某温度下,在体积不变的容器中,若COS和H2的起始体积比为1:V,平衡后COS和H2的体积比为1:10V,则此温度下该反应的化学平衡常数K=_________。(关于V的表达式)
(1)COS完全燃烧会生成大气污染物SO2。目前,科学家正在研究一种以乙烯作为还原剂的脱硫(SO2)方法,其脱硫机理如图2,脱硫率与温度、负载率(分子筛中催化剂的质量分数)的关系如图3。
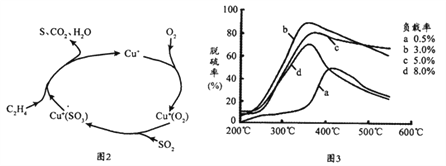
①该脱硫原理总反应的化学方程式为_________________________________________;
②据图3,为达到最佳脱硫效果,应采取的具体反应条件是________________________;
③根据a曲线在450℃以上的变化趋势,分析可能的原因是:______________________。
(5)为测定某工厂烟道气中SO2的含量,现将16.00 L烟道气缓慢通过1.00 L水,设SO2完全被吸收,且溶液体积不变。取出20.00 mL溶液,用1.18×10-3mol·L-1的饱和碘水与之反应,若恰好完全反应时消耗碘水19.07 mL,则该厂烟道气中SO2的含量为________________mg·L-1。
-
羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+ H2O(g) H2S(g) +CO2(g) △H=-34kJ/mol
H2S(g) +CO2(g) △H=-34kJ/mol
氢解反应:COS(g) +H2(g)  H2S(g)+CO(g) △H=+7kJ/mol。
H2S(g)+CO(g) △H=+7kJ/mol。
已知:2H2(g) +O2(g)=2H2O(g) △H=-484 kJ/mol。
写出表示CO燃烧热的热化学方程式:______________。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率____(填“增大”“减小”或“不变”,下同),COS 的转化率_______。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5 min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5 min 内,v(H2S)=_______mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________。
-
氧硫化碳(COS,结构类似于CO2)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。有多种方法可以脱氧硫化碳中的硫,其中氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g) + H2(g)⇌H2S(g) + CO(g) ΔH1 = + 7kJ/mol
②水解反应:COS(g) + H2O(g)⇌H2S(g) + CO2(g) ΔH2= -35 kJ/mol
请回答下列问题:
(1)氧硫化碳的电子式为____________。
(2)CO2和H2能反应生成CO和H2O(g),写出该反应的热化学方程式______________。
(3)在密闭恒温(高于100℃)恒容装置中进行水解反应,下列能说明达到平衡状态的是___________________。
A.混合气体密度不再改变 B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变 D. COS(g) 的浓度不变
(4)①上述氢解反应的平衡常数K随温度降低而________(填“增大”或“减小”)。
②某温度下,体积为2L的恒容体系中,物质的量分别为m mol、n mol的COS蒸气和H2气发生氢解,已知COS的转化率为α,则该温度下的平衡常数K=___________(用m、n、α等符号表示)。
(5)某科研小组研究改进催化剂TiO2/Al2O3和温度对COS水解的影响,得到如图图像:
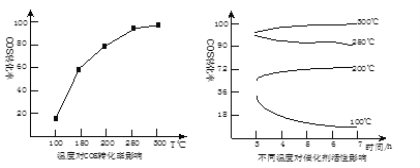
COS水解的最佳温度是 __________ ;理由是 ________ 。
-
(1)羰基硫(COS)多产生于煤化工合成气中,能引起催化剂中毒,可通过水解反应除去,其热化学方程式为COS(g)+H2O(g) H2S(g)+CO2(g) △H。相关的化学键键能数据如下表所示:
H2S(g)+CO2(g) △H。相关的化学键键能数据如下表所示:
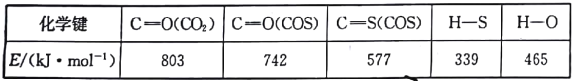
则△H为___。
(2)近期太阳能的利用又有新进展。利用太阳能由CO2制取C的原理如图所示,若重整系统发生的反应中 =4,则重整系统中发生反应的化学方程式为:___。
=4,则重整系统中发生反应的化学方程式为:___。

(3)已知:常温下,Ka(HCOOH)=1.77×10-4,Ka(CH3COOH)=1.75×10-5,Kb(NH3·H2O)=1.76×10-5。下列说法正确的是___(填字母代号)。
A.浓度均为0.1mol·L-1的HCOONa和NH4Cl溶液中阳离子的物质的量浓度之和:前者大于后者
B.用相同浓度的NaOH溶液分别滴定等体积、pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C.0.2mol·L-1CH3COONa与0.1mol·L-1盐酸等体积混合后的溶液中(pH<7):c(CH3COO-)>c(Cl-)>c(CH3COOH)>C(H+)
D.0.2mol·L-1HCOOH与0.1mol·L-1 NaOH等体积混合后的溶液中:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+)
(4)NaHS可用作污水处理的沉淀剂。已知:25℃时,H2S的电离常数Ka1=1.0×10-7、Ka2=7.0×10-15,反应Hg2+(aq)+HS-(aq) HgS(s)+H+(aq)的平衡常数K=1.75×1038。则Ksp(HgS)=___。
HgS(s)+H+(aq)的平衡常数K=1.75×1038。则Ksp(HgS)=___。
-
硫化氢(H2S)的转化是资源利用和环境保护的重要研究课题。
(1)H2S和CO混合加热可制得羰基硫(COS)。已知羰基硫与CO2的结构相似,但它能在O2中完全燃烧。羰基硫可作粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。制备羰基硫反应方程式为:
CO(g)+H2S(g) COS(g)+H2(g)
COS(g)+H2(g)
①羰基硫的电子式为_________
②羰基硫分子中三种原子半径由大到小的顺序________________
③羰基硫的沸点比二氧化碳_________(填“高或低”)理由是_____________________
④写出羰基硫在O2中完全燃烧的化学方程式__________________________________
(2)H2S具有还原性,在硫酸存在的条件下,能与KMnO4反应生成一种淡黄色沉淀,写出该反应的离子方程式________________________________。
-
人们在研究金星大气成分时发现金星大气中有一种称为羰基硫(COS)的分子,其结构与CO2类似,羰基硫是一种与生命密切相关的物质,下列有关COS的推测不正确的是
A.COS分子是含有极性键的极性分子
B.COS的电子式为:
C.COS的分子中所有原子满足8电子稳定结构
D.COS分子中三个原子处于同一直线上
-
二氧化碳在石油开采、人工降雨、消防、有机合成等领域有着广泛的应用。
(1)甲醇是重要的化工原料。利用合成气(CO、CO2、H2)在催化剂作用下合成甲醇,已知反应相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(KJ/mol) | 436 | 343 | 803 | 465 | 413 |
写出CO2和H2在催化剂作用下生成CH3OH(g)和H2O(g)的热化学方程式________
(2)CH4超干重整CO2的催化转化原理示意图如图所示:
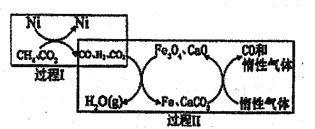
①过程Ⅰ,生成1molH2时吸收123.5kJ热量,其热化学方程式是_______
②过程Ⅱ,实现了含然物种与含碳物种的分离,生成H2O(g)的化学方程式是________
-
CO是生产羰基化学品的基本原料, 850℃时,在恒容密闭容器中通入CO和H2O(g),发生:CO(g)+H2O(g)  H2(g)+CO2(g)
H2(g)+CO2(g)  H<0,测定浓度随时间关系如下表:
H<0,测定浓度随时间关系如下表:
| t/min | c(CO)/ mol·L-1 | c(H2O)/ mol·L-1 |
| 0 | 0.30 | 0.20 |
| 2 | \ | 0.10 |
| 3 | 0.18 | \ |
| 4 | \ | 0.08 |
回答下列问题
(1)t=3min时,υ(正)____________υ(逆)(选填:“>”,“<”,“=”)。
(2)0~2min,CO的平均反应速率为 ____________。
(3)上述反应中的CO平衡转化率为______;该温度下反应的平衡常数为______。
(4)850℃时,以下表中不同的起始浓度在体积可变的密闭容器中进行反应,其CO平衡转化率与原平衡相同的是______(选填a、b、c、d)。
| c(CO) | c(H2O) | c(H2) | c(CO2) |
| a | 2 | 1 | 1 | 1 |
| b | 0.6 | 0.4 | 0 | 0 |
| c | 0.2 | 0 | 0.1 | 0.1 |
| d | 1 | 1 | 1 | 1 |
(5)在一定条件下,发生下列反应:CO(g)+H2O(g)  H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示
H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示
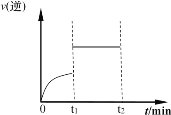
则t1时改变的某种反应条件可能是_____(填序号)。
a.增大CO浓度 b.加压
c.恒容时充入氩气 d.使用催化剂
-
化学与生产、生活、社会密切相关,下列说法正确的是( )
A.少量的生石灰能作为鸡舍和猪栏的消毒剂
B.石油裂化和裂解制取乙烯、丙烯等化工原料不涉及化学变化
C.误食重金属盐引起的人体中毒,可以喝大量的食盐水解毒
D.常用危险化学品标签中的阿拉伯数字主要表示的是危险级别
-
水星大气中含有一种被称为硫化羰(化学式为COS)的物质。已知硫化羰与CO2的结构相似,但能在O2中完全燃烧,下列有关硫化羰的说法正确的是
A. OCS的电子式为
B. OCS分子中三个原子位于同一直线上
C. OCS的沸点比CO2的低
D. OCS分子中含有1个σ键和1个π键
H2S(g)+ CO(g) △H=+7 kJ/mol
H2S(g)+ CO2(g) △H = ?

H2(g)+ CO2(g) △H3 则△H3 =__________kJ/mol。
,式中a和b均为常数。







