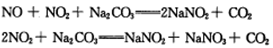-
燃煤造成的SO2的大量排放已经给我们的生存环境造成了严重破坏,科学研究发现:一定条件下,通过下列反应可实现燃煤烟气中硫的回收。
2CO(g)+SO2(g)  2CO2 (g)十S(1) △H
2CO2 (g)十S(1) △H
(1)已知:2CO(g)十O2 (g)=2 CO2 (g) △H1=-566 kJ/mol
S(1)+O2(g)= SO2(g) △H2=-296 kJ/mol,
则反应2CO(g)+SO2(g)  2CO2(g)+S(1) △H=__________;
2CO2(g)+S(1) △H=__________;
(2)燃煤烟气中硫的回收反应的平衡常数表达式K=__________。在温度和容积不变时,下列说法正确的是__________(填字母序号)。
A.容器内压强不再改变时,反应达到平衡状态
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.当n((CO):n(SO2):n(CO2)=2:1:2时,反应达到平衡状态
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
(3)假设在容器中发生上述反应,下列能提高SO2转化率的是__________;(填字母序号)。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)SO2尾气处理的方法之一是将尾气直接通入NaOH溶液中。若将1 mol SO2气体通入1L2 mol/L的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为__________;
(5)尾气中的CO可以制成CO一空气燃料电池。CO一空气燃料电池中使用的电解质是掺杂Y2O3的ZrO2晶体,它在高温下能传导O2-。该电池负极的电极反应式为__________;总反应式为__________.
-
燃煤造成的SO2的大量排放已经给我们的生存环境造成了严重破坏,科学研究发现:一定条件下,通过下列反应可实现燃煤烟气中硫的回收。
2CO(g)+SO2(g) 2CO2 (g)十S(1) △H
2CO2 (g)十S(1) △H
(1)已知:2CO(g)十O2 (g)=2 CO2 (g) △H1=-566 kJ/mol
S(1)+O2(g)= SO2(g) △H2=-296 kJ/mol,
则反应2CO(g)+SO2(g)  2CO2(g)+S(1) △H=__________;
2CO2(g)+S(1) △H=__________;
(2)燃煤烟气中硫的回收反应的平衡常数表达式K=__________。在温度和容积不变时,下列说法正确的是__________(填字母序号)。
A.容器内压强不再改变时,反应达到平衡状态
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.当n((CO):n(SO2):n(CO2)=2:1:2时,反应达到平衡状态
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
(3)假设在容器中发生上述反应,下列能提高SO2转化率的是________;
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)SO2尾气处理的方法之一是将尾气直接通入NaOH溶液中。若将1 mol SO2气体通入1L2 mol/L的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为__________;
-
燃煤烟气中含有一定量的二氧化硫,会造成大气污染。一定条件下,通过下列反应可以实现燃煤烟气中硫的回收:2CO(g)+SO2(g) 2CO2(g)+S(l) ∆H, 请回答:
2CO2(g)+S(l) ∆H, 请回答:
⑴已知CO(g)+ O2(g)=CO2(g) △H1=-a kJ·mol-1
O2(g)=CO2(g) △H1=-a kJ·mol-1
S(s)+O2(g)=SO2(g) ∆H2=-b kJ·mol-1
S(l)=S(s) ∆H3=-c kJ·mol-1
则△H=_______kJ·mol-1。
⑵一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,在不同条件下进行反应:2CO(g)+SO2(g) 2CO2(g)+S(l),反应体系总压强随时间的变化如图所示:
2CO2(g)+S(l),反应体系总压强随时间的变化如图所示:
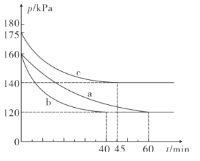
①图中三组实验从反应开始至达到平衡时的反应速率v(CO)由大到小的次序为___( 填实验序号); 与a组相比,c组改变的实验条件可能是___。
②若b组反应进行到40min时达到平衡状态,此时测得容器中气体的密度比反应前减少了12.8 g·L-1,则CO的物质的量浓度c(CO)=___,反应在此条件下的化学平衡常数K=___
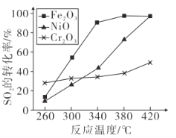
⑶其他条件相同、催化剂不同时,SO,的转化率随反应温度的变化如下图,260°C时,______(填Fe2O3、NiO或Cr2O3)作催化剂反应速率最快;Fe2O3和NiO作催化剂均使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是_______。
⑷SO2—O2质子交换膜燃料电池实现了制硫酸、发电、环保三项目标,此电池的负极反应式为____________。
-
(9分)燃煤锅炉将排放大量SO2,污染大气造成公害,常采用两种方法消除燃煤SO2的污染。
(1)使排放的烟气通过氨水洗涤,化学方程式是________
(2)在煤中加适量石灰,使SO2与石灰反应,化学方程式为________,
该生成物仍可被氧化而成稳定的石膏,化学方程式为________ 。
-
研究NOx(氮的氧化物)SO2、CO等大气污染气体的测量及处理具有重要意义。
(1)下图是 反应过程中能量示意图。
反应过程中能量示意图。
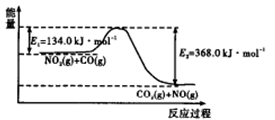
该反应的焓变
(2)一定条件下,通过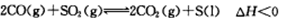 可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。
可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。
①求以v(CO2)表示的反应速率为________。
②该反应的平衡常数的表达式为:K=________。
③若想加快正反应速率的同时提高SO2的转化率,可以采用的方法是________。
(3)工业上常用Na2CO3溶液吸收法处理氮的氧化物(以NO和NO2的混合物为例)。
已知:NO不能与Na2CO3溶液反应。
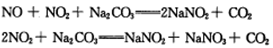
若用足量的Na2CO3溶液完全吸收NO和NO2的混合物,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则混合气体中NO和NO2的体积比为________。
-
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)
 2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
-
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
-
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g) +2CO(g) 2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l) △H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其它条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其它条件不变,使用不同催化剂,该反应的平衡常数不变
-
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2CO2(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
A. 平衡前,随着反应的进行,容器内压强始终不变
B. 平衡时,其他条件不变,分离出硫,正反应速率加快
C. 平衡时,其他条件不变,升高温度可提高SO2的转化率
D. 其他条件不变,使用不同催化剂,该反应平衡常数不变
-
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)
 2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO2的转化率
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
2CO2 (g)十S(1) △H
2CO2(g)+S(1) △H=__________;


 反应过程中能量示意图。
反应过程中能量示意图。
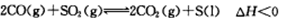 可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。
可以实现燃煤烟气中硫的回收。某研究小组向2L某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中通入CO和SO2,10分钟后测得容器CO2的物质的量为0.9mol。