-
(9分)燃煤锅炉将排放大量SO2,污染大气造成公害,常采用两种方法消除燃煤SO2的污染。
(1)使排放的烟气通过氨水洗涤,化学方程式是________
(2)在煤中加适量石灰,使SO2与石灰反应,化学方程式为________,
该生成物仍可被氧化而成稳定的石膏,化学方程式为________ 。
高三化学填空题简单题查看答案及解析
-
煤燃烧排放的烟气含有SO2和NOx,大量排放烟气形成酸雨、污染大气,因此对烟气进行脱硫、脱硝,对环境保护有重要意义。回答下列问题:
Ⅰ.利用CO脱硫
(1)工业生产可利用CO气体从燃煤烟气中脱硫,则25℃时CO从燃煤烟气中脱硫的热化学方程式2CO(g)+SO2(g)⇌2CO2(g)+S(s)的焓变△H=_____________。25℃,100kPa时,由元素最稳定的单质生成1mol纯化合物时的反应热称为标准摩尔生成焓,已知一些物质的“标准摩尔生成焓”如下表所示:
物质
CO(g)
CO2(g)
SO2(g)
标准摩尔生成焓∆fHm(25℃)/kJ∙mol-1
-110.5
-393.5
-296.8
(2)在模拟脱硫的实验中,向多个相同的体积恒为2L的密闭容器中分别通入2.2mol CO和1mol SO2气体,在不同条件下进行反应,体系总压强随时间的变化如图所示。
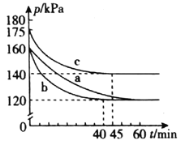
①在实验b中,40 min达到平衡,则0~40 min用SO2表示的平均反应速率v(SO2)=_______。
②与实验a相比,实验b可能改变的条件为_______________,实验c可能改变的条件为_________________。
Ⅱ.利用NH3脱硝
(3)在一定条件下,用NH3消除NO污染的反应原理为:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)△H=-1807.98kJ·mol-1。在刚性容器中,NH3与NO的物质的量之比分别为X、Y、Z(其中X<Y<Z),在不同温度条件下,得到NO脱除率(即NO转化率)曲线如图所示。
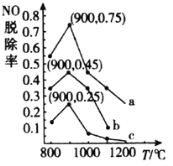
①NH3与NO的物质的量之比为X时对应的曲线为_____________(填“a”“b”或“c”)。
②各曲线中NO脱除率均先升高后降低的原因为__________。
③900℃条件下,设Z=
,初始压强p0,则4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)的平衡常数Kp=_____________(列出计算式即可)。
Ⅲ.利用NaCIO2脱硫脱硝
(4)利用NaClO2的碱性溶液可吸收SO2和NO2(物质的量之比为1:1)的混合气体,自身转化为NaCl,则反应的离子方程式为________________。
高三化学综合题困难题查看答案及解析
-
燃煤造成的SO2的大量排放已经给我们的生存环境造成了严重破坏,科学研究发现:一定条件下,通过下列反应可实现燃煤烟气中硫的回收。
2CO(g)+SO2(g)
2CO2 (g)十S(1) △H
(1)已知:2CO(g)十O2 (g)=2 CO2 (g) △H1=-566 kJ/mol
S(1)+O2(g)= SO2(g) △H2=-296 kJ/mol,
则反应2CO(g)+SO2(g)
2CO2(g)+S(1) △H=__________;
(2)燃煤烟气中硫的回收反应的平衡常数表达式K=__________。在温度和容积不变时,下列说法正确的是__________(填字母序号)。
A.容器内压强不再改变时,反应达到平衡状态
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.当n((CO):n(SO2):n(CO2)=2:1:2时,反应达到平衡状态
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
(3)假设在容器中发生上述反应,下列能提高SO2转化率的是__________;(填字母序号)。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)SO2尾气处理的方法之一是将尾气直接通入NaOH溶液中。若将1 mol SO2气体通入1L2 mol/L的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为__________;
(5)尾气中的CO可以制成CO一空气燃料电池。CO一空气燃料电池中使用的电解质是掺杂Y2O3的ZrO2晶体,它在高温下能传导O2-。该电池负极的电极反应式为__________;总反应式为__________.
高三化学填空题困难题查看答案及解析
-
燃煤造成的SO2的大量排放已经给我们的生存环境造成了严重破坏,科学研究发现:一定条件下,通过下列反应可实现燃煤烟气中硫的回收。
2CO(g)+SO2(g)
2CO2 (g)十S(1) △H
(1)已知:2CO(g)十O2 (g)=2 CO2 (g) △H1=-566 kJ/mol
S(1)+O2(g)= SO2(g) △H2=-296 kJ/mol,
则反应2CO(g)+SO2(g)
2CO2(g)+S(1) △H=__________;
(2)燃煤烟气中硫的回收反应的平衡常数表达式K=__________。在温度和容积不变时,下列说法正确的是__________(填字母序号)。
A.容器内压强不再改变时,反应达到平衡状态
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.当n((CO):n(SO2):n(CO2)=2:1:2时,反应达到平衡状态
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
(3)假设在容器中发生上述反应,下列能提高SO2转化率的是________;
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)SO2尾气处理的方法之一是将尾气直接通入NaOH溶液中。若将1 mol SO2气体通入1L2 mol/L的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为__________;
高三化学填空题困难题查看答案及解析
-
燃煤烟气中含有大量SO2和NO是大气主要污染物,需要经过净化处理后才能排放。
(1)尿素[CO(NH2)2]可用于SO2和NO的吸收。
①已知:CO(NH2)2(aq)+2H2O(l)═(NH4)2CO3(aq) △H1=akJ•mol-1
(NH4)2CO3(aq)+SO2(g)═(NH4)2SO3(aq)+CO2(g) △H2=bkJ•mol-1
2(NH4)2SO3(aq)+O2(g)═2(NH4)2SO4(aq) △H3=ckJ•mol-1
反应2CO(NH2)2(aq)+4H2O(l)+O2(g)+2SO2(g)═2(NH4)2SO4(aq)+2CO2(g)的△H=__kJ•mol-1。
②尿素[CO(NH2)2]可将NO转化为N2和CO2而除去,该反应的化学方程式为__。
(2)利用电化学联合处理法可实现SO2和NO同时除去,工作原理如图所示。
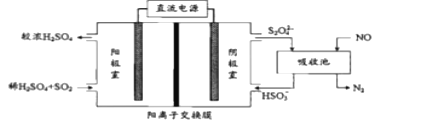
①阳极的电极反应式为__。
②若工作前后阴极室成分不变,被处理的SO2和NO的在相同条件下的体积比V(SO2):V(NO)=__。
(3)用石灰乳与NaClO3的混合物吸收SO2和NO可得到CaSO4和Ca(NO3)2,吸收剂的浓度和反应温度对吸收率及吸收产物有影响。
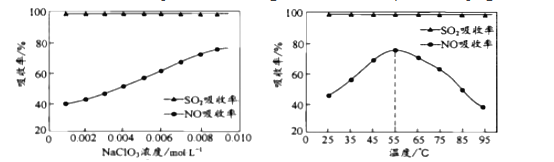
①NaClO3浓度变化对SO2和NO吸收率影响如图所示,NaClO3浓度变化对SO2吸收率影响比NO吸收率影响小的原因是___。
②温度对SO2和NO吸收率影响如图所示,当温度高于55℃时,随着温度升高NO吸收率下降,其原因是___。
高三化学综合题中等难度题查看答案及解析
-
燃煤烟气中含有一定量的二氧化硫,会造成大气污染。一定条件下,通过下列反应可以实现燃煤烟气中硫的回收:2CO(g)+SO2(g)
2CO2(g)+S(l) ∆H, 请回答:
⑴已知CO(g)+
O2(g)=CO2(g) △H1=-a kJ·mol-1
S(s)+O2(g)=SO2(g) ∆H2=-b kJ·mol-1
S(l)=S(s) ∆H3=-c kJ·mol-1
则△H=_______kJ·mol-1。
⑵一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,在不同条件下进行反应:2CO(g)+SO2(g)
2CO2(g)+S(l),反应体系总压强随时间的变化如图所示:
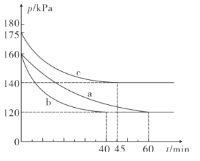
①图中三组实验从反应开始至达到平衡时的反应速率v(CO)由大到小的次序为___( 填实验序号); 与a组相比,c组改变的实验条件可能是___。
②若b组反应进行到40min时达到平衡状态,此时测得容器中气体的密度比反应前减少了12.8 g·L-1,则CO的物质的量浓度c(CO)=___,反应在此条件下的化学平衡常数K=___
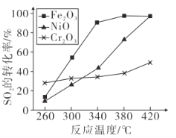
⑶其他条件相同、催化剂不同时,SO,的转化率随反应温度的变化如下图,260°C时,______(填Fe2O3、NiO或Cr2O3)作催化剂反应速率最快;Fe2O3和NiO作催化剂均使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是_______。
⑷SO2—O2质子交换膜燃料电池实现了制硫酸、发电、环保三项目标,此电池的负极反应式为____________。
高三化学综合题困难题查看答案及解析
-
二氧化硫是大气的主要污染物之一。催化还原SO2不仅可以消除SO2的污染,还可以得到工业原料S。燃煤烟气中硫的回收反应为:2CO(g)+SO2(g)
2CO2(g)+S(l) △H。
(1)已知:2CO(g)+O2(g)===2CO2(g) △H1=-566.0kJ·mol-1
S(l)+O2(g)===SO2(g) △H2=-296.8 kJ·mol-1
则硫的回收反应的△H=___________ kJ·mol-1。
(2)其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图所示。260℃时,___________(填“La2O3”、“NiO”或“TiO2”)的催化效率最高。La2O3和NiO作催化剂均可能使SO2的转化率达到很高,不考虑价格因素,选择La2O3的主要优点是___________。
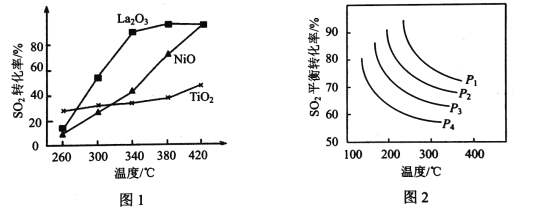
(3)一定条件下,若在恒压密闭容器中发生硫的回收反应,SO2的平衡转化率与温度、压强的关系如图所示,则P1、P2、P3、P4由大到小的顺序为___________;某温度下,若在恒容密闭容器中,初始时c(CO)=2 a mol·L-1,c(SO2)= a mol·L-1,SO2的平衡转化率为80%,则该温度下反应的化学平衡常数为___________。
(4)某实验小组为探究烟气流速、温度对该反应的影响,用La2O3作催化剂,分别在两种不同烟气流量、不同温度下进行实验。实验结果显示:在260℃时,SO2的转化率随烟气流量增大而减小,其原因是___________;在380℃时,SO2的转化率随烟气流量增大而增大,其原因是___________。
(5)工业上常用Na2SO3溶液吸收烟气中的SO2,将烟气通入1.0 mol·L-1的N2SO3溶液,当溶液pH约为6时,吸收SO2的能力显著下降此时溶液中c(HSO3-)c︰(SO32-)=___________。(已知H2SO3的Ka1=1.5×10-2、Ka2=1.0×10-7)
高三化学综合题困难题查看答案及解析
-
二氧化硫是大气的主要污染物之一。催化还原SO2不仅可以消除SO2的污染,还可以得到工业原料S。燃煤烟气中硫的回收反应为:2CO(g)+SO2(g)
2CO2(g)+S(l) △H。
(1)已知:2CO(g)+O2(g)===2CO2(g) △H1=-566.0kJ·mol-1
S(l)+O2(g)===SO2(g) △H2=-296.8 kJ·mol-1
则硫的回收反应的△H=___________ kJ·mol-1。
(2)其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图所示。260℃时,___________(填“La2O3”、“NiO”或“TiO2”)的催化效率最高。La2O3和NiO作催化剂均可能使SO2的转化率达到很高,不考虑价格因素,选择La2O3的主要优点是___________。
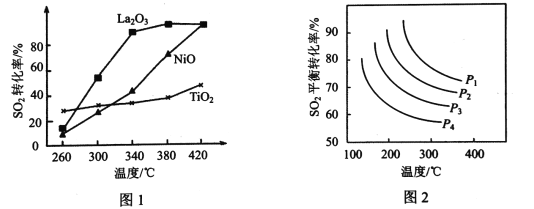
(3)一定条件下,若在恒压密闭容器中发生硫的回收反应,SO2的平衡转化率与温度、压强的关系如图所示,则P1、P2、P3、P4由大到小的顺序为___________;某温度下,若在恒容密闭容器中,初始时c(CO)=2 a mol·L-1,c(SO2)= a mol·L-1,SO2的平衡转化率为80%,则该温度下反应的化学平衡常数为___________。
(4)某实验小组为探究烟气流速、温度对该反应的影响,用La2O3作催化剂,分别在两种不同烟气流量、不同温度下进行实验。实验结果显示:在260℃时,SO2的转化率随烟气流量增大而减小,其原因是___________;在380℃时,SO2的转化率随烟气流量增大而增大,其原因是___________。
(5)工业上常用Na2SO3溶液吸收烟气中的SO2,将烟气通入1.0 mol·L-1的N2SO3溶液,当溶液pH约为6时,吸收SO2的能力显著下降此时溶液中c(HSO3-)c︰(SO32-)=___________。(已知H2SO3的Ka1=1.5×10-2、Ka2=1.0×10-7)
高三化学综合题困难题查看答案及解析
-
党的十九大报告中提出要建设美丽中国,推进绿色发展。燃煤烟气(污染气体包括NOx、CO、SO2等)的综合治理是解决大气污染的主要途径。
(1)用CH4催化还原氮氧化物可以消除其污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ·mol-1
③H2O(g)=H2O(1)△H=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式__________。
(2)选择合适的催化剂,在一定条件下可对部分燃煤烟气回收,其主要反应是:2CO(g)+SO2(g)
2CO2(g)+S(1)△H=-270kJ·mol-1
①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是__________。
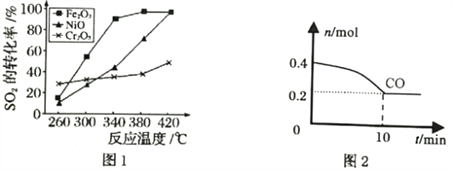
②T℃Fe2O3催化作用下,将等物质的量的CO和SO2充入容积为2L的密闭容器中,保持温度和体积不变,反应过程中CO的物质的量随时间变化如图2所示。10min内该反应的速率v(SO2)=________;T℃时该化学反应的平衡常数K=______;保持容积固定,若升高温度,反应的平衡常数_________(填“增大”“减小”或“不变”,下同),容器内混合气体的密度__________。
(3) 图3是用食盐水做电解液电解烟气脱氮的原理图,NO被阳极产生的氧化性物质氧化为NO3-,尾气经NaOH溶液吸收排入空气。
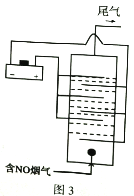
①NO被氧化的离子方程式是__________。
②若通入的烟气2240L(标准状况),烟气中NO含量为15%,(假设烟气中无其他含氮气体),测得溶液中含有NO3-的物质的量为1.47mol,则NO除去率为__________%。
高三化学综合题困难题查看答案及解析
-
燃煤的烟气中常含有大量的NOx、CO、SO2等有害气体,治理污染、消除有害气体对环境的影响是化学工作者研究的重要课题。
Ⅰ.已知氮氧化物可采用强氧化剂Na2S2O8氧化脱除,过程如下所示:
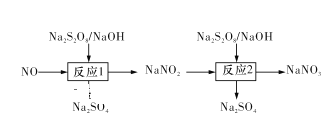
(1)写出反应1的离子方程式:____ 。
(2)反应2为NO2-+S2O82-+2OH-=NO3-+2SO42-+H2O。此反应在不同温度下达到平衡时,NO2-的脱除率与Na2S2O8初始浓度的关系如图1所示。
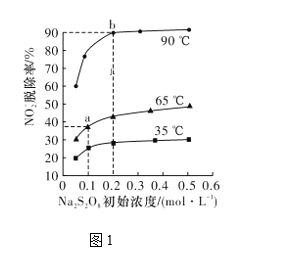
①比较a、b点的反应速率:va正____vb逆(填“>”“<”或“=”)。
②根据图像可以判断该反应为吸热反应,理由是____________。
Ⅱ.沥青混凝土可作为反应2CO(g)+O2(g)
2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
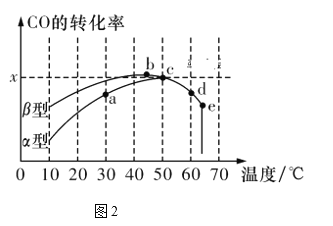
(3)下列关于图2的说法正确的是________。
A.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
B.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
C.a、b、c、d四点中,达到平衡状态的只有b、c两点
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
(4)已知c点时容器中O2浓度为0.02 mol/L,则50 ℃时,在α型沥青混凝土中CO转化反应的平衡常数K=_____________(用含x的代数式表示)。
Ⅲ.利用图3所示装置(电极均为惰性电极)可吸收SO2。
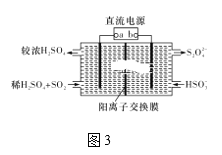
(5)直流电源b极为____,阳极发生的反应为______。
高三化学综合题中等难度题查看答案及解析