能源是当今社会发展的三大支柱之一。有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为
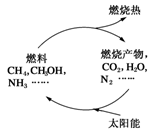
A.化学能 B.电能 C.生物质能 D.热能
高三化学选择题简单题
能源是当今社会发展的三大支柱之一。有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为

A.化学能 B.电能 C.生物质能 D.热能
高三化学选择题简单题
能源是当今社会发展的三大支柱之一。有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为

A.化学能 B.电能 C.生物质能 D.热能
高三化学选择题简单题查看答案及解析
能源是当今社会发展的三大支柱之一。有专家提出:如果能够利用太阳能使燃料燃烧产物(如CO2、H2O、N2等)重新组合(如下图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为( )
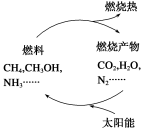
A.化学能 B.热能 C.生物能 D.电能
高三化学选择题中等难度题查看答案及解析
能源是当今社会发展的三大支柱之一。有专家提出:如果能够利用太阳能使燃料燃烧产物,如CO2、H2O、N2等重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为
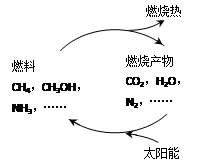
A.化学能 B.热能
C.生物能 D.电能
高三化学选择题中等难度题查看答案及解析
利用太阳能、风能、生物质能等可再生能源,转化利用二氧化碳设计出适合高效清洁的合成燃料分子结构,实现CO2+H2O→CxHy的分子转化,生产合成甲烷、醇醚燃料、烷烃柴油、航空燃油等可再生合成燃料。因此二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
(1)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
CO(g)+3H2(g)CH4(g)+H2O(g) △H1=-206.2kJ/mol
CO(g)+H2O(g)CO2(g)+H2(g) ∆H2
若CO2氧化H2生成0.1molCH4(g)和一定量的H2O(g),整个过程中放出的热量为16.5kJ,则△H2=__。
(2)合成二甲醚的总反应为2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) ∆H=-122.4kJ·mol-1。某温度下,将2.0molCO2(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图所示,则p1__(填“>”“<"或“=”,下同)p2。若T3、p3,T4、p4时平衡常数分别为K3、K4则K3__K4,T1、p1时H2的平衡转化率为___。(结果保留三位有效数字)
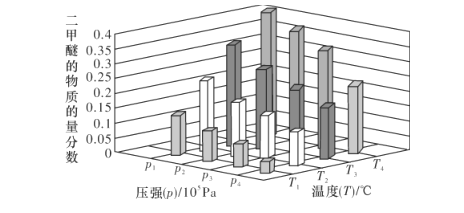
(3)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,下列反应能自发进行:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。
①该反应△H__(填“>”“<”或“=”)0。
②下列叙述能说明此反应达到平衡状态的是__(填字母代号)。
a.混合气体的平均相对分子质量保持不变
b.1molCO2生成的同时有3molH-H键断裂
c.CO2的转化率和H2的转化率相等
d.混合气体的密度保持不变
③上述反应常用CuO和ZnO的混合物作催化剂。相同的温度和时间段内,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率影响的实验数据如下表所示:
| ω(CuO)% | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| CH3OH的产率 | 25% | 30% | 35% | 45% | 50% | 65% | 55% | 53% | 50% |
| CO2的转化率 | 10% | 13% | 15% | 20% | 35% | 45% | 40% | 35% | 30% |
由表可知,CuO的质量分数为__催化效果最佳。
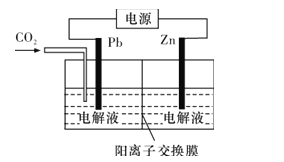
(4)CO2可用于工业制备草酸锌,其原理如图所示(电解液不参加反应),Zn电极是__极。已知在Pb电极区得到ZnC2O4,则Pb电极上的电极反应式为__。
高三化学综合题中等难度题查看答案及解析
(14分)发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H________(填“增大”、“减小”或“不变”),判断的理由是________。
(2)CO2制备甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH=-49.0kJ·mol-1,在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如右图所示。
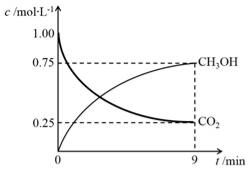
①该反应化学平衡常数K的表达式是________。
②0~9min时间内,该反应的平均反应速率ν(H2)=________。
③在相同条件下,密闭容器的体积缩小至0.5L时,此反应达平衡时放出的热量(Q)可能是________(填字母序号)kJ。
a.0<Q<29.5
B.29.5<Q<36.75
C.36.75<Q<49
D.49<Q<98
④在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如右图所示,L和X分别表示温度或压强。
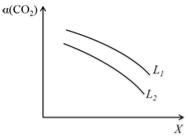
X表示的物理量是。判断L1与L2的大小关系。
(3)科学家用氮化镓材料与铜组装如右图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.
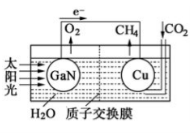
写出铜电极表面的电极反应式,为提高该人工光合系统的工作效率,可向装置中加入少量(选填“盐酸”或“硫酸”).
(4)利用CO2和NH3为原料也合成尿素,在合成塔中的主要反应可表示如下:
反应①:2NH3(g)+CO2(g)=NH2CO2NH4(s)△H1=__________________
反应②:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
总反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-86.98kJ·mol-1;
则反应①的△H1=_______________。
(5)现将amol铁和bmol铜的混合物与含有cmolHNO3的稀溶液充分反应,设还原产物为NO。下列结论不正确的是(填序号)
A.若剩余金属0.5amol,则氧化产物为一种或二种
B.若只有一种氧化产物,则3c=8a
C.若有二种氧化产物,被还原的硝酸物质的量为0.25cmol
D.若有三种氧化产物,被还原的硝酸物质的量为0.25cmol
高三化学简答题极难题查看答案及解析
发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g) CO(g)+H2(g)可有效提高能源利用率, 若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H ________(填“增大”、“减小”或“不变”)。
(2)CO2制备甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g); ΔH=-49.0 kJ·mol-1,
在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g) 和CH3OH(g)
浓度随时间变化如图1所示
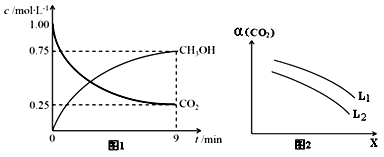
①0~9min时间内,该反应的平均反应速率ν(H2) = _________________________。
②在相同条件下,密闭容器的体积压缩至0.5 L时,此反应达平衡时放出的热量(Q)可能是________(填字母序号)kJ。
a. 0 < Q < 29.5 b. 29.5 < Q < 36.75 c. 36.75 < Q < 49 d. 49 < Q < 98
③在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如图2所示,L和X 分别表示温度或压强。
i. X表示的物理量是 ________________ 。
ii. 判断L1与L2的大小关系,并简述理由:________。
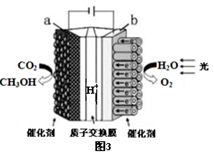
(3)利用铜基催化剂光照条件下由CO2和H2O制备CH3OH的装置示意图如图3所示,该装置工作时阴极的电极反应式是_____________________。
(4)利用CO2和NH3为原料也合成尿素,在合成塔中的主要反应可表示如下:
反应①:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1= __________________。
反应②:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
总反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H=-86.98kJ·mol-1;
则反应①的△H1=_______________。
高三化学填空题极难题查看答案及解析
(12分)能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。

① Ni原子的价电子排布式是▲。
② 该合金储氢后,含1mol La的合金可吸附H2的数目为▲。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是▲。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是▲ 。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构。该阴离子的电子式是▲,其中心原子N的杂化方式是▲。
高三化学填空题中等难度题查看答案及解析
能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。
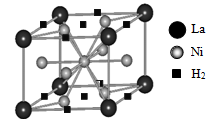
① Ni原子的价电子排布式是________________________________________________________________________________________________________________ 。
② 该合金储氢后,含1mol La的合金可吸附H2的数目为________________________________________________ 。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是________________________________________________________________________________________________________________ 。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是________________________________________________________ 。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构。该阴离子的电子式是________________________________________________ ,其中心原子N的杂化方式是________________________________ 。
(4)在金刚石晶体的一个晶胞(如图1)中,含有________________ ________________________________________个碳原子。在二氧化硅晶体的一个晶胞中,含有________________________________________ 个化学键。原子晶体能否形成最密堆积结构,原因是________________________________________________________________________________________________________________________________________________________________________________________________________________ 。
(5)铁晶体的晶胞结构(如图2):若铁原子的半径是r cm,则铁的密度是________________________________ 。

高三化学填空题困难题查看答案及解析
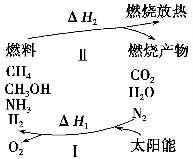
为保护环境并缓解能源危机,专家提出利用太阳能促使燃烧循环使用的构想,转化关系如图所示。
已知:
(1)过程Ⅰ可用如下反应表示:①2CO22CO+O2
②2H2O(g) 2H2+O2
③2N2+6H2O4NH3+3O2
④2CO2+4H2O2CH3OH+3O2
⑤2CO+4H2O________+3O2。
(2)25 ℃时,a g CH4完全燃烧释放出b kJ热量。下列说法不正确的是( )。
A.过程Ⅰ是将太阳能转化成化学能
B.反应⑤的另一种产物为CH4
C.ΔH1=-ΔH2
D.表示甲烷燃烧热的热化学反应方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-16b kJ·mol-1
高三化学选择题简单题查看答案及解析
为保护环境并缓解能源危机,专家提出利用太阳能促使燃烧循环使用的构想,转化关系如图所示。
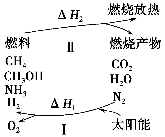
已知:
(1)过程Ⅰ可用如下反应表示:①2CO22CO+O2
②2H2O(g)2H2+O2
③2N2+6H2O4NH3+3O2
④2CO2+4H2O2CH3OH+3O2
⑤2CO+4H2O________+3O2。
(2)25 ℃时,a g CH4完全燃烧释放出b kJ热量。下列说法不正确的是( )。
A.过程Ⅰ是将太阳能转化成化学能
B.反应⑤的另一种产物为CH4
C.ΔH1=-ΔH2
D.表示甲烷燃烧热的热化学反应方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-16b kJ·mol-1
高三化学填空题中等难度题查看答案及解析