已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如下图:
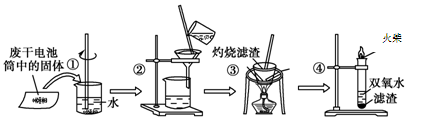
下列说法不正确的是
A. 步骤①②的名称分别为溶解、过滤
B. 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒
C. 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同
D. 步骤④的离子方程式为2Fe2++2H++H2O2 = 2Fe3++2H2O
高三化学选择题困难题
已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如下图:

下列说法不正确的是
A. 步骤①②的名称分别为溶解、过滤
B. 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒
C. 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同
D. 步骤④的离子方程式为2Fe2++2H++H2O2 = 2Fe3++2H2O
高三化学选择题困难题
已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如下图:

下列说法不正确的是
A. 步骤①②的名称分别为溶解、过滤
B. 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒
C. 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同
D. 步骤④的离子方程式为2Fe2++2H++H2O2 = 2Fe3++2H2O
高三化学选择题困难题查看答案及解析
高三化学解答题中等难度题查看答案及解析
(14分)废旧电池乱扔不仅污染环境,更是一种资源的浪费。普通锌锰干电池是圆筒形的,外筒由锌制成,筒中央为碳棒,筒内黑色糊状物主要成分是淀粉、氯化铵、氯化锌和二氧化锰等。某研究性学习小组设计如下流程,变废为宝:
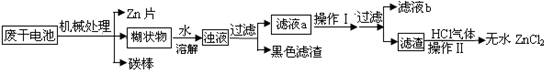
(1) “溶解”步骤中,为提高溶解速度,可采取的措施有加热、________等;
“操作Ⅰ”的名称是;
(2)检验“滤液b”中含有NH4+的方法是。
(3) 某同学将黑色滤渣与足量的浓盐酸充分反应后的液体进行过滤,得到的滤渣还是黑色,该黑色物质在热的浓硫酸中能完全消失,则该黑色物质与浓硫酸反应的化学方程式为 ________。
(4) 二氧化锰还可大量用于炼钢、有机合成工业等。在制备高纯二氧化锰过程中,用FeSO4、稀H2SO4对软锰矿(主要成分为MnO2)进行酸浸富集锰元素生成Mn2+,写出酸浸时发生反应的离子方程式_________________________。
(5) 已知:SOCl2极易与水发生下列反应:SOCl2+H2O=SO2+2HCl。有人用SOCl2代替“操作Ⅱ”中的HCl气体,使其与ZnCl2·xH2O混合加热制取无水氯化锌,请你对使用SOCl2试剂作个评价。
高三化学填空题中等难度题查看答案及解析
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:

已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
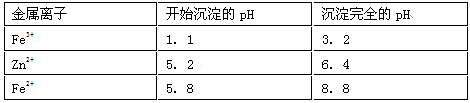
(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 (选填序号:a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 。
(3)氯化锌能催化乳酸()生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。
高三化学实验题极难题查看答案及解析
以炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,制取氯化锌晶体(ZnCl2·xH2O)的工艺流程如图: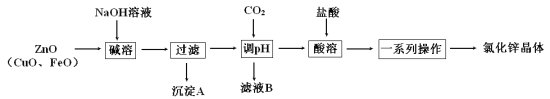
已知:Zn及其化合物的性质与Al及其化合物的性质相似,pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。
(1)碱溶时加入过量NaOH溶液的目的是___,发生反应的化学方程式是___。
(2)沉淀A的主要成分的化学式是___。
(3) “调pH”步骤中通入过量CO2,化学反应方程式___。
(4)酸溶时发生反应的离子方程式是___。
(5)一系列操作过程中的一系列操作是:___、___、过滤、洗涤、干燥。
高三化学综合题中等难度题查看答案及解析
锌锰干电池的负极材料是电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生Mn2O3。利用废旧电池回收Zn、Mn化合物,对环境保护意义重大。
步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得到固体和滤液。
步骤二:处理固体,提取MnO2通过对获得的滤渣进行灼烧,灼烧的目的是__。灼烧时用到的实验仪器有酒精灯、玻璃棒、__。
步骤三:处理滤液,得到ZnCl2·xH2O晶体,再通过将SOCl2与ZnCl2·xH2O晶体混合可制取无水ZnCl2。有关的实验装置如图(夹持及加热装置略):
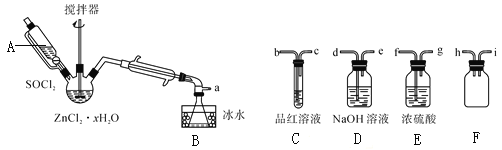
已知:SOCl2是一种常用的脱水剂,熔点-105℃,沸点79℃。140℃以上易分解,与水剧烈反应生成两种气体。
①仪器A的名称为__。
②蒸馏烧瓶中发生反应的化学方程式为:__。
③为回收剩余的SOCl2并验证生成物中含有SO2。上述仪器接目的连接响序为a→__。装置E中浓硫酸的作用___。
④为提高SOCl2的利用率,该实验宜采用的加热方式为__。
⑤讨论:将ZnCl2·xH2O晶体置于坩埚中加热均烧,__(能,不能)得到无水ZnCl2,原因是__。
高三化学实验题困难题查看答案及解析
普通锌锰干电池的简图(下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:Zn+2NH4++2MnO2=[Zn(NH3)2]2++Mn2O3+H2O
关于锌锰干电池的下列说法中正确的是
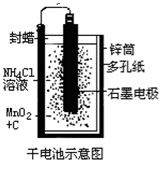
A.当该电池电压逐渐下降后,利用电解原理能重新充电复原
B.电池负极的电极反应式为:2MnO2+2NH4++2e- = Mn2O3+2NH3+H2O
C.该电池碳棒可用铜棒代替,但是工作电压会下降
D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5g
高三化学选择题困难题查看答案及解析
将废旧锌锰电池处理得到含锰混合物,既能减少它对环境的污染,又能实现废电池的资源化利用。
Ⅰ. 回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
(1)写出MnO(OH)与浓盐酸反应的化学方程式:_________。
Ⅱ. 锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH + MnO2 + 2H2C2O4 + 3H2SO4 == 3MnSO4 + 4CO2↑ + 6H2O
(2)与使用浓盐酸回收锰相比,新方法的优点是_________(答1点即可)。
(3)欲以MnSO4溶液为原料制备MnCO3,选用的加料方式___________(填字母),原因是___________。
已知:Ksp(MnCO3)=2.3×10﹣11、Ksp[Mn(OH)2]=2.1×10﹣13
a. 将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b. 将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c. 将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d. 以上三种方式都无法得到MnCO3.
Ⅲ. 现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示:
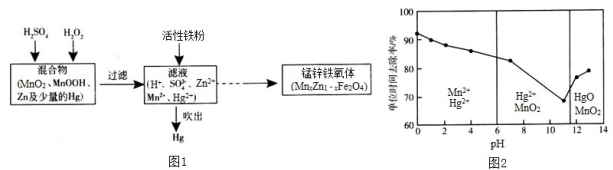
请回答下列问题:
(4)MnxZn1﹣xFe2O4中铁元素化合价为+3,则锰元素的化合价为___________。
(5)活性铁粉除汞时,铁粉的作用是_________(填“氧化剂”或“还原剂”)。
(6)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为__________________。
(7)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的。在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图2所示:
①写出pH=10时KMnO4溶液吸收汞蒸气的离子方程式________________。
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是__________________。
高三化学填空题困难题查看答案及解析
废旧锌锰电池回收处理,既能减少它对环境的污染,又能实现废电池的资源化利用。
(1)回收二氯化锰。将废旧锌锰电池处理,得到含MnO(OH)混合物,向该混合物加入浓盐酸并加热,试写出MnO(OH)与浓盐酸反应的化学方程式: 。
(2)制备锰锌铁氧体。锰锌铁氧体可用作隐形飞机吸收雷达波的涂料。一种以锌锰废电池为原料制备锰锌铁氧体的主要流程如下:
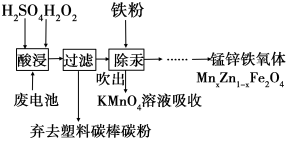
除汞时,铁粉的作用是______________ _(填“氧化剂”或“还原剂”或“吸附剂”);MnxZn1-xFe2O4中Fe元素为+3价,则Mn元素的化合价为 。
(3)在不同pH下,KMnO4溶液对Hg的吸收率的影响及主要产物如下图。
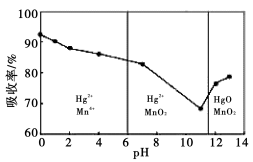
据图说明pH对Hg吸收率的影响规律 ;在强酸性环境下Hg的吸收率高的原因可能是 。
(4)锰回收新方法。向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。其主要反应为:2MnO(OH)+ MnO2+2H2C2O4 +3H2SO4 = 3MnSO4+ 4CO2↑+6H2O
①每1molMnO2参加反应时,共有 mol电子发生转移。
②新方法的优点是 (答1点即可)。
高三化学填空题困难题查看答案及解析
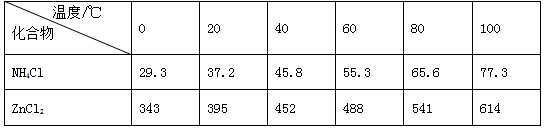
(14分)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100g水)
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的负极为 ,正极反应式为 ,
(2)维持电流强度为0.5A,电池工作5分钟,理论消耗Zn g(已知F=96500C/mol)。
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以通过 分离回收,滤渣的主要成分是二氧化锰、 和 ,欲从中得到较纯的二氧化锰,最简便的方法是 ,其原理是 。
(4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为 加碱调节PH为 ,铁刚好完全沉淀(离子浓度≤1×10-5mo1·L-1时即可认为离子沉淀完全)继续加碱调节PH为 锌开始沉淀(假定此时溶液中Zn2+的浓度为0.1 mo1·L-1)。若上述过程不加双氧水的后果 ,原因是 。
高三化学填空题困难题查看答案及解析