-
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H= + 571.2 kJ・mol—1
BaS(s)= Ba(s)+S(s) △H= +460 kJ・mol—1
已知:2C(s)+O2(g)=2CO(g) △H= -221 kJ・mol—1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) △H= ________________ 。
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料。已知As2S3和HNO3有如下反应:
As2S3+10H++ 10NO3-=2H3AsO4+3S+10NO2↑+ 2H2O
当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为 ________ ________ 。
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中主要含硫各物种(H2S、HS—、S2—)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如下图所示(忽略滴加过程H2S气体的逸出)。
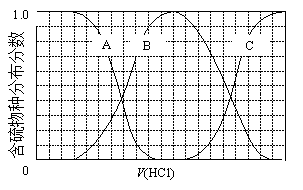
①含硫物种B表示 ________________。在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为 ________________(填字母)。
a.c(Na+)= c(H2S)+c(HS—)+2c(S2—)
b.2c(Na+)=c(H2S)+c(HS—)+c(S2—)
c.c(Na+)=3[c(H2S)+c(HS—)+c(S2—)]
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是 ________________ (用离子方程式表示)。
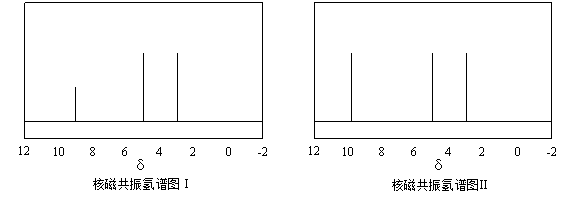
(4)硫的有机物( )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O。
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O。
 及X的核磁共振氢谱如下图,其中 ________________(填“Ⅰ”或“Ⅱ”)为
及X的核磁共振氢谱如下图,其中 ________________(填“Ⅰ”或“Ⅱ”)为 的核磁共振氢谱图。写出X的结构简式: ________________。
的核磁共振氢谱图。写出X的结构简式: ________________。
-
(12分)(Ⅰ)硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
①BaSO4(s)+4C(s)=BaS(s)+4CO(g) △H=+ 571.2 kJ・mol—1
②BaS(s)=Ba(s)+S(s) △H=+460 kJ・mol—1
已知:③2C(s)+O2(g)=2CO(g) △H= -221 kJ・mol—1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) △H= 。
(Ⅱ)污染与环境保护已经成为现在我国最热门的一个课题,污染分为空气污染,水污染,土壤污染等。
(1)为了减少空气中SO2的排放,常采取的措施就洗涤含SO2的烟气。以下物质可作洗涤剂的是 (选填序号)。
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(2)为了减少空气中的CO2,目前捕碳技术在降低温室气体排放中具有重要的作用,捕碳剂常用(NH4)2CO3,反应为:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3 (aq) ΔH3为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,其关系如图

则:
①△H3 0(填“>”、“=”或“<”)。
②在T4~T5这个温度区间,容器内CO2气体浓度变化趋势的原因是: 。
(3)催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化反硝化法中,用H2将NO3-还原为N2,一段时间后,溶液的碱性明显增强。则反应离子方程式为: 。
②电化学降解NO3-的原理如图,阴极反应式为: 。

-
Ⅰ.硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)重晶石(BaSO4)高温锻烧可发生一系列反应,其中部分反应如下;
①BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
②BaS(s)=Ba(s)+S(s) ΔH=+460 kJ·mol-1
己知:③2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH =________________。
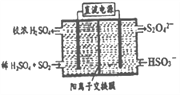
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。
①阳极的电极反应式为__________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成。该反应中氧化剂与还原剂的物质的量之比为________________。
Ⅱ.乙炔(C2H2)在气焊、气割及有机合成中用途非常广泛,可由电石(CaC2)直接水化法或甲烷在1500℃左右气相裂解法生产。哈斯特研究得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。
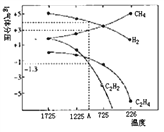
(3)T2℃时,向1L恒容密闭容器中充入0.3molCH4只发生反应2CH4(g) C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH____0(填“>”或“<”),CH4的平衡转化率为_________。
C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH____0(填“>”或“<”),CH4的平衡转化率为_________。
上述平衡状态某一时刻,若改变温度至T℃,CH4以0.01mol/(L·s)的平均速率增多,经ts后再次达到平衡,平衡时2c(C2H4) = c(CH4),则t=________s。
(4)列式计算反应2CH4(g) =C2H2(g)+3H2(g)在图中A点温度时的平衡常数K=_________ (用平衡分压代替平衡浓度计算:lg ≈-1.3)
≈-1.3)
-
(14分)硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式 。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图所示。电解时阳极区会产生气体,产生气体的原因是 。

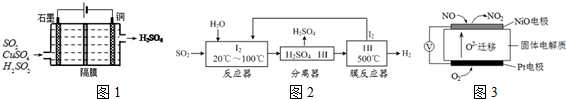
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
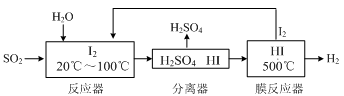
①用离子方程式表示反应器中发生的反应是 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 。
(3)氢化亚铜是一种红色固体,可由硫酸铜为原理制备
4CuSO4 + 3H3PO2 + 6H2O=4CuH↓ + 4H2SO4 + 3H3PO4 。
①该反应中还原剂是 (写化学式)。
②该反应每生成1molCuH,转移的电子物质的量为 。
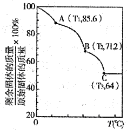
(4)硫酸铜晶体常用来制取波尔多液,加热时可以制备无水硫酸铜。将25.0 g胆矾晶体放在坩埚中加热测定晶体中结晶水的含量,固体质量随温度的升高而变化的曲线如下图。
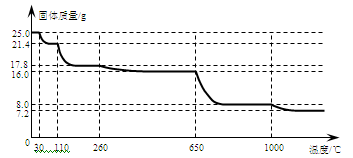
请分析上图,填写下列空白:
①30℃~110℃间所得固体的化学式是 ,
②650℃~1000℃间所得固体的化学式是 。
-
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)某科研小组用SO2为原料制取硫酸.
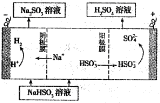
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触.请写出该电池的负极的电极反应式______________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸.电解原理示意图如图1所示.电解时阳极区会产生气体,产生气体的原因是____________。
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图2:
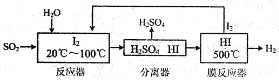
①用离子方程式表示反应器中发生的反应是______________。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是______________。
(3)氢化亚铜是一种红色固体,可由硫酸铜为原理制备4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
①该反应中氧化剂是______________(写化学式)。
②该反应每生成1molCuH,转移的电子物质的量为______________。
(4)硫酸铜晶体常用来制取波尔多液,加热时可以制备无水硫酸铜.右图是硫酸铜晶体受热分解图示。请写出A→B的方程式______________。
-
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用.
(1)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2nCu+(n+1)O2+(2﹣2n)H2O═2n CuSO4+(2﹣2n) H2SO4从环境保护的角度看,催化脱硫的意义为 ;每吸收2molSO2,被SO2还原的O2的质量为 g.
②利用如图1所示电化学装置吸收另一部分SO2,并完成Cu的再生.写出装置内所发生反应的离子方程式 .
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图2:
①用离子方程式表示反应器中发生的反应是:
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 .
Ⅱ.汽车尾气是造成雾霾天气的重要原因之一.
已知氮的氧化物是汽车尾气的污染物,用如图3装置可监测其含量,电池中每转移0.4mole﹣,Pt 电极消耗 L氧气(标况下)该装置的负极反应式为 .
-
硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s) +4C(s)===BaS(s) +4CO(g) ΔH=+571.2 kJ·mol-1
BaS(s)===Ba(s)+S(s) ΔH=+460 kJ·mol-1
已知:2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
则:Ba(s)+S(s)+2O2(g)===BaSO4(s) ΔH=____________。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法:反应原理:恒温恒容时2C(s)+2SO2(g)  S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
反应进行到不同时间测得各物质的浓度如图:
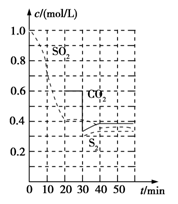
①0~20 min反应速率表示为v(SO2)=____________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是____________;
③平衡常数的表达式K=____________。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是____________(填序号)。
a.c(Na+)+c(H+)>c(S )+c(HS
)+c(HS )+c(OH-)
)+c(OH-)
b.c(Na+)=c(S )+c(HS
)+c(HS )+c(H2SO3)
)+c(H2SO3)
c.c(Na+)>c(HS )>c(H+)>c(S
)>c(H+)>c(S )
)
d.水电离出c(H+)=1×10-8 mol/L
(3)电化学处理法
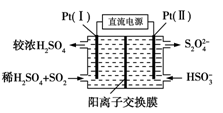
①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加________mol离子。
-
硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)===BaS(s)+4CO(g) ΔH=+571.2 kJ·mol-1
BaS(s)===Ba(s)+S(s) ΔH=+460 kJ·mol-1
已知:2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
则:Ba(s)+S(s)+2O2(g)===BaSO4(s) ΔH=________。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法
反应原理:恒温恒容时2C(s)+2SO2(g) S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
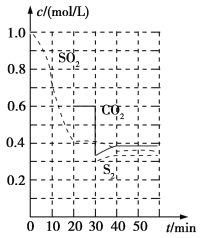
反应进行到不同时间测得各物质的浓度部分图像如图:
①0~20 min反应速率表示为v(SO2)=________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是________;
③40 min时,平衡常数K=________。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是________(填序号)。
a.c(Na+)+c(H+)>c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
b.水电离出c(H+)=1×10-8 mol/L
c.c(Na+)>c(HSO )>c(H+)>c(SO
)>c(H+)>c(SO )
)
(3)电化学处理法
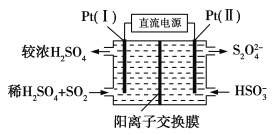
①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加________mol离子。
-
硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2kJ·mol-1
BaS(s)=Ba(s)+S(s) ΔH=+460kJ·mol-1
已知:2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s)ΔH=__。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法
反应原理:恒温恒容时2C(s)+2SO2(g)=S2(g)+2CO2(g)。
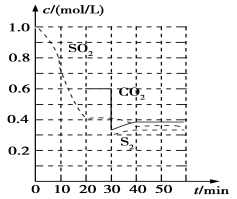
反应进行到不同时间测得各物质的浓度如图:
①0~20min反应速率表示为v(SO2)=__;
②30min时,改变某一条件平衡发生移动,则改变的条件最有可能是__;
③40min时,平衡常数K=__。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是__(填序号)。
a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-)
b.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
c.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
d.溶液中c(H+)=1×10-8mol/L
(3)电化学处理法
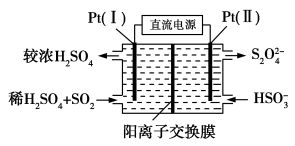
①如图所示,Pt(Ⅰ)电极的反应式为__;
②当电路中转移0.02mole-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加__mol离子。
-
硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)  BaS(s)+4CO(g) ΔH=+571.2 kJ·mol−1
BaS(s)+4CO(g) ΔH=+571.2 kJ·mol−1
BaS(s)  Ba(s)+S(s) ΔH=+460 kJ·mol−1
Ba(s)+S(s) ΔH=+460 kJ·mol−1
已知:2C(s)+O2(g)  2CO(g) ΔH=−221 kJ·mol−1
2CO(g) ΔH=−221 kJ·mol−1
则:Ba(s)+S(s)+2O2(g)  BaSO4(s) ΔH=_____________。
BaSO4(s) ΔH=_____________。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法
反应原理:恒温恒容时2C(s)+2SO2(g) S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
反应进行到不同时间测得各物质的浓度部分图象如图:
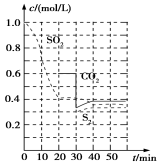
①0~20 min反应速率表示为v(SO2)=________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是________;
③40 min时,平衡常数K=________。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是________(填序号)。
a.c(Na+)+c(H+)>c( )+c(
)+c( )+c(OH−)
)+c(OH−)
b.水电离出c(H+)=1×10−8 mol/L
c.c(Na+)>c( )>c(H+)>c(
)>c(H+)>c( )
)
(3)电化学处理法
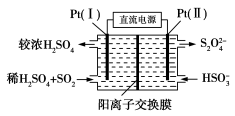
①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e−时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加____mol离子。


C2H4(g)+2H2(g) ΔH,达到平衡时,测得c(C2H4)= c(CH4)。该反应的ΔH____0(填“>”或“<”),CH4的平衡转化率为_________。
≈-1.3)


















