-
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
实验序号
样品的质量/g
NaOH溶液的体积/mL
氨气的体积/L
Ⅰ
7.4
40.00
1.68
Ⅱ
14.8
40.00
3.36
Ⅲ
22.2
40.00
1.12
Ⅳ
37.0
40.00
0
(1)测定过程中有关反应的离子方程式为
_____________________________________。
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为__________L。
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4)欲计算该NaOH溶液的物质的量浓度应选择第______组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程。
高三化学计算题简单题查看答案及解析
-
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
实验序号
样品的质量/g
NaOH溶液的体积/mL
氨气的体积/L
Ⅰ
7.4
40.00
1.68
Ⅱ
14.8
40.00
3.36
Ⅲ
22.2
40.00
1.12
Ⅳ
37.0
40.00
0
(1) 测定过程中有关反应的离子方程式为
______________________________________。
(2) 3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为__________L。
(3) 试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4) 欲计算该NaOH溶液的物质的量浓度应选择第______组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程。
高三化学计算题中等难度题查看答案及解析
-
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
实验序号
样品的质量/g
NaOH溶液的体积/mL
氨气的体积/L
Ⅰ
7.4
40.00
1.68
Ⅱ
14.8
40.00
3.36
Ⅲ
22.2
40.00
1.12
Ⅳ
37.0
40.00
0
(1) 测定过程中有关反应的离子方程式为
______________________________________。
(2) 3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为__________L。
(3) 试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4) 欲计算该NaOH溶液的物质的量浓度应选择第______组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程。
高三化学计算题困难题查看答案及解析
-
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。
为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00 mL,加热至1200C左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(气体体积均折算到标准状况的体积):
实验序号
样品质量(克)
NaOH溶液的体积(mL)
氨气的体积(L)
Ⅰ
7.4
40.00
1.68
Ⅱ
14.8
40.00
3.36
Ⅲ
22.2
40.00
1.12
Ⅳ
37.0
40.00
0.00
(1)实验过程中有关反应的离子方程式为:
________;________。
(2)计算用1.85克样品进行同样实验时,生成氨气在标准状况的体积为________L
(3)计算确定该混合物中(NH4)2SO4和NH4HSO4的物质的量之比________。
(4)欲计算该NaOH溶液的物质的量浓度应选择第________组数据,由此求得NaOH溶液的物质的量浓度为。
高三化学计算题困难题查看答案及解析
-
工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气.某校化学兴趣小组的同学为确定该方法所得固体的成分,称取该固体四份,溶于水后,分别逐滴加入相同浓度的硫酸溶液50mL,产生SO2的体积(标准状况)如下表(实验时设法使水中溶解的SO2几乎完全逸出):
(1)上述四组实验中,SO2体积与固体的质量之比相同的组别有______;由第①组实验中的SO2体积与固体的质量之比,可以推算用6.945g该固体进行同样的实验时,产生SO2______mL(标准状况);根据表中______两组数据变化可确认该固体中一定含有(NH4)2SO3.实验组别 ① ② ③ ④ 硫酸溶液的体积(mL) 50 50 50 50 盐的质量(g) 9.260 13.890 20.835 32.410 二氧化硫的体积(mL) 1344 2016 3024 2464
(2)另取9.260g该固体与足量的熟石灰共热,收集到标准状况的氨气的体积为3136mL,则该固体的成分除(NH4)2SO3外还有______(填化学式),该实验中使用的硫酸的物质的量浓度为______.高三化学解答题中等难度题查看答案及解析
-
(15分)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。某校化学兴趣小组的同学为确定该方法所得固体的成分,称取该固体四份,溶于水后,分别逐滴加入相同浓度的硫酸溶液50 mL,产生SO2的体积(标准状况)如下表(实验时设法使水中溶解的SO2几乎完全逸出):
实验组别
①
②
③
④
硫酸溶液的体积(mL)
50
50
50
50
盐的质量(g)
9.260
13.890
20.835
32.410
二氧化硫的体积(mL)
1344
2016
3024
2464
⑴上述四组实验中,SO2体积与固体的质量之比相同的组别有__________________;由第①组实验中的SO2体积与固体的质量之比,可以推算用6.945 g该固体进行同样的实验时,产生SO2_________mL(标准状况);根据表中________两组数据变化可确认该固体中一定含有(NH4)2SO3。
⑵另取9.260 g该固体与足量的熟石灰共热,收集到标准状况的氨气的体积为3136 mL,则该固体的成分除(NH4)2SO3外还有___________(填化学式),该实验中使用的硫酸的物质的量浓度为_______________。
高三化学计算题简单题查看答案及解析
-
(16分)回收利用炼铜工业产生的排放物,既能节约资源,又能保护环境。
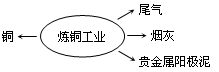
(1)用氨水吸收尾气中的SO2后,再加入硫酸,可获得SO2
和(NH4)2SO4两种产品。相关反应的化学方程式为________、________。
(2)烟灰中金属元素以硫酸盐和氧化物形态存在,其中锌、铅的含量最大,其次为铜、铁等。烟灰的回收利用工艺如下:
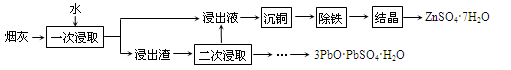
①“沉铜”可得到单质铜,该步骤应加入的试剂是________。
②“一次浸取”铜浸出率较低,原因是烟灰中部分铜元素以________(填化学式)残留在浸出渣中,“二次浸取”应选择_________(填化学式)作浸取剂。
(3)从贵金属阳极泥中可提取粗银。电解法精炼粗银时采用AgNO3和HNO3的混合液作电解液,阴极的主要电极反应式为________。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为________。
高三化学简答题困难题查看答案及解析
-
回收利用炼铜工业产生的排放物,既能节约资源,又能保护环境.
(1)用足量氨水吸收尾气中的SO2后,再加入硫酸,可获得SO2和(NH4)2SO4两种产品.相关反应的化学方程式为________、________.

(2)烟灰中金属元素以硫酸盐和氧化物形态存在,其中锌、铅的含量最大,其次为铜、铁等.烟灰的回收利用工艺如下:
①“沉铜”可得到单质铜,该步骤应加入的试剂是________.
② “一次浸取”铜浸出率较低,原因是烟灰中部分铜元素以________(填化学式)残留在浸出渣中,“二次浸取”应选择_________(填化学式)作浸取剂.
(3)从贵金属阳极泥中可提取粗银.电解法精炼粗银时采用AgNO3和HNO3的混合液作电解液,阴极的主要电极反应式为________.阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为________.
高三化学综合题困难题查看答案及解析
-
(15分)
硫酸工厂排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前必需进行尾气处理并设法进行综合利用。
⑴硫酸工厂排放尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理。
①写出上述过程的化学反应方程式:________,________
②请说出这种尾气处理方法的优点(说出两点即可)________
③若某硫酸厂每天排放的1万米3。(标准状况)尾气中含0.2%(体积百分数)的SO2,通过上述方法处理,理论上需生石灰________kg。
⑵近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法,该方法:第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
这种尾气处理方法与(1)相比的优点是________。
⑶某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法;其中阴阳膜组合循环再生机理如图,a、b离子交换膜将电解槽分为三个。区域,电极材料为石墨。
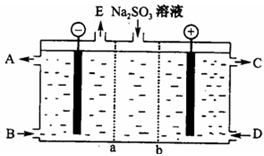
①图中a表示________离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品,其中C为硫酸,则A表示________,E表示________。
②阳极的电极反应式为________。
高三化学填空题中等难度题查看答案及解析
-
[化学一一选修化学与技术](15分)
硫酸工厂排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前必需进行尾气处理并设法进行综合利用。
(1)硫酸工厂排放尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理。
①写出上述过程的化学反应方程式:
________,________
②请说出这种尾气处理方法的优点(说出两点即可)
________
③若某硫酸厂每天排放的1万米3。(标准状况)尾气中含0.2%(体积百分数)的SO2,通过上述方法处理,理论上需生石灰________kg。
(2)近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法,该方法:第一步是用Na2SO3水溶液吸收SO2,第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。
这种尾气处理方法与(1)相比的优点是________。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO。溶液进行电解循环再生,这种新工艺叫再生循环脱硫法;其中阴阳膜组合循环再生机理如A图,a、b离子交换膜将电解槽分为三个。区域,电极材料为石墨。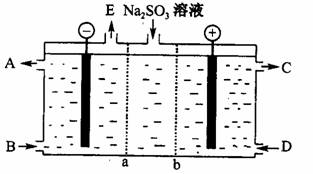
①图中a表示________离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品,其中C为硫酸,则A表示________,E表示________。
②阳极的电极反应式为________。
高三化学填空题中等难度题查看答案及解析